Свойства льда для его модификаций
Сообщение:
Здравствуйте, Олег, я студент второго курса Кузбасского государственного технического института, занимаюсь научной работой. И передо мной встала проблема: я не могу нигде найти свойства льда для всех его модификаций (уд. теплота плавления, уд. сопротивление, скорость распространения поперечных и продольных звуковых волн, коэф. поглощения этих волн, склонность к трещинообразованим, а также механические свойства). Не могли бы Вы "подкинуть" мне известную вам информацию по данным вопросам, за что я буду вам искренне благодарен.
Здравствуйте, Дмитрий.
К сожалению такой полной информации по физико-механическим свойствам я не располагаю, поскольку я специально не занимался изучением льда и его свойств. Всё что мне известно по данной тематике, привожу ниже:
В природе известны 14 модификаций льда. Правда, все, кроме привычного нам льда, кристаллизующего в гексагональной сингонии и обозначающегося как лёд I , образуются в условиях экзотических — при очень низких температурах (порядка -110150 0С) и высоких давлениях, когда углы водородных связей в молекуле воды изменяются и образуются системы, отличные от гексагональной. Такие условия напоминают космические и не встречаются на Земле. Например, при температуре ниже –110 °С водяные пары выпадают на металлической пластине в виде октаэдров и кубиков размером в несколько нанометров — это так называемый кубический лед. Если температура чуть выше –110 °С, а концентрация пара очень мала, на пластине формируется слой исключительно плотного аморфного льда.
Некоторые данные о структурных модификациях льда, температуре, давлении, плотности и диалектрической проницаемости показаны в Таблице 1 и Таблице 2.
Табл. 1. — Некоторые данные о структурах модификаций льда
Модифи
кация
Сингония
Фёдоровская группа
Длины водородных связей,
Углы О—О—О в тетраэдрах
I
Ic
II
III
V
VI
VII
VIII
IX
Гексагональная
Кубическая
Тригональная
Тетрагональная
Моноклинная
Тетрагональная
Кубическая
Кубическая
Тетрагональная
P63/mmc
F43m
R3
P41212
A2/a
P42/nmc
Im3m
Im3m
P41212
2,76
2,76
2,75—2,84
2,76—2,8
2,76—2,87
2,79—2,82
2,86
2,86
2,76—2,8
109,5
109,5
80—128
87—141
84—135
76—128
109,5
109,5
87—141
Примечание. 1 A=10-10 м.
Табл. 2. — Температура, давление, плотность и диэлектрическая проницаемость различных льдов
Модификация
Темп-ра, °С
Давление, Мн/м2
Плотность, г/см2
Диэлектрическая проницаемость
I
Ic
II
III
V
VI
VII
VIII
IX
0
—130
—35
—22
—5
15
25
—50
—110
0,1
0,1
210
200
530
800
2500
2500
230
0,92
0,93
1,18
1,15
1,26
1,34
1,65
1,66
1,16
94
—
3,7
117
144
193
~150
~3
~4
Кристаллы всех модификаций льда построены из молекул воды H2O, соединённых водородными связями в трёхмерный каркас (рис. 1). Молекулу воды можно упрощенно представить себе в виде тетраэдра (пирамиды с треугольным основанием). В её центре находится атом кислорода, в двух вершинах — по атому водорода, электроны которых задействованы в образовании ковалентной связи с кислородом. Две оставшиеся вершины занимают пары валентных электронов кислорода, которые не участвуют в образовании внутримолекулярных связей, поэтому их называют неподеленными.
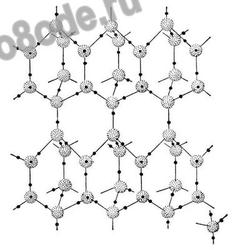
Рис.1. Структура льда I.
Наиболее изученным является лёд I-й природной модификации. В структуре льда каждая молекула воды участвует в 4 связях, направленных к вершинам тетраэдра. При взаимодействии протона одной молекулы с парой неподеленных электронов кислорода другой молекулы возникает водородная связь, менее сильная, чем связь внутримолекулярная, но достаточно могущественная, чтобы удерживать рядом соседние молекулы воды. Каждая молекула может одновременно образовывать четыре водородные связи с другими молекулами под строго определенными углами, равными 109°28', направленных к вершинам тетраэдра, которые не позволяют при замерзании создавать плотную структуру. При этом в структурах льда I, Ic, VII и VIII этот тетраэдр правильный. В структурах льда II, III, V и VI тетраэдры заметно искажены. В структурах льда VI, VII и VIII можно выделить 2 взаимоперекрещивающиеся системы водородных связей. Этот невидимый каркас из водородных связей располагает молекулы в виде сетчатой сетки, по структуре напоминающей соты с полыми каналами. Если лед нагреть, сетчатая структура разрушится: молекулы воды начинают проваливаться в пустоты сетки, приводя к более плотной структуре жидкости, — поэтому вода тяжелее льда.
Многое в структуре льда и его свойствах выглядит необычно. В узлах кристаллической решетки льда атомы кислорода выстроены упорядоченно, образуя правильные шестиугольники, а атомы водорода занимают самые разные положения вдоль связей. Поэтому возможны 6 эквивалентных ориентаций молекул воды относительно их соседей. Часть из них исключается, поскольку нахождение одновременно 2 протонов на одной водородной связи маловероятно, но остаётся достаточная неопределённость в ориентации молекул воды. Такое поведение атомов нетипично, поскольку в твердом веществе все подчиняются одному закону: либо все атомы расположены упорядоченно, и тогда это — кристалл, либо случайно, и тогда это — аморфное вещество. Такая необычная структура может реализоваться в большинстве модификаций льда — I, III, V, VI и VII (и по-видимому в Ic), а в структуре льда II, VIII и IX молекулы воды ориентационно упорядочены. По выражению Дж. Бернала лёд кристалличен в отношении атомов кислорода и стеклообразен в отношении атомов водорода.
Всё же обычный лёд, который образуется при атмосферном давлении и плавится при 0 °С, — самое привычное, но всё же до конца не понятное вещество. В связи с широким распространением воды и льда на Земле отличие свойств льда от свойств других веществ играет важную роль в природных процессах. Вследствие меньшей, чем у воды, плотности лёд образует на поверхности воды плавучий покров, предохраняющий реки и водоёмы от донного замерзания. Зависимость между скоростью течения и напряжением у поликристаллического льда гиперболическая; при приближённом описании её степенным уравнением показатель степени увеличивается по мере роста напряжения.
Кроме того, скорость течения льда прямо пропорциональна энергии активации и обратно пропорциональна абсолютной температуре, так что с понижением температуры лёд приближается по своим свойствам к абсолютно твёрдому телу. В среднем при близкой к таянию температуре текучесть льда в 106 раз выше, чем у горных пород. Благодаря своей текучести лёд не накопляется в одном месте, а в виде ледников постоянно перемещается.
Лед трудно расплавить, как бы ни странно это звучало. Не будь водородных связей, сцепляющих молекулы воды, он плавился бы при –90°С. При этом, замерзая, вода не уменьшается в объеме, как это происходит с большинством известных веществ, а увеличивается — за счет образования сетчатой структуры льда.
Вследствие очень высокой отражательной способности льда (0,45) и снега (до 0,95) покрытая ими площадь — в среднем за год около 72 млн. км2 в высоких и средних широтах обоих полушарий — получает солнечного тепла на 65% меньше нормы и является мощным источником охлаждения земной поверхности, чем в значительной мере обусловлена современная широтная климатическая зональность. Летом в полярных областях солнечная радиация больше, чем в экваториальном поясе, тем не менее температура остаётся низкой, т. к. значительная часть поглощаемого тепла затрачивается на таяние льда, имеющего очень высокую теплоту таяния.
К другим необычным свойствам льда относят и генерацию электромагнитного излучения его растущими кристаллами. Известно, что большинство растворенных в воде примесей не передается льду, когда он начинает расти; они вымораживается. Поэтому даже на самой грязной луже пленка льда чистая и прозрачная. При этом примеси скапливаются на границе твердой и жидкой сред, в виде двух слоев электрических зарядов разного знака, которые вызывают значительную разность потенциалов. Заряженный слой примесей перемещается вместе с нижней границей молодого льда и излучает электромагнитные волны. Благодаря этому процесс кристаллизации можно наблюдать в деталях. Так, кристалл, растущий в длину в виде иголки, излучает иначе, чем покрывающийся боковыми отростками, а излучение растущих зерен отличается от того, что возникает, когда кристаллы трескаются. По форме, последовательности, частоте и амплитуде импульсов излучения можно определить, с какой скоростью замерзает лед и какая при этом получается ледовая структура.
Табл. 3. — Некоторые свойства льда I
Свойство
Значение
Примечание
Теплоемкость, кал/(г··°C) Теплота таяния, кал/г Теплота парообразования, кал/г
0,51 (0°C) 79,69 677
Сильно уменьшается с понижением температуры
Коэффициент термического расширения, 1/°C
9,1·10—5 (0°C)
Теплопроводность, кал/(см сек··°C)
4,99·10—3
Показатель преломления: для обыкновенного луча для необыкновенного луча
1,309 (—3°C) 1,3104 (—3°C)
Удельная электрическая проводимость, ом—1·см—1
10—9 (0°C)
Кажущаяся энергия активации 11ккал/моль
Поверхностная электропроводность, ом—1
10—10 (—11°C)
Кажущаяся энергия активации 32ккал/моль
Модуль Юнга, дин/см
9·1010 (—5°C)
Поликристаллич. лёд
Сопротивление, Мн/м2 : раздавливанию разрыву срезу
2,5 1,11 0,57
Поликристаллический лёд Поликристаллический лёд Поликристаллический лёд
Средняя эффективная вязкость, пз
1014
Поликристаллический лёд
Показатель степени степенного закона течения
3
Энергия активации при деформировании и механической релаксации, ккал/моль
11,44—21,3
Линейно растет на 0,0361 ккал/(моль·°C) от 0 до 273,16 К
Примечание. 1 кал/(г°С)=4,186 кджl (kг (К); 1 ом-1см-1=100 сим/м; 1 дин/см=10-3н/м; 1 кал/(см (сек°С)=418,68 вт/(м (К); 1 пз=10-1 н (сек/м2.
Природный лёд I обычно значительно чище, чем вода, т.к. растворимость веществ (кроме NH4F) во льде крайне низкая. А вот лёд II наоборот стабилизуется только в присутствии следовых количеств газов; в чистом виде его никто не получал из-за его нестабильности. Если, например, давление создают с помощью гелия, он обязательно растворится в замерзающей воде. Есть сведения, что аргон — другой инертный газ, пригодный для использования в этой установке, — тоже способен давать со льдом твёрдые растворы. Однако изучением таких клатратных соединений льда с благородными газами специально никто не занимался.
Лёд II, III и V-й модификации длительное время сохраняются при атмосферном давлении, если температура не превышает —170°С. При нагревании приблизительно до —150°С лёд превращаются в кубический лёд Ic.
Расположен лёд II на диаграмме состояния между льдом III и льдом IX. Они различаются между собой упорядочением протонов, кислородный же каркас у них одинаков: спирали из одних молекул воды, как будто нанизанные на оси из других молекул воды. Когда же вероятности протона занять то или иное место равны, лёд будет неупорядоченным.
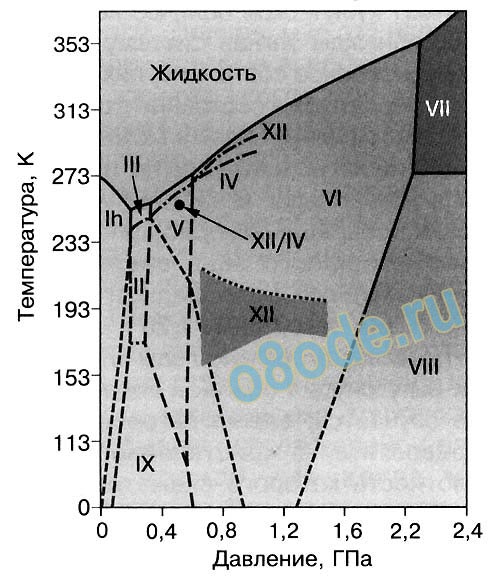
Рис. 2. Диаграмма состояния кристаллических льдов
Однако, все эксперименты с экзотическими льдами, как правило, связаны с их охлаждением до температур сухого льда, жидкого азота, а то и гелия, а также со сжатием до давления в тысячи атмосфер. Общее представление о результатах можно получить, глядя на рисунок, где показана диаграмма состояния кристаллических льдов.
Многие льды высокого давления можно сохранить и при нормальном давлении. Для этого их охлаждают в жидком азоте, а затем давление сбрасывают. Именно на таких закалённых льдах и были проведены основные исследования. Они показали, что их строение весьма разнообразно.
Структуру первого льда высокого давления, льда II, определили на заре исследований в этой области, когда появились первые мощные приборы для рентгеноструктурного в 1964 году. Как оказалось, этот лёд состоит из полых колонок, образованных шестизвенными гофрированными циклами. Каждая колонка окружена шестью такими же колонками, сдвинутыми друг относительно друга на треть периода. Структуру этого льда можно получить, если часть сот льда Ih развалить и превратить их в ажурные каркасы, связывающие остальные соты. При этом размер получившихся шестигранных каналов сильно увеличивается — именно у льда II самые широкие каналы, их диаметр составляет 3 Å. В таких каналах могут располагаться атомы гелия, неона и даже молекулы водорода.
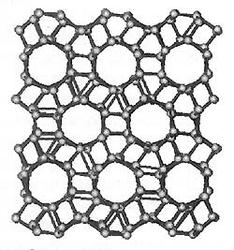
Рис. 3. Структура льда II
Получить гидраты благородного газа, например, гелия на основе льда II можно двумя способами. Во-первых, приложить (в атмосфере гелия) к воде давление в 0,28–0,5 ГПа и охладить её до 250–270К. Хотя в этой области диаграммы стабильны льды III и V, получится гидрат на основе льда II. Что интересно, протоны в нём уже упорядочены. (Обычно они упорядочиваются только при сильном охлаждении уже получившегося льда.)
Во-вторых, можно растворить гелий во льду Ih при низкой температуре и давлении 0,3 ГПа. Появление гелия приводит к расширению кристаллической решётки, и затем её нагрев до 180К помогает пройти структурному превращению.
Относительная лёгкость получения твёрдых растворов в льду II, а также его высокий потенциал в качестве хранилища газообразного водорода (одна молекула газа на шесть молекул воды) привлекают к нему внимание учёных-практиков: сейчас активно обсуждается возможность его применения в водородной энергетике.
При конденсации паров воды на более холодной подложке образуется аморфный лёд. Обе эти формы льда Лёд II и аморфный лёд могут самопроизвольно переходить в гексагональный лёд, причём тем скорее, чем выше температура.
Лёд IV-й модификации является метастабильной фазой льда. Он образуется гораздо легче и особенно стабилен, если давлению подвергается тяжёлая вода.
Кривая плавления льда V и VII исследована до давления 20 Гн/м2 (200 тыс. кгс/см2). При этом давлении лёд VII плавится при температуре 400°С.
Лёд VIII является низкотемпературной упорядоченной формой льда VII.
Лёд IX — метастабильная фаза, возникающая при переохлаждении льда III и по существу представляющая собой его низкотемпературную форму.
Впервые полиморфизм льда был обнаружен Г. Тамманом в 1900 г. и подробно изучен П. Бриджеменом в 1912 г. В табл. 3 и 4 приведены некоторые данные о структурах модификаций льда и некоторые их свойства.
Две последние модификации льда — XIII и XIV — открыли ученые из Оксфорда совсем недавно, в 2006 году. Предположение о том, что должны существовать кристаллы льда с моноклинной и ромбической решетками, было трудно подтвердить: вязкость воды при температуре –160°С очень высока, и собраться вместе молекулам чистой переохлажденной воды в таком количестве, чтобы образовался зародыш кристалла, трудно. Этого удалось достичь с помощью катализатора — соляной кислоты, которая повысила подвижность молекул воды при низких температурах. В земной природе подобные модификации льда образовываться не могут, но они могут встречаться на замерзших спутниках других планет.
НЕКОТОРЫЕ ФИЗИКО-МЕХАНИЧЕСКИЕ СВОЙСТВА ЛЬДА.
Устойчивость льда – это многофакторный феномен, зависящий от многих факторов, которые нужно учитывать при расчётах:
ТВЕРДОСТЬ ЛЬДА. Способность льда оказывать сопротивление проникновению другого тела, не получающего остаточных деформаций. Определяется как отношение действующей нагрузки Р к поверхности образовавшейся вмятины S. Твердость Н = P/S является средним значением давления во вмятине. В зависимости от температуры льда и времени приложения нагрузки (короткому времени соответствует динамическая твердость, длительному — статическая твердость) значения Н могут различаться более чем на порядок.
ТЕКСТУРА ЛЬДА. Особенность строения льда, обусловленная пространственными расположениями воздушных, минеральных и органических включений.
С учетом воздушных включений лед подразделяется на монолитный (лишенный видимых включений) и пористый (с наличием включений, которые могут иметь равномерное, слоистое и вертикально-волокнистое распределение).
По размеру включений лед подразделяется на мелкопузыристый (включения менее 0,2 мм), среднепузыристый (включения от 0,2 до 0,5 мм), крупнопузыристый (включения от 0,5 до 1,0 мм), крупно-полостной (включения более 1,0 мм).
Форма включений бывает овальная, трубчатая, ветвистая и трансформирующаяся. По происхождению включения подразделяются на первичные (аутогенные), вторичные (ксеногенные) и с нарушенной текстурой (катакластические).
ТЕМПЕРАТУРА ПЛАВЛЕНИЯ ЛЬДА. Температура, при которой происходит плавление льда при постоянном внешнем давлении. Плавление морского льда происходит не при определенной температуре, как у пресного льда, а непрерывно, начиная с момента, когда температура ниже 0°С до температуры замерзания морской воды данной солености.
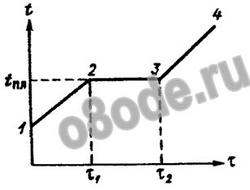
Ход температуры во льду во времени при подводе к нему теплоты
1 — 2 — нагревание льда; 2 — 3 — плавление льда: 3 — 4— нагревание воды; tпл —температура плавления льда.
Плавление льда при атмосферном давлении происходит при температуре 0,01°С (в практических расчетах принимают 0°С). Количество теплоты, которое необходимо сообщить 1 кг льда, находящемуся при температуре плавления, для превращения его в воду, называют удельной теплотой плавления Lпл. Удельная теплота плавления пресноводного льда при нормальных условиях равна удельной теплоте кристаллизации воды 33,3·104 Дж/кг.
ТЕМПЕРАТУРОПРОВОДНОСТЬ ЛЬДА (КОЭФФИЦИЕНТ ТЕМПЕРАТУРОПРОВОДНОСТИ). Параметр, характеризующий скорость изменения температуры льда в нестационарных тепловых процессах. Коэффициент температуропроводности льда
a = λ/Cpρ),
где Cp — удельная теплоемкость льда при постоянном давлении, ρ — плотность льда, λ— коэффициент теплопроводности, численно равен повышению температуры единицы объема льда в результате теплового потока, соответствующего коэффициенту теплопроводности Cp.
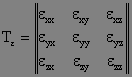
Деформированное состояние элемента льда считается известным, если известны компоненты тензора деформации льда.
ТЕОРЕТИЧЕСКАЯ ПРОЧНОСТЬ ЛЬДА. Свойство льда, которое характеризуется расчетным значением напряжения, при котором мог бы произойти одновременный разрыв всех межатомных связей на поверхности разрыва. Как и у других твердых тел, оценивается значением 0,1 Е, где Е — модуль Юнга льда.
Обычно фактические значения прочности на несколько порядков ниже теоретических. Причина низкой прочности льда — неравномерное распределение внутренних напряжений; межатомные связи нагружены неодинаково, а в атомной структуре тел имеются слабые места.
При сложении одноименных внешних и внутренних напряжений возникают локальные перенапряжения, которые могут достичь значений теоретической прочности, приводя к разрыву межатомных связей. В слабых местах структуры под действием больших локальных напряжений разрыв межатомных связей происходит очень легко—так зарождаются разрывы сплошности тела. Рост и слияние разрывов сплошности образует макроскопическую трещину, развитие которой приводит к разрушению тела. Теоретическую прочность также называют идеальной прочностью, плотностью сил когезии (т. е. сил молекулярного взаимодействия частей одного и того же тела) или просто когезией, которая может быть охарактеризована теплотой (работой) испарения.
ТЕПЛОЕМКОСТЬ ЛЬДА. Одна из основных термодинамических характеристик льда, отражающая степень его нагрева в результате количества теплоты, полученной льдом. В практических расчетах обычно используют удельную теплоемкость льда, понимая под этим количество теплоты, которое необходимо сообщить единице массы льда, чтобы повысить его температуру на 1 К. Теплоемкость пресноводного льда уменьшается с понижением температуры (от 2,12 кДж/(кг*К) при 0°С), стремясь к нулю при О К.
ТЕПЛОПРОВОДНОСТЬ ЛЬДА (КОЭФФИЦИЕНТ ТЕПЛОПРОВОДНОСТИ). Величина, характеризующая процесс переноса тепловой энергии в неравномерно нагретом льду, приводящий к выравниванию температуры. Теплопроводность является коэффициентом пропорциональности между плотностью теплового потока q и градиентом температуры Т, входящих в известное уравнение
q= - λ grad T.
Теплопроводность льда численно равна плотности теплового потока при разности температуры 1К на единицу расстояния. С понижением температуры теплопроводность возрастает. Согласно теоретическим расчетам и многочисленным экспериментальным данным, при температуре ~0°С теплопроводность пресноводного льда равна ~2,22 Вт/(м*К).
ТЕРМИЧЕСКОЕ РАЗРУШЕНИЕ. Разрушение ледяного покрова вследствие его таяния при повышении температуры воздуха. Термическое разрушение уменьшает прочность льда, изменяет его структуру и текстуру, сокращает горизонтальные размеры и др.
Внешними проявлениями термического разрушения ледяного покрова являются взлом и дробление льдов, фиксируемые следующими сроками их появления: дата начала весеннего взлома (день, когда произошел откол части припая, день появления первых признаков таяния и снижения его прочности); дата первой весенней подвижки припая (день, когда видимая площадь припая (за исключением его подошвы), расчлененного большим количеством трещин, испытала горизонтальный сдвиг, сохранив при этом взаимное положение блоков льда; дата окончательного разрушения припая (день, когда произошел распад припая на блоки льда, которые сместились относительно друг друга, понизив тем самым сплоченность льда).
ТРЕЩИНЫ В ЛЕДЯНОМ ПОКРОВЕ. Нарушения сплошности ледяного покрова, представляющие собой зону, в которой прекращается взаимодействие между ионами и атомами кристаллической решетки на разных ее сторонах. Образуются в результате разрыва или разлома, как результат превышения прочности льда на растяжение, сжатие, изгиб и сдвиг. Трещины в ледяном покрове подразделяются по генетическим и морфологическим признакам.
По морфологическим признакам трещины подразделяются на следующие виды.
По форме в плане их простирания — прямые (прямолинейные, клиновидные, щелевидные), изогнутые (дугообразные, кулисообразные, круговые), изломанные (зигзагообразные, синусоидные, циклоидные) (фото 38).
По форме разреза краев трещин—гладкие, неровные, зазубренные.
По длине—внутриблоковые (длиной до 5 км), межблоковые (длиной до 100 км), магистральные (длиной в несколько сотен километров).
По величине раскрытия—узкие (шириной до 5 м), средние (шириной от 5 до 15 м), широкие (шириной до 50 м).
По глубине проникновения — зияющие, нераскрывшиеся.
ТЕПЛОФИЗИЧЕСКИЕ (ТЕРМИЧЕСКИЕ) СВОЙСТВА ЛЬДА.
Свойства льда, определяющие условия теплопередачи и формирования температуры льда показаны в таблице 4.
Tаблица 4. Теплофизические свойства пресноводного льда
- t, 0С; сл, кДж/(кгК); ρ л, кг/м3; λл, Вт/(мК); ал 106, м2/с
- 0; 2,12; 916,4; 2,23; 1,2
- -5; 2,08; 917,4; 2,24; 1,2
- -10; 2,04; 918,2; 2,25; 1,2
- -15; 1,99; 919,1; 2,27; 1,24
- -20; 1,96; 919,96; 2,29; 1,3
- -25; 1,92; 920,8; 2,31; 1,3
- -30; 1,88; 920,8; 2,32; 1,34
Удельная теплота сублимации (возгонки) льда равна сумме удельной теплоты плавления льда и удельной теплоты испарения воды; при 0°С она равна Lвоз = 33,3·104 + 250·104 = 283,3·104 Дж/кг.
Коэффициент теплопроводности льда λ принимают в среднем равным 2,24Вт/(м·°С). С повышением температуры λ уменьшается незначительно и линейно.
Удельную теплоемкость льда вычисляют по формуле Б. П. Вейнберга:
c = 2,12 (1 + 0,0037t).
Учитывая, что при t=0°С плотность льда ρ = 917 кг/м3, а удельная теплоемкость его c = 2,12 кДж/(кг·°С), получаем коэффициент температуропроводности льда при нормальных условиях a = λ/(cρ)=2,24/(2,12·917) = 4,1·10-3 м2/ч. С понижением температуры коэффициент a существенно повышается, так как при этом не только увеличивается λ, но и уменьшается c:
a = 4,1(1 – 0,0063t) 10-3
Удельная теплота плавления (кристаллизации) морского льда в сильной степени зависит от его солености.
МОДУЛЬ УПРУГОСТИ ЛЬДА E при сжатии, растяжении и изгибе зависит от температуры и структуры льда и изменяется в очень широких пределах: от 0,12·1010 до 1·1010 Па. При сжатии его принимают в среднем равным 0,9·1010Па. Модуль упругости линейно уменьшается с повышением температуры.
МОДУЛЬ СДВИГА ЛЬДА G, так же как и модуль упругости E, зависит от температуры и структуры льда, но изменяется он не в столь большом диапазоне. В среднем его можно принять равным 3·109 Па.
Значения предела прочности льда, так называемое временное сопротивление льда, в различных условиях его напряженного состояния и при температуре, близкой к 0°С, приведены в таблице. С понижением температуры прочность льда увеличивается, а с повышением солености используемой воды — уменьшается.
Таблица 5. Значения предела прочности льда, Па
- Характер деформации; Ориентировка усилия; Обозначение; Реки Севера и Сибири; Реки европейской части России
- Сжатие; Перпендикулярно; Rсж; (45…65) 104; (25…40) 104
- Местное смятие; Перпендикулярно; Rсм; (110…150) 104; (55…80) 104
- Растяжение; Параллельно; Rр; (70…90) 104; (30…40) 104
- Срез; Параллельно; Rср; (40…60) 104; (20…30) 104
- Изгиб; Параллельно; Rиз; (45…65) 104; (25…40) 104
С уважением,
К.х.н. О.В. Мосин
На английском языке можно посмотреть сайты:
Ice Structure - о структуре льда. Аннотация статьи: Ice? A mineral is a naturally occurring inorganic chemical compound. What part of that definition doesn't apply to ice? Many mineralogy books list the properties of ice, not because anyone needs help identifying it, but for comparison with other materials. Steven Dutch, Natural and Applied Sciences.

At left is the phase diagram for water, ice, and vapor. Note, for those accustomed to seeing pressures in kilobars, that the pressure scale here is in millibars. The liquid-vapor curve predictably passes through 100 C and 1000 mb.
The liquid-ice curve actually has a slight negative slope, but it doesn't show at this scale. The melting point of ice actually decreases by about 1 degree per 100 bars pressure. At the deepest points in the ocean, pressures exceed one kilobar, where the freezing point of water would be about -10 C. Since the deep oceans are almost always at a temperature of 3-4 C, they are well above the freezing point.
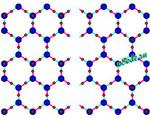
Ordinary Ice
Hydrogen Bonding and Proton Ordering.
The hydrogen atoms in a water molecule are about 108 degrees apart, which isjust about the right angle to build tetrahedral structures. The positivelycharged portion of one water molecule is attracted to the negatively chargedportion of a neighbor. This attraction, termed hydrogen bonding, giveswater many of its unique properties.
Here are two hypothetical networks of water molecules. Dark blue represents oxygen and red hydrogen. Magenta bonds are bonds within each water molecule, light blue bonds are hydrogen bonds between molecules.
Some bonds extend up or down out of the plane of the diagram. Hydrogen-Oxygen bonds extending up are shown by a hydrogen atom superimposed on the oxygen. If a water molecule is show with only one bond, the other extends down. Hydrogen bonds in and out of the plane of the diagram are not shown.
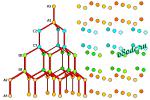
Cubic Ice (Ice Ic)
It is natural to wonder if a structure like ordinary ice, but based on acubic close packing arrangement, is possible. It is. The structure is shown.
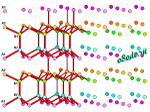
Ordinary ice consists of two interpenetrating lattices with a hexagonal closepacked stacking arrangement. The stacking arrangement is that of hexagonal closepacking, but the molecules themselves are not close packed. To construct atetrahedron of equal spheres with a fifth sphere in the center, the vertices ofthe tetrahedron must be about 3.27 radii apart.
The structure is shown below. The sets of layersare numbered 1 and 2 and colored for identification, with darker colors towardthe rear of the structure. Red lines show O-H-O links. Ordinary ice is called Ice Ih for reasons that will soon becomeobvious.
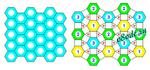
Ice II
Ice II is rhombohedral. It has similarities, not surprisingly, to Ice I inthat it consists of undulating six-membered rings joined to another ring belowit. However, neighboring rings do not form a complete hexagonal network butinstead surround threefold screw axes. The diagram below shows the rings in Ice I(left) and Ice II (right). Altitudes of rings around the screw axes areindicated on the right diagram. Since the rings enclose vacancies, the Ice IIstructure actually has less void space and is denser. The density is 1.17 gm/cc.
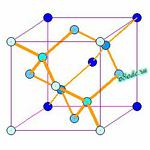
If the structure above looks familiar, it should. The oxygen atoms have the same arrangement as the carbon atoms in diamond. This form of ice is called Ice Ic.
At left is a cubic unit cell of Ice Ic, with only the oxygens shown. O-H-O links are in orange.
The diagram below shows the relationship of the cubic unit cell to the close packing layers.
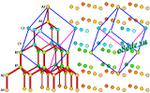
Ice Ic forms from the vapor below about -80 C and appears to be a metastableform of ice, although it has almost exactly the same density as Ice Ih. Ice Ihdoes not change to Ice Ic at very low temperatures but Ice Ic reverts readily toIce Ih when warmed above -80 C. Ice Ic may form in extremely high clouds andsome halo features not readily explainable in terms of hexagonal ice have beenattributed to Ice Ic.

The structure of Ice II is shown. There are two sets of rings withslightly differing degrees of undulation, shown in green and light blue. In terms ofc-axis dimensions, one set is centered on altitudes 0, 1/3, 2/3 and one, theother on 1/6, 1/2 and 5/6. The two sets alternate vertically and are clusteredaround three-fold screw axes. If we denote the two sets of rings as P and Q,then the rings are linked around each three-fold axis in the mannerP-Q-P-Q-P-Q-. Links in the two types of rings are red and purple, cross-linksare dark blue.

Ice III
Ice II is tetragonal. The unit cell is cubic in dimensions (6.83 Angstromunits on a side) but tetragonal in symmetry. The density is 1.14 gm/cc. The tetrahedral O-H-O links aresomewhat distorted. In the diagram below, oxygen atoms are shown in blue withlarger atoms closer to the viewer. O-H-O links are in red, with thicker linescloser to the viewer. Links ending in an arrow are pointing down to a deeperlevel, those with pointed ends are pointing up to a higher level. Several levelsof the structure are shown. Atoms shown as the same size may actually be atslightly different elevations. For example, the L-shaped sets of three atoms ina right angle are actually slightly tilted relative to the plane of the diagram.The tilted squares of oxygens surround fourfold screw axes.
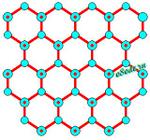
At left is a top view of the Ice Ih structure. Red dots on some atoms mark a B layer with O-H-O links pointing up to the next B layer. Other atoms are in an A layer and have O-H-O links pointing down to the next A layer.
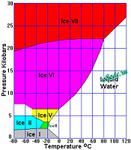
High-Pressure Ice Polymorphs
Ice exhibits a large number of polymorphs as shown at left. The ice in your tea is Ice I.
Ice I converts to Ice II or Ice III at about 2 kb. At the base of the Antarctic Ice Cap (5 km thick) the pressure is only about 0.5 kb. So ice on earth never gets thick enough to convert to a denser phase. We reach higher pressures in the crust, but at temperatures far beyond the melting points of any type of ice.
However, dense phases of ice almost certainly exist in the interiors of large satellites in the outer Solar System, and are probably easily produced by shock metamorphism during meteoroid impacts.
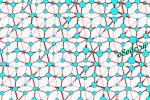
Ice V
Ice V is monoclinic. In the diagram below, oxygen atoms are shown in blue withlarger atoms closer to the viewer. O-H-O links are in red, with thicker linescloser to the viewer. Links ending in an arrow are pointing down to a deeperlevel, those with pointed ends are pointing up to a higher level. Several levelsof the structure are shown. Atoms shown as the same size may actually be atslightly different elevations. The unit cell is shown in gray (one set of edgesruns horizontally and is largely hidden by atoms and bonds, but it's there. Lookclosely).
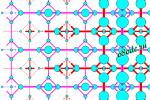
Ice VI
Ice VI is tetragonal, with a = 6.27 Angstrom units and c = 5.79 - nearlycubic. The density is 1.31 gm/cc. It can be described as a "self-clathrate." A clathrate is amolecule surrounded by a cage of water molecules. In Ice VI, there are clustersof five water molecules, a central molecule in a tetrahedral cage of fourothers. The centers of the clusters lie at the corners and centers of abody-centered tetragonal lattice, and the surrounding molecules are 3/8c aboveand below the central molecule.
Closely packed structures do not allow tetrahedral linkages very well. Ice VIand Ice VII achieve their density by having two interpenetrating butdisconnected lattices. In this diagram the O-H-O links in the two separatenetworks are shown in red and purple.
oxygen atoms are shown in blue with larger atoms closerto the viewer. The two networks of O-H-O links are in red and purple, with thicker lines closer to the viewer.Links ending in an arrow are pointing down to a deeper level, those with pointedends are pointing up to a higher level. Several levels of the structure areshown.
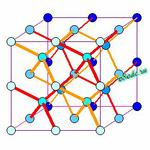
In some ways Ice VII is easiest to understand, because it consists of twointerpenetrating Ice Ic lattices.
The two interpenetrating sets of lattices are shown in orange and red. The unit cell consists of eight body-centered cubes.
Ice VII has a density of 1.66 gm/cc.
The Ice VII unit cell consists of body-centered cubes, which are prettytightly packed. An ice structure based on close-packed water molecules wouldrequire highly distorted bonds, and theoretical calculations suggest that IceVII is the stable form up to at least 200 kilobars. At earth gravity, 200kilobars would correspond to a depth of about 1500 kilometers of ice, takingphase changes into account.
At extremely high pressures we might expect water molecules to break downentirely and a close packed structure with ionic bonding to form.