Влияние кислорода и водорода на свойства воды
Часть 1. Измерение ОВП
Проблемы с измерениями окислительно-восстановительных потенциалов (ОВП) в водных растворах существуют уже давно. В последние несколько десятилетий они стали возникать при измерениях ОВП в питьевой, технической воде и в воде бассейнов. Особенно массовый характер измерения приобрели после открытия получения и использования электролизной активированной воды. Чаще всего ОВП в воде измеряют с помощью платиновых электродов относительно вспомогательного хлорсеребряного электрода. Измеряют разность потенциалов между этими электродами с помощью высокооомного милливольтметра.
Поэтому перед тем как приступить к особенностям измерения ОВП с помощью таких электродов полезно рассмотреть состав воды на примере просто дистиллированной воды. Не будем пока учитывать влияние катионных редокс-пар, минерализации, наличия примесей и т.д. В такой воде кроме обычных молекул Н2О может присутствовать целый ряд составляющих – растворенные молекулярные и атомарные кислород и водород, ОН-, Н+, Н3О-, О3- и т.д.
Основными газами, растворенными в воде являются (как и в атмосфере) - кислород, водород, углекислый газ и азот. Наиболее легко растворимым является СО2, относительная растворимость углекислого газа примерно в 70 раз выше растворимости кислорода и в 150 раз выше растворимости азота. На рис.1 приведены кривые зависимости растворимости кислорода, водорода и азота в мл в 100 г воды от температуры. Если растворимость кислорода при кипячении падает почти в 5 раз по сравнению с водой при нуле, то растворимость водорода меняется менее чем в два раза.
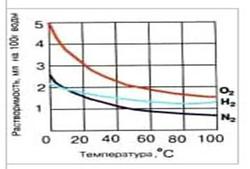
Зависимость растворимости кислорода в мг/л от температуры из других данных показана на рисунке 2.
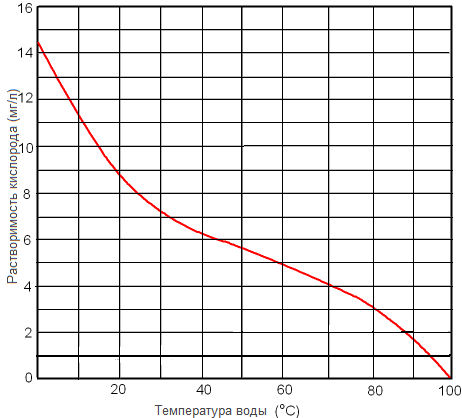
Видно, что в весовом отношении разница между водой при 0оС и 100оС составляет почти 15 раз.
Кстати, это и есть одно из объяснений-почему чай лучше заваривается в кипятке. Чай в этом случае меньше окисляется, так как в кипятке мало растворенного кислорода. Отсюда следует еще одно интересное наблюдение. Если кипяток быстро охладить, то получается вода с отрицательным ОВП.
Т. е. это один из самых простых способов получения малокислородной воды. Мы это проверили на опыте. Чем быстрее удается охладить воду, тем более отрицательным получается значение ОВП.
Этот метод обескислороживания воды широко применяется для обработки воды в трубопроводах охлаждения тепловых и атомных станций (это однако отдельная интересная тема).
Перейдем непосредственно к измерениям ОВП в воде с помощью платинового электрода. Согласно классику нашей электрохимии А.Н.Фрумкину, растворенный в воде кислород, адсорбируясь на платине, образует соединения различной степени прочности – разнообразные кристаллические продукты окисления. Так при анодном окислении электрода образуются поверхностные кислородные соединения типа PtO2, действующие потом как окислители. Найдено, что при этом возможно «подползание» кислорода под внешний слой атомов в решетке платины.
При потенциометрических измерениях в воде с помощью платиновых электродов необходимо учитывать не менее 4-х групп реакций, протекание которых возможно в воде и на электроде:
1) Окислительно-восстановительную, протекающую в воде
2) Электродную, т.е. реакцию взаимодействия окислительно-восстановительной системы в воде с материалом электрода
3) Побочную электродную реакцию, т.е. реакцию взаимодействия электрода с примесями, мешающими измерению (чаще всего с кислородом)
Найдено, что большое значении при измерениях с помощью платиновых электродов играют величина площади электродов, «гладкость» поверхности, обработка электрода перед измерениями, а также структура металла.
Чем больше площадь электрода, выше чистота обработки, применены специальные методы удаления окисных слоев, тем электрод более чувствителен к изменению содержания кислорода в воде и имеет более отрицательную величину потенциала.
Так, например, мы взяли партию в 100 шт платиновых лабораторных электродов типа ЭПЛ-02, изготовливаемых на Гомельском ЗИП (Беларусь), и провели измерения в воде с различным содержанием кислорода. Платина у этих электродов представляет шарик диаметром примерно 1мм, вплавленный в стекло. Разброс потенциалов у таких электродов на уровне воды, имеющей потенциал минус 200 мВ, составлял 150 мВ. При просмотре поверхности платины под микроскопом видно, что поверхность неровная, изрытая ямками, которые возникли при обработке платины в газовой горелке.
Гораздо лучшая воспроизводимость получается, если брать платину в виде отполированной проволоки диаметром более 1,5 мм и длиной 2-3 мм или в виде диска диаметром 1 см электроды фирмы «ЮМО» (Германия).
Дополнительно к качеству поверхности платины и её площади важное значение имеет обработка электрода в некоторых восстановительных растворах.
Мы проанализировали «качество» платиновых электродов у портативных ОВПметров как правило китайского производства. К сожалению, из-за экономии платины ( стоимость платины сейчас составляет почти 2000 руб/г) все электроды не отвечают вышеназванным требованиям для получении достаточно достоверных и воспроизводимых результатов.
Подводя итоги, можно в большой мере утверждать, что при отсутствии в воде редокс-систем типа Fe2+/Fe3+ потенциал платинового электрода (ОВП) во многом определяется количеством растворенного кислорода.
В следующей части мы рассмотрим существующие методы и приборы для изменения содержания кислорода в воде.
Санкт-Петербург. О.С.Е.
Контакты с автором - ose240@mail.ru.