Изотопный состав воды
к.х.н. О.В. Мосин
ИЗОТОПНЫЙ СОСТАВ ВОДЫ
Вода состоит из самых распространенных атомов в нашем мире – из водорода и кислорода, причем самым распространенным атомом во Вселенной является водород.
Солнце состоит в основном из водорода, а также содержит немного гелия, углерода и кислорода. Вся Вселенная на 98% состоит из водорода.
Вселенная образовалась с концентрации межзвездной воды (НОН) с образованием из нее гигантских протозвезд. Уплотняясь и сжимаясь, сжигая водород и образуя дейтерий, протозвезды постоянно превращаются в звезды и планеты.
Вода – самое загадочное вещество на свете. Она не подчиняется никаким законам физики и химии, обладает, как говорят ученые, аномальными свойствами. По законам химии она должна кипеть при температуре – 76 °С, и замерзать при температуре – 90 °С. Но мы знаем, что вода замерзает при 0 °С, а кипит при 100 °С.
Известным киевским учёным Бердышевым создана специальная наука – аквабиотика, наука о роли воды в жизненных процессах.
Из каких же изотопов состоит человек? Как любая материя человеческий организм сложен из кирпичиков - атомов, атомы одного сорта отличаются количеством элементарных частиц, их составляющих, то есть обладают свойством изотопии. Представим себе человека, вес которого составляет 50 кг. Тогда на кислород, углерод, азот и водород приходится в общей сложности 48.3 кг. На все другие элементы – оставшиеся 1.3 кг. Легко посчитать, какое количество в таком гипотетическом человеке содержится тех или иных изотопов. Больше всего в человеке кислорода (30.481 кг). Это означает, что изотопа кислорода с массовым числом 16 (обозначается 16О) в человеке 30.4 кг, изотопа с массовым числом 17 (17О) 12.3 г и с массовым числом 18 (18О) 68.6 г. Углерода в нашем человеке 11.537 кг и он распределен между изотопом с массовым числом 12 (12С) – 11.4 кг - и изотопом с массовым числом 13 (13С) – 137 г. Водорода в человеке чуть больше пяти кг: с массовым числом 1 (1Н) 5.0 кг, с массовым числом 2 (2Н или D - дейтерий) 1.5 г. Наконец, изотопы азота с массовыми числами 14 (14N ) и 15 (15N ) содержатся в количествах 1.3 кг и 5.1 г, соответственно. Такого "изотопного человека" можно изобразить в следующем виде:
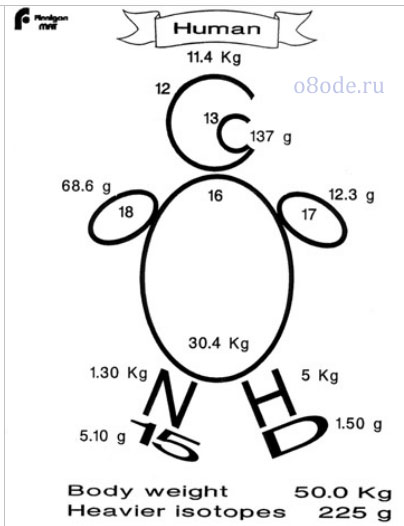
Таким образом при весе тела человека 50 кг в нем содержится 225 г тяжелых изотопов. Человек растет и прибавляет в весе за счет питания. Также за счет питания компенсируются затраты энергии, поддерживается температура тела, обеспечиваются процессы обмена веществ. Пища – это белки, жиры и углеводы. Все эти вещества состоят, в основном, как раз из тех четырех элементов, о которых шла речь выше (кислород, углерод, водород и азот). Все органические вещества в конечном итоге обязаны своим происхождением фотосинтезу в растениях. Растения поглощают углекислый газ из воздуха, который под действием света и катализаторов (в роли последних выступают особые белковые структуры, так называемые энзимы) взаимодействует с водой, втягиваемой корневой системой, с образованием простейших «кирпичиков» органических веществ. Из этих «кирпичиков» также с помощью катализаторов – энзимов создаются сложные органические молекулы углеводов, жиров и белков.
ТЯЖЕЛАЯ И ЛЕГКАЯ ВОДА
До 1932 года никто и понятия не имел, что в природе может быть еще и тяжелая вода, в состав которой могут входить тяжелые изотопы водорода - дейтерий и тритий пусть даже в малых количествах. Именно это обстоятельство и послужило причиной того, что эти элементы "прятались" от ученых, маскируясь под ошибки опытов и недостаточную точность измерений.
Тяжелый водород - дейтерий был открыт американским физико-химиком Гарольдом Юри (1893-1981) в 1931 году. Одному из своих помощников Г. Юри поручил выпарить шесть литров жидкого водорода и в последней фракции объемом 3 см спектральным анализом впервые был обнаружен тяжелый изотоп водорода, с атомной массой в два раза превышающий известный протий.
Ученые пришли к выводу, что, по-видимому, существует тяжелый изотоп водорода с атомным весом 2. В 1932 году Г. Юри и Э.Ф. Осборн впервые обнаружили в природной воде тяжелую воду. Через два года Гарольд Юри был удостоен Нобелевской премии. Открытие третьего сверхтяжелого изотопа водорода трития с атомным весом 3 первые годы держали в секрете по стратегическим соображениям. В 1951 году была получена и исследована тритиевая вода. Если дейтериевая вода сейчас уже хорошо изучена практически во всех отраслях науки и техники, то "звездный" час тритиевой воды еще не настал, потому что трития на Земле очень малое количество. Всего его на Земле около 25-30 кг и содержится он в основном в мировых водах (около 20кг). Но его количество в водах Земли непрерывно возрастает, так как он образуется при бомбардировке ядер азота и кислорода атмосферы космическими лучами. В результате этого содержание трития в первоначальных (реликтовых) водах непрерывно увеличивается.
В отличие от протия и дейтерия тритий - радиоактивный элемент с периодом полураспада девять лет. По своим свойствам сверхтяжелая тритиевая вода отличается от протиевой (легкой) воды больше, чем дейтериевая вода (см. таблицу 1).
Таблица 1
Основные физические показатели легкой, тяжелой и сверхтяжелой воды
- Вода; Химическое обозначение; Молекулярный вес; Температура,°С плавления/кипения; Плотность, г/см3
- Легкая; Н1 2О16; 18; 0 100; 1,00
- Тяжелая; Н1 2О16 (Д2О); 20; 3,8 101,42; 1,11
- Сверхтяжелая; Н1 2О16 (Т2О); 22; 9 104; 1,33
Тритий зарождается в сверхвысоких слоях атмосферы в основном при бомбардировке ядер азота и кислорода нейтронами космического излучения.
В природной воде содержание трития ничтожно - всего 10-18 атомных процента. И тем не менее он есть в той воде, которую мы пьем, и за долгие годы жизни он наносит существенный вред нашим генам, вызывая старение, болезни.
Получают тяжелую дейтериевую воду с мизерным присутствием тритиевой воды концентрированном ее в остатке электролита после электролитического разложения природной воды, а также при фракционной перегонке жидкого водорода. Промышленное производство тяжелой воды с каждым годом возрастает почти во всех странах и особенно в странах, обладающих ядерным оружием. Тяжелую воду используют главным образом как замедлитель быстрых нейтронов при расщеплении радиоактивных элементов в ядерных реакторах. Перспектива использования тяжелой воды для нужд человечества грандиозна. Тяжелая вода может стать неисчерпаемым источником энергаи: 1 грамм дейтерия может дать энергии в 10 млн.раз больше, чем сгорание 1 грамма угля. А запасы дейтерия в Мировом океане составляют поистине колоссальную величину - около 1015 тонн?
Тритиевая вода пока имеет ограниченное применение и используется в настоящее время главным образом при термоядерных реакциях, а. также в физико-химических и биологических исследованиях в качестве меченых радиоактивных молекул НТО.
У кислорода обнаружены шесть изотопов: О14, О15, О16 О17, О18 и О19. Три из них: О16, О17 и О18 - стабильные, а О14, О15 и О19 являются радиоактивными изотопами. Стабильные изотопы кислорода содержатся во всех природных водах: их соотношение таково: на 10000 частей О16 приходится 4 части О17 и 20 частей О18.
Получают тяжелокислородную воду из природной фракционной перегонкой и Используют главным образом для исследовательских целей. По физико-химическим свойствам тяжелокислородная вода значительно меньше отличается от обычной, чем тяжеловодородная.
Учитывая разнообразие изотопного состава водорода и кислорода, с большой долей достоверности можно утверждать о наличии 36 изотопных разновидаостей природной воды. 99,73% в ней содержится протиевая легкая вода НО16, далее следуют тяжелокислородаые воды Н1О17 (0,04%) и Н1О18 (0,20%). Изотопная водородная разновидность тяжелой воды Н1ДО16 и Д2О16 составляет 0,03%.
ИЗОТОПЫ В СОСТАВЕ ВОДЫ
Водород воды имеет три изотопа: протий 1Н (протон + электрон), дейтерий 2Н или Д (протон + нейтрон + электрон), тритий 3Н или Т (протон + два нейтрона + электрон), с массовыми числами соответственно 1, 2 и 3. Протий и дейтерий – стабильные изотопы. Тритий – бета радиоактивен, период полураспада равен 12,26 года. Атомы Н бывают разной степени возбуждения.
Кроме водорода, изотопы обнаружены и у кислорода, их пять, кроме известного всем стабильного изотопа О16 (с молекулярным весом 16). Три из них оказались радиоактивными – О14, О15 и О19, а О17 и О18 – стабильными. О16, О17 и О18 содержатся во всех природных водах, причем их соотношение (с колебаниями до 1%) таково: на 10000 частей О16 приходится 4 части О17 и 20 частей О18.
По физическим свойствам тяжелокислородная вода меньше отличается от обычной, чем тяжеловодородная. Получают ее из природной воды фракционной перегонкой и используют как источник препаратов с меченым кислородом.
Учитывая все разнообразие изотопного состава водорода и кислорода, можно говорить о большом разнообразии изотопных разновидностей воды. Девять из них включают только стабильные изотопы и составляют основное содержание природной воды. В ней преобладает обычная вода Н12О16 (99,73%), далее следует тяжелокислородные воды Н12О17 (0,04%) и Н12О18 (0,2%), а также изотопная разновидность тяжелой воды H1D1O16 (0,03%).
Кислорода в человеке 60%, но по количеству атомов все живые существа на 2/3 состоят из атомов водорода и на ¼ из атомов кислорода. Изотопное отношение: П:Д = 1:4700 в материковых водах, П:Д = 1:6800 атомов в морской воде. То есть концентрация в материковых водах Д = 0,0135 ат.% или 0,015 вес%, в морской воде Д = 0,015 ат.% или 0,017 вес%. В природной воде содержание трития ничтожно – всего 10-18 атомных процента. И тем не менее он есть и в питьевой воде.
В зависимости от видов и содержания изотопов водорода (Н, Д, Т) и кислорода (О14, О15, О16, О17, О18, О19), от степени чистоты и загрязнения исследователи выделяют свыше тысячи разновидностей питьевой воды.
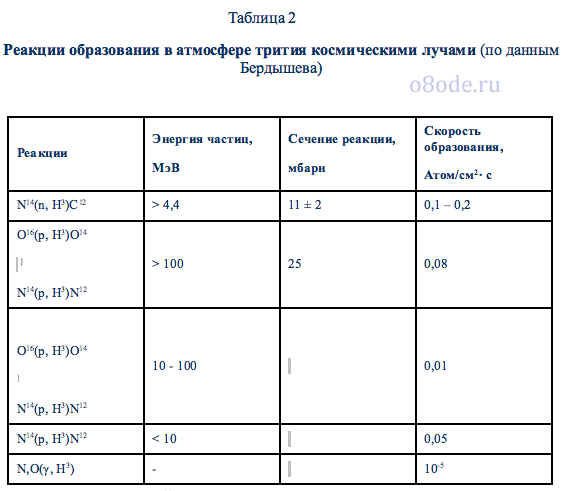
Поскольку Вселенная в основном состоит из атомов водорода, космические ядра водорода протоны, пронизывая атмосферу, захватывают О2, образуют Н2О. В этой воде много трития и дейтерия. Каждые сутки на Землю падает 1,5 тонны тритиевой-дейтерированой воды. Поэтому основным источником природного трития, дейтерия и радиоактивных кислородов является атмосфера. В таблице 2 приведены некоторые реакции образования Т и О14 в атмосфере под действием космических лучей.
Таблица 2
Реакции образования в атмосфере трития космическими лучами (по данным Бердышева)
БИОЛОГИЧЕСКИЕ СВОЙСТВА ВОДЫ С РАЗНЫМ ИЗОТОПНЫМ СОСТАВОМ
Вода, обогащенная дейтерием, тритием, тяжелыми и радиоактивными изотопами кислорода вредна для всего живого и человека.
Биологические эффекты тяжёлой воды заключаются:
Снижение скорости биохимических реакций, тканевого дыхания
Повышение вязкости протоплазмы клеток, скорости старения организма
Индукция мутаций, повреждение генофонда, рак, другие болезни
Торможение деления клеток, снижение роста
Гибель высших позвоночных
Благоприятствует жизни то обстоятельство, что 97% массы воды представлены легкими и стабильными изотопами Н и О.
Современная теория целебной питьевой воды, разработанная Бердышевым, требует полного удаления или существенного снижения концентрации тяжелых и радиоактивных изотопов водорода и кислорода из воды, являющейся основой жизни.
В тонне речной воды содержится 150 г тяжелой воды (Д2О). За 70 лет потребления 3 л питьевой воды в день через организм человека пройдет около 80 тонн воды, содержащей 12 кг дейтерия и значительное количество коррелирующих с ним радиоактивных изотопов водорода и кислорода.
Такое значительное количество тяжелых и радиоактивных изотопов водорода и кислорода воды, являющейся матрицей жизни, уже к наступлению половой зрелости человека повреждает его гены, вызывает различные болезни, рак, инициирует старение организма.
Массивное повреждение генофонда радиоактивными и тяжелыми изотопами водорода и кислорода воды может вызвать вымирание видов растений, животных и человека. По расчетам Бердышева, виду Homo Sapiens также грозит вымирание, если он не перейдет на употребление воды, обедненной радиоактивными и тяжелыми изотопами О2 и Н.
В опытах с различными клетками тканей печени, фибробластов куриных зародышей, в экспериментах на мышах, с курами, со свиньями, а также с пшеницей и овощами, - был зафиксирован повреждающий эффект тяжелой и тритированой воды и высокий положительный эффект воды с пониженным содержанием вредных изотопов водорода и трития.
Для приготовления талой воды свежий снег сгребали, наполняли емкость, таяние снега производили не до конца. Четвертую оставшуюся часть (25%) выбрасывали, предполагая, что с этой частью уйдет 25% дейтерия. Такая талая вода с пониженным содержанием тяжёлых изотопов оказывала благоприятное положительное влияние на организм.
Половая активность мышей повысилась, а у самок было ярко выражено многоплодие, новорожденные мышата весили на 20% больше своих собратьев, родители которых пили обычную воду. От кур, которых поили талой водой, за три с половиной месяца было получено в 2 раза больше яиц. Урожайность пшеницы возросла на 56%, а огурцов и редиса на 250% (14, 15).
Двадцать пять больных разного возраста в течение трех месяцев для питья и приготовления пищи применяли только полученную талую воду. Результаты превзошли все ожидания: у всех улучшилось общее состояние здоровья, снизилось количество холестерина в крови, улучшился обмен веществ.
Биологические эффекты лёгкой воды:
Оптимизация скорости биологических реакций
Стимуляция деления клеток, роста организмов
Стимуляция деления клеток, роста организмов
Радиопротекторное действие
Антимутагенные эффекты
Лечебно-профилактическое, антираковое действие
Учёные считают, что гравитационное поле Земли – недостаточно сильно для удержания 1Н, и наша планета постепенно теряет протий в результате его диссоциации в межпланетное пространство. Протий улетучивается быстрее тяжелого D. По мнению некоторых исследований, в течение геологического времени должно происходить накопление дейтерия в атмосфере и в поверхностных водах.
На нашей планете осуществляется гигантский испарительно-конденсационный процесс получения протиевой воды и обогащения его туч и облаков. В горах из них на одних склонах проливается преимущественно дейтерированая вода, на других – вода, обогащенная протием. В организме животных изотопный состав воды близок к составу дождевых вод в местах обитания. Для человека существенные коррективы в эту зависимость вносят овощи и фрукты, выращенные в других климато-географических условиях. Так, тропические фрукты, выращенные близко к экватору, имеют более низкие величины Д и О18. Весь Д в обычной воде находится в форме НДО, а не Д2О. Этиловый спирт также хороший накопитель дейтерия.
ЗАЧЕМ ЧЕЛОВЕЧЕСТВУ НУЖНА ТЯЖЁЛАЯ ВОДА?
Все, что мы до сих пор говорили, касалось тех свойств, которые зависят от строения атомов, от их порядкового номера, от числа и расположения электрических зарядов в атомных ядрах и электронов в молекуле. Только это и определяет химическое поведение вещества. Строение молекулы не зависит от массы атомного ядра. Поэтому одинаковые молекулы с разным изотопным составом химически почти неразличимы.
Правда, в науке слово «почти» нужно употреблять очень осторожно и осмотрительно. Это верно, что химические соединения, различные по изотопному составу, по химическим свойствам почти неразличимы. Но все же они ведут себя немного по-разному, хотя наблюдаемые при этом изотопные эффекты очень невелики: различаются по скорости реакций, у них различны значения константы равновесия. Различаются между собой спектры одинаковых по составу и строению молекул с разным изотопным составом. Сходство в свойствах изотопных соединений прекращается, когда вопрос касается кинетических и ядерных характеристик. Молекула, содержащая тяжелый изотопный атом, при той же температуре движется с меньшей скоростью, при столкновении таких частиц иначе протекает обмен кинетической энергией. А самое главное — изменяется способность вступать в ядерные превращения. Все эти-то свойства резко отличают тяжелую воду от любой другой воды с иным изотопным составом: ведь в ее состав входит тяжелый водород. В наши дни тяжелая вода успешно применяется в атомной энергетике для замедления нейтронов в ядерных реакторах.
Роль тяжёлой воды как замедлителя в атомном котле очень важна. Когда ядро урана-235 распадается на два атомных ядра-осколка, из него одновременно вылетают два или три нейтрона. Скорость их огромна, она превышает 20 000 км/с. Эти быстрые нейтроны не могут сами вызвать новый распад в других атомах урана. Они пролетят мимо них с такой быстротой, что просто не успеют прореагировать.
Нейтроны нужно замедлить примерно до 2,2 км/с, так чтобы они пришли в равновесие с тепловым движением окружающих молекул. При этом энергия нейтронов должна уменьшиться почти в 60 млн. раз. Далеко не всякое вещество пригодно в качестве замедлителя. Выбор очень ограничен. Во-первых, оно не должно поглощать нейтроны, вступая само в ядерные реакции, а во-вторых, оно должно состоять обязательно из легких элементов с малыми массовыми числами. При соударении с тяжелым ядром скорость нейтрона почти не изменяется, точно так же как почти не изменяется скорость мяча, отскакивающего при ударе о стенку.
Самым лучшим замедлителем мог бы быть легкий водород, но он заметно поглощает нейтроны. Тяжелый водород их почти не поглощает. Нейтрону, попавшему в тяжелую воду, достаточно всего 25 раз столкнуться с тяжелым водородом, чтобы потерять свою высокую энергию и приобрести способность взаимодействовать с ураном. Неплохой замедлитель — углерод в форме графита, но нейтрону в нем приходится испытывать около 110 столкновений, чтобы утратить начальную скорость. Используя тяжелую воду как замедлитель, конструкторы создают очень эффективные, а главное, легкие и компактные атомные энергетические установки, применяемые в основном на транспорте.
Тяжёлая вода также нужна чтобы исследовать механизм многих химических, физических и биологических процессов. Это, конечно, скромное, но очень важное применение тяжелой воды. Наверное, нет ни одного природного процесса, в котором не принимали бы участия вода или водород. Атомы тяжелого водорода — наиболее важные меченые атомы. Их, как разведчиков в бой, направляют химики в исследуемые реакции, чтобы проследить за ее ходом. В наши дни уже возникла и быстро развивается самостоятельная область науки — химия изотопного обмена. Наиболее важная ее задача — изучать с помощью дейтерия механизм химических реакций при получении органических соединений и исследовать их строение.


А физики сумели установить возможность ядерных реакций между легкими атомами, в том числе возможность реакции между атомами дейтерия.
В такой реакции неприменим закон сохранения массы, каким пользуется обычная химия; в результате реакции получается недостача. Это немалая недостача. Она означает, что если бы удалось найти условия, при которых может протекать реакция между двумя молями тяжелого водорода, то, согласно уравнению Эйнштейна, можно было бы получить энергию.
Смотрите рисунок с формулами справа.)
Это немалая энергия. В наше время, чтобы получить такую энергию, приходится сжигать в топках котлов ни много ни мало 13,5 т первосортного угля. А ведь его еще нужно добыть из шахт и доставить из-под земли к топке.
Между тем в соответствии с уравнением ядерной реакции такую энергию можно получить при затрате всего лишь двух молей дейтерия, которые содержатся в одном моле тяжелой воды. Следовательно, простой воды потребуется:
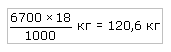
или 120 л. Значит, из одного литра обычной воды можно добыть больше энергии, чем можно получить ее из ста килограммов высококачественного угля. А запасы воды на нашей Земле огромны.
Что же мешает получать энергию из воды? Такая возможность пока что кажется фантастической, но она вполне реальна. На пути к ее осуществлению наука уже преодолела немало трудностей. Решена сложнейшая проблема, как извлекать тяжелую воду из природной. Теоретически исследованы и рассчитаны условия, при которых возможны ядерные реакции между легкими атомами.
Но к сожалению, исследователи встретили много трудностей. Насколько они серьезны, может показать простой расчет: чтобы два атома могли вступить в ядерную реакцию, их ядра должны столкнуться, т. е. сблизиться до расстояния примерно 10–14 м, начиная с которого межъядерные силы уже могут преодолеть электростатическое отталкивание.
Но ядра атомов защищены, как броней, своими электронными оболочками. Эти оболочки простираются на расстояние в десятки тысяч раз большее. А самое главное — ядра заряжены и отталкиваются друг от друга, как и все одноименно заряженные тела. Энергию, необходимую для того, чтобы преодолеть их взаимное отталкивание, рассчитать нетрудно. Из закона Кулона следует, что потенциальная энергия двух ядер, сблизившихся на расстояние 10–14 м, должна быть равна:

если между собой сталкиваются элементы с атомными номерами Z1 и Z2.
Конечно, мир атомных величин не очень привычен и нагляден, и трудно сразу представить себе, какова же эта энергия — мала или не очень мала. Но легко сообразить, с какой скоростью должны сталкиваться атомы, чтобы преодолеть потенциальную энергию электростатического отталкивания. Они должны обладать не меньшей кинетической энергией или по крайней мере равной.

массу одного атома можно найти из атомной массы, зная, сколько атомов содержится в одном моле).
Можно найти и скорость, с которой должны столкнуться атомы, чтобы могла начаться ядерная реакция:

У дейтерия атомный номер Z=1. Масса изотопа А=2, следовательно, скорость атомов должна быть равна: V=3,8х108 м/с, или 3800 км/с. При обычной температуре физикам известна средняя скорость теплового движения у атомов дейтерия, она равна всего лишь 1,9 км/с. При комнатной температуре, равной примерно 293 К, кинетическая энергия молекул возрастает пропорционально абсолютной температуре, или, что то же самое, пропорционально квадрату скорости.
Следовательно, чтобы средняя скорость молекул дейтерия была достаточной для реакции между ядрами, нужно нагреть тяжелый водород до температуры:
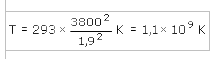
Итак, сталкиваться и реагировать между собой могут только ядра дейтерия, «нагретые» до температуры свыше миллиарда Кельвинов. Вот в этом-то и заключается довольно серьезное затруднение для подлинных героев науки — физиков, посвятивших свою жизнь труднейшей и величественнейшей из проблем — стремлению обеспечить энергией будущие поколения.
Литературные источники:
Бердышев Г.Д., Варнавский И.Н., Прилипенко В.Д. Аквабиотика – наука о роли воды в жизненных процессах. В кн.: Информоенергетика ІІІ-го тисячоліття: соціолого-синергетичні та медично-екологічні підходи. Київ – Кривий Ріг: ЗАТ “ЗТНВФ “Коло”, 2003, с. 22 – 28.
Бердышев Г.Д., Корочкин Л.И., Таранов С.Н., Михтарьянц Э.А. Влияние гистонов на структуры фибробластов куриных зародышей. В кн.: Материалы теоретической и клинической медицины. Томск: из-во ТГУ, 1964, в.3., с.44-45.
Варнавский И.Н., Бердышев Г.Д., Прилипенко В.Д. Целебная реликтовая вода – открытие третьего тысячелетия. Вопросы химии и химической технологии, 2002, № 5, с. 168 – 174.
Денько Е.И. Влияние тяжелой воды D2O на клетки животных, растений и микроорганизмы. Успехи совр. биол., 1970, т. 20. - № 1 (4). - с. 41 - 85.
Лобышев В.Н., Калиниченко Л.П. Изотопные эффекты D2O в биологических системах. М.: Наука, 1978. – 215 с.
Мосин О.В., Складнев Д.А., Швец. Исследование физиологической адаптации бактерий на тяжёловодородной среде. Биотехнология. 2000 г. N 8.