Гипотеза происхождения жизни в свете изотопного состава воды и ее температуры
Д-р, проф. И. Игнатов (Болгария)
Олег Мосин, к.х.н. (Россия)
3-4 миллиарда лет тому назад состав атмосферы на Земле отличался от современной атмосферы. Он практически не содержал кислорода и состоял, в основном, из углекислого газа, водорода, водяных паров, аммиака и метана. Кроме того, высокая вулканическая активность того времени способствовала выбросу в атмосферу также таких компонентов как азот (N), сероводород (H2S) и двуокись серы (SO2).
Вода также была не такая как сейчас. В 1996 г. российский учёный О. В. Мосин предположил, что первичная вода содержала намного больше дейтерия в начале эволюции жизни. Согласно его мнению жизнь начала зарождаться в воде с большим количеством молекул воды, содержащих дейтерий. О.В. Мосин считает, что в первичной атмосфере Земли не было защитного кислородно-озонового слоя, способного защитить поверхность Земли от жёсткого коротковолнового излучения Солнца, несущего огромную энергию. Поэтому излучение свободно проходило через бескислородную атмосферу и достигая гидросферы, вызывало радиолиз и фотолиз воды. Энергия Солнечного излучения, вулканические геотермальные процессы на горячей поверхности Земли и электрические разряды в атмосфере, могли явиться результатом обогащения гидросферы дейтерием в виде HDO, которая испаряется медленнее обычной воды, а конденсируется в закрытых водоемах быстрее.
Изотопный состав Вселенной на ранних этапах её эволюции также отличался от современного изотопного состава. Вселенная, образовавшаяся в результате “Большого взрыва” 13,7 миллиардов лет тому назад, была значительно горячее и плотнее, чем сейчас и состояла, в основном, из одного элемента – водорода. Дейтерий сформировался в последующие мгновения эволюции Вселенной в результате столкновения свободного нейтрона и протона при температурах миллион градусов Цельсия. А ещё позже два атома дейтерия вошли в состав ядра гелия, который состоит из двух протонов и двух нейтронов (рис. 1).
В 2007 году американский астроном Джефри Лински с помощью ультрафиолетового телескопа FUSE (Far Ultraviolet Spectroscopic Explorer) провёл исследование дейтерия в галактике Млечный Путь и обнаружил, что дейтерия в нём содержится значительно больше, чем об этом свидетельствовали данные предыдущих исследований. В частности, на звездообразование было потрачена не треть, а всего 15% изотопа водорода и он распределён неравномерно. Эти данные свидетельствуют о том, что для формирования звёзд требовалось значительно меньше водорода, превратившегося затем в гелий, как предполагалось раньше. По мнению Дж. Линдски этот факт меняет прежде существующие взгляды на эволюцию звезд и галактик.
Таким образом, дейтерий может служить своеобразным индикатором эволюции Вселенной, поскольку количество дейтерия в мире постоянно. Вплоть до настоящего времени считалось, что в процессе формирования гелия израсходовался почти все атомы дейтерий, и лишь 10 тысяч атомов дейтерия остались неизрасходованными. Исходя из этого количества дейтерия в Космосе, природная распространённость дейтерия составляет по расчётам 0.015% (от общего числа всех атомов водорода).
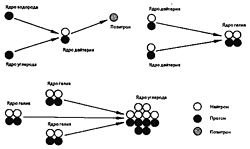
Рис. 1. Ядерные реакции с участием дейтерияИсточником дейтерия во Вселенной сейчас являются вспышки сверхновых звёзд и термоядерные процессы, идущие внутри звёзд. Возможно, этим объясняется тот факт, что мировое количество дейтерия повышается в период глобальных потеплений и изменений климата.
Гравитационное поле Земли, по мнению астрономов недостаточно сильное для удержания лёгкого водорода, и наша планета постепенно теряет водород в результате его диссоциации в межпланетное пространство. Водород улетучивается быстрее тяжелого дейтерия, который способен накапливаться в гидросфере Земли. Поэтому в результате этого природного процесса фракционирования изотопов в течение всей эволюции Земли должно происходить накопление дейтерия в поверхностных водах, в то время как в атмосфере и в водяном паре содержание дейтерия низкое. Таким образом, на планете происходит гигантский Вселенский природный процесс разделения изотопов водорода и дейтерия, играющий существенный роль в поддержании жизни на планете. При этом важным обстоятельством, является то, что углеродные связи с участием дейтерия более прочны и стабильны, чем углеродные связи с участием водорода. Изотопные эффекты, энергия связи, константа диссоциации, подвижность, длина связи для пары водород/тритий также различны. А это означает, что в первичной воде на Земле самоорганизующиеся дейтерированные структуры смогли сохраниться дольше во времени. Есть основания полагать, что в ту эпоху существовал процесс структурирования в водной тяжёловодородной среде органических молекул, поскольку структурирующее свойства и стабилизирующее воздействие тяжёлой воды на химические связи более выражены, чем у обычной воды (О. В. Мосин, 1996).
Табл. 1. Физические свойства обычной и тяжёлой воды
Физические свойства
D2O
H2O
Молекулярная масса
20
18
Плотность при 20 0C (г/см3)
1,1050
0,9982
T кристаллизации (0C)
3,8
0
T кипения (0C)
101,4
100
Тяжёлая вода (D2O или 2H2O) впервые была открыта американским учёным Юри в 1939 году. Тяжёлая вода имеет ту же химическую формулу, что и обычная вода, но вместо атомов водорода содержит два атома тяжёлых изотопа водорода — дейтерия. Внешне тяжёлая вода выглядит как обычная — бесцветная жидкость без вкуса и запаха, однако физико-химические свойства тяжёлой воды – температура плавления, кристаллизации, плотность, вязкость, теплота испарения и др. отличаются от свойств обычной воды. В смесях воды с тяжелой водой с большой скоростью происходит быстрый изотопный обмен с формированием “полутяжелой” воды: D2O + H2O = 2HDO. Поэтому тяжелая воды в растворах всегда находится в форме HDO.
См. ссылку: www.o8ode.ru/article/oleg/deiterii_tagelaa_voda_evolucia_i_gizn.htm
Разные природные воды содержат различное содержание дейтерия. Сотношение D/H (изотопные сдвиги, δ, ppm) по международному стандарту SMOW, соответствующему стабильной по изотопному составу воде Мирового океана, составляет: D/H = (155,76±0,05).10−6 (155,76 ppm). По международному стандарту природной воды из Антарктики SLAP с самым низким содержанием дейтерия, соотношение D/H в воде составляет D/H = 89.10−6 (89 ppm). Для природных вод чаще всего характерны отрицательные отклонения от SMOW на (1,0-1,5).10-5, в отдельных случаях до (6,0-6,7).10-5, но встречаются и положительные отклонения до 2,0.10-5. В среднем в природных водах соотношение D/H составляет 1:5700. Дейтерий в природных водах распределен неравномерно: варьируя от 0,015 атом.% D для воды из Антарктического льда, до 0,02-0,03 атом.% D для речной и морской воды. Талая вода и горная вода, полученная за счет таяния ледников содержит на ~3-5 % меньше дейтерия, чем речная вода. В среднем, в 1 тонне речной воды содержится ~150-300 г. дейтерия. Воды других подземных и поверхностных источников содержат разное количество дейтерия от δ = +5,0 D,%, SMOW (Средиземное море) до δ = –105 D,%, SMOW (река Волга).
Горная вода содержит гораздо меньшее количество дейтерия, чем другие виды вод, что благоприятно сказывается на метаболизм и функционирование организма. Представители Клуба медицинской биофизики из города Тетевена, Болгария провели следующий научный эксперимент под руководством проф. Игнатова. Они поливали семена одной культуры обычной водопроводной и горной водой. Результаты показали, что растения, политые горной водой, росли быстрее, чем растения, которых поливали обычной водопроводной водой (рис. 2). Согласно полученным данным, большее содержание дейтерия уменьшало проницаемость мембраны клетки и тем самым, замедляло транспорт питательных веществ внутрь клетки. На рисунке ниже показан результат опыта с кукурузой спустя месяц после ее поливки горной водой с пониженным содержанием дейтерия (д-р Игнатов, Цветкова, 2010).

Рис. 2. Слева – растение, которое поливали водой из-под крана. С правой стороны – растение, которое поливали горной водой из Тетевена, Болгария (д-р Игнатов, Цветкова, 2010)Научно достоверные результаты демонстрирует проф. Клима при росте растений, поливаемых разной водой. Проводя научные исследования с водой воде, мы сталкиваемся с ее уникальными свойствами, связанными с зарождением жизни.
Результаты показывают, что дейтерий играет огромную роль в биологических системах. Присутствие дейтерия в биологических системах приводит к изменениям структуры и свойствам жизненно-важных макромолекул, таких как дезоксирибонуклеиновые кислоты (ДНК) и протеины. При этом различают первичные и вторичные изотопные эффекты дейтерия в зависимости от того, какое положение занимает атом дейтерия в молекуле. Наиболее важными для структуры макромолекулы связи являются динамические короткоживущие водородные (дейтериевые) связи. Они формируются между соседними атомами дейтерия (водорода) и гетероатомами кислорода, углерода, азота, серы и т.д. и играют главную роль в поддержании пространственной структуры макромолекулярных цепей и как эти структуры взаимодействуют с другими соседними макромолекулярными структурами, а также с тяжелой водной окружающей среды.
При попадании клеток в тяжёлую воду из них не только исчезает протонированная вода за счет реакции обмена Н2О-D2О, но и происходит быстрый H±D обмен в гидроксильных, сульфгидрильных и аминогруппах всех органических соединений, включая белки, нуклеиновые кислоты, липиды, сахара. Только С—Н-связь не подвергается обмену и соединения типа С—D синтезируются «de поvo».
Интересно, что после обмена H±D ферменты не прекращают своей функции (Thоmson et al., 1966; Денько, 1974), но изменения в результате изотопного замещения за счет первичного и вторичного изотопных эффектов (Thomson, 1963; Halevy, 1963), а также действие тяжёлой воды как растворителя (большая структурированность и вязкость по сравнению с обычной водой) приводят к изменению скоростей (замедлению) и специфичности ферментативных реакций в тяжёлой воде.
В 1972 г. Креспи и Катц доказали, что с увеличением процентного содержания дейтерия в воде, рост растений замедляется (рис. 3). Было установлено, что высокие концентрации тяжёлой воды могут приводить к ингибированию многих жизненно-важных мутаций, включая блокировку митоза в стадии профазы, и даже в некоторых случаях вызывать спонтанные мутации. Тяжёлая вода высокой концентрации токсична для организма; химические реакции в её среде проходят несколько медленнее, по сравнению с обычной водой, водородные связи с участием дейтерия несколько сильнее обычных. Так, клетки животных способны выдерживать до 25-30% D2O, растений - 50-60% D2O, а клетки простейших микроорганизмов и микроводорослей способны жить на 80-90% D2O.

Рис. 3. Поливка томатов 30, 50 и 60%-ной D2O ингибирует рост растения (по данным Креспи и Катца, 1972).В 1996 г. О.В. Мосин показал, что к гибели клеток на тяжёлой воде могут приводить изменение соотношения основных „метаболитов” в процессе адаптации клеток к тяжелой воде. Клетки высших организмов погибают при содержании D2O в составе тела свыше 30%, но микроорганизмы, легко приспосабливающиеся к резким изменениям среды обитания, способны жить и размножаться даже в 98%-ной D2O (Мосин О.В, 1996). О.В. Мосиным в ходе ступенчатой адаптации к дейтерию на агаризованных средах с увеличивающими концентрациями D2O были получены адаптированные к D2O клетки микроорганизмов, относящиеся к различным таксономическим группам микроорганизмов. Общей особенностью микроорганизмов при росте на D2O являлось пропорциональное увеличение продолжительности лаг-фазы и времени клеточной генерации, в то время как выходы микробной биомассы уменьшались (гистограмма 1).
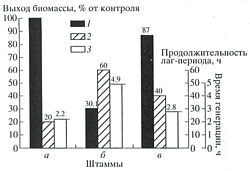
Гистограмма 1. Выход микробной биомассы –1, продолжительность лаг-фазы –2 и время клеточной генерации – 3 для метилотрофной бакрерии Brevibacterium methylicum при росте на средах с различными концентрациями тяжёлой воды: а – исходный микроорганизм на протонированной среде; б – исходный микроорганизм на 98%-ной тяжёлой воде; в – адаптированный к тяжёлой воде микроорганизм на 98%-ной тяжёлой воде. (О. В. Мосин, 1996)Характерной особенностью полученных адаптированных к тяжёлой воде объектов являлось то, что весь биологический материал клетки вместо природного водорода содержал дейтерий. Этот факт очень важен для изучения молекулярной организации клетки методами ЯМР-спектроскопии.
Полученные для исследуемых микроорганизмов данные свидетельствуют о том, что способность к адаптации к высоким концентрациям тяжёлой воды связана с эволюционным уровнем организации объекта, т. е. чем ниже уровень развития живого, тем выше способность к адаптации (О.В. Мосин, 1996). Возможно, лёгкость адаптации простейших к тяжёлой воде объясняется тем фактом, что клетка генетически “помнит” из какой воды вышла жизнь. О.В. Мосин считает также, что эффекты, наблюдаемые при адаптации к тяжёлой воде связаны с образованием в тяжёлой воде конформаций макромолекул с иными структурно-динамическими свойствами, чем конформаций, образованных с участием водорода, и поэтому имеющих другую активность и биологические свойства. Так, по теории абсолютных скоростей разрыв СH-связей может происходить быстрее, чем СD-связей, подвижность иона D+ меньше, чем подвижность Н+, константа ионизации тяжёлой воды меньше константы ионизации обычной воды. Всё это отражается на кинетике химической связи и скорости хим. реакций в тяжёлой воде. Связи, образованные атомами углерода с дейтерием прочнее, чем СН-связи из-за того, что амплитуда колебания дейтерона, имеющего в два раза большую чем протон массу, меньше амплитуды колебания протона в аналогичной связи и тем самым, это стабилизирует химическую связь.
Другое важное свойство определяется самой пространственной структурой тяжёлой воды, которая имеет тенденцию сближать гидрофобные группы макромолекулы, чтобы минимизировать их эффект на водородную (дейтериевую) связь в присутствии молекул тяжёлой воды. Поэтому структура спирали, каковой является ДНК в присутствии тяжёлой воды стабилизируется. Кроме этого, отмечены радиопротекторные свойства тяжёлой воды на клетки печени животных, в которой экспонировались эти клетки. Также было показано, что жизненный цикл плоских червей, выращенных на тяжёлой воде увеличивается примерно в 1,5 раза по-сравнению с червями, выращенными на обычной воде (М. Шепенинов, 2006).
Вероятно, клетка реализует лабильные адаптивные механизмы, которые способствуют функциональной реорганизации работы жизненно-важных систем в тяжёлой воде (О. В. Мосин, 1996). Так, нормальному биосинтезу и функционированию в тяжёлой воде таких биологически активных соединений, как нуклеиновые кислоты и белки способствует поддержание их структуры посредством формирования водородных (дейтериевых) связей в молекулах. Связи, сформированные атомами дейтерия различаются по прочности и энергии от аналогичных водородных связей. Различия в нуклеарной массе атома водорода и дейтерия косвенно могут служить причиной различий в синтезах нуклеиновых кислот, которые могут приводить в свою очередь к структурным различиям и, следовательно, к функциональным изменениям в клетке. Ферментативные функции и структура синтезируемых белков также изменяются при росте клеток на тяжёлой воде, что может отразиться на процессах метаболизма и деления клетки.
Отмечено, что адаптация к тяжёлой воде проходит легче при постепенном увеличении содержания дейтерия в среде, так как чувствительность к тяжёлой воде разных ключевых систем различна (О.В. Мосин, 1996). Практически даже высокодейтерированные среды содержат протоны от 0,2—10%. Возможно, что остаточные протоны в момент адаптации к тяжёлой воде облегчают перестройку к изменившимся условиям, встраиваясь в те участки, которые наиболее чувствительны к замене на дейтерий. Если допустить это, то встраивание протонов должно приводить к накоплению легкого изотопа в органическом материале клеток и соответственно к обогащению тяжелым изотопом среды культивирования.
Адаптация к тяжёлой воде является фенотипическим феноменом, поскольку адаптированные к тяжёлой воде клетки возвращаются к нормальному росту в протонированных средах после некоторого лаг-периода (О.В. Мосин с соавт., 1996). В то же время обратимость роста на D- и Н-средах не исключает возможности изменения метаболизма дейтерированных клеток, т.е. морфологической и функциональной перестройки в тяжёловодородной среде. Электронная микроскопия дейтерированных клеток бактерий Micrococcus lysodeikticus (В. А. Ерёмин, Л. Н. Чекулаева, 1978) выявила существенные различия в морфологии выращенных на тяжёлой воде клеток (рис. 4). Клетки, выращенные на тяжёлой воде имели в 2—3 раза более толстую клеточную стенку; чем протонированные клетки, распределение в них ДНК было неравномерным (В. А. Ерёмин, Л. Н. Чекулаева, 1978). На микрофотографии дейтерированных клеток Micrococcus lysodeikticus видны как плотные (одинарная стрелка), так и электронно-прозрачные участки (двойная стрелка), состоящие из плотно упакованных мембран, наподобие мезосом. Кроме того, для дейтерированного микроорганизма (рис. 4, в) было также характерно резкое изменение формы клеток и направления их деления с образованием сложных структур, состоящих из 6—8 клеток. По наблюдениям авторов, клеточное деление не заканчивалось обычным расхождением дочерних клеток, а приводило к образованию атипичных клеток—«монстров», описанных Мозесом с соавт. (Moses et al., 1958).
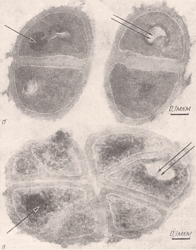
Рис. 4. Электронные микрофотографии клеток бактерий Micrococcus lysodeikticus; б – клетки, выращенные на протонированной среде, в – дейтерированные клетки, выращенные на тяжёловодородной среде (по данным В. А. Ерёмина и Л. Н. Чекулаевой, 1978 ).Вероятно, наблюдаемые морфологические изменения на тяжёлой воде связаны с ингибированием роста дейтерированных клеток и обусловлены перестройкой в процессе адаптации к тяжёлой воде. Факт, что дейтерированные клетки более крупные, чем протонированные является общебиологическим и наблюдается при выращивании целого ряда животных и растительных объектов (Мосин О. В., 1996).
Полученные данные позволяют видеть аналогию между адаптацией к тяжёлой воде и адаптации к низким температурам. Ещё Юнг на клетках Escherichia coli, помещенных в 98,6%-ную тяжёлую воду, показал, что эффект торможения роста тяжелой воды может быть компенсирован повышением температуры роста (Jung, 1967). Аналогия с охлаждением позволяет рассматривать адаптацию к тяжёлой воде, как адаптацию к неспецифическому фактору, действующему одновременно на функциональное состояние большого числа систем: превращение энергии, биосинтетические процессы, транспорт веществ, структуру и функции макромолекул. Возможно, что наиболее чувствительными к замене Н+ на D+ оказываются именно те системы, которые используют высокую подвижность протонов и высокую скорость разрыва протонных связей. Такими системами в клетке могут быть дыхательная цепь и аппарат биосинтеза макромолекул, которые располагаются в цитоплазматической мембране или находятся под ее контролем. Аналогия между адаптацией к тяжёлой воде и температурной адаптацией очень важна для конструирования дейтерированных ферментов, которые смогут функционировать в условиях высоких температур. Такие стабильные дейтерированные ферменты необходимы в биотехнологии, медицине и сельском хозяйстве.
Структурно-динамические свойства клеточной мембраны, которые в большинстве зависят от качественного и количественного состава липидов, также могут изменяться в присутствии тяжёлой воды. Полученный результат объясняется тем, что клеточная мембрана является одной из первых органелл клетки, которая испытывает воздействие тяжёлой воды, и тем самым компенсирует реалогические параметры мембраны (вязкость, текучесть, структурированность) изменением количественного и качественного состава липидов.
В клетках бактерий одним из важнейших инструментов регуляции метаболизма является мембрана, объединяющая в себе аппараты биосинтеза полисахаридов, трансформации энергии, снабжении клетки метаболитами и участвующая в биосинтезе белков, нуклеиновых кислот и липидов. Можно предположить, что в адаптации к тяжёлой воде мембраны играют не последнюю роль. Однако до сих пор не понятно, что происходит с мембранами, как они реагируют на замену среды и какое это имеет значение для выживания клеток на среде, лишенной протонов.
Структурно-динамические свойства клеточной мембраны, которые в большинстве зависят от качественного и количественного состава липидов, также могут изменяться в присутствии тяжёлой воды. Так, сравнительный анализ липидного состава дейтерированных клеток Bacillus subtilis, полученных при росте на тяжёлой воде показал различия в количественном составе мембранных липидов по сравнению с обычной водой (О. В. Мосин 2001, рис. 5). Примечательно, что в образце полученном с тяжёлой воды соединения, имеющие времена удерживания - 33.38; 33.74 и 33.2 мин не детектируются (рис. 5). Это свидетельствует об ингибировании биосинтеза жирных кислот в присутствии тяжелой воды. Полученный результат, по видимому, объясняется тем, что клеточная мембрана является одной из первых органелл клетки, которая испытывает воздействие тяжёлой воды, и тем самым компенсирует реалогические параметры мембраны (вязкость, текучесть, структурированность) изменением количественного состава липидов.

Рис.5. Липидные профили протонированных (а) и дейтерированных (б) клеток Basilus subtilis; хроматограф Beckman Gold System (США), снабжённый насосом Model 166 (США) и детектором Model 126 (США); неподвижная фаза: Ultrasphere ODS 5 мкм; 4.6 x 250 мм; подвижная фаза: линейный градиент 5 мМ KH2PO4-ацетонитрил; 100% в течении 50 мин; скорость подачи: 0.5 мл/мин; детекция при 210 нм (О. В. Мосин, 2001).Дейтерированные клетки адаптированных к максимальной концентрации тяжёлой воды в среде микроорганизмов – удобные объекты для исследования эволюции и адаптации. В процессе роста клеток на тяжёлой воде в них синтезируются макромолекулы, в которых атомы водорода в углеродном скелете почти полностью замещены на дейтерий. Как было показано О.В. Мосиным, такие дейтерированные макромолекулы претерпевают структурно-адаптационные модификации, необходимые для нормального функционирования клетки в тяжёлой воде (О. В. Мосин, 2001).
Регулируя количественное содержание дейтерия в организме, вплоть до полного его устранения, мы можем планомерно ускорять или замедлять ход жизненных процессов, тем самым мы можем моделировать эволюцию. Это привело бы к ускорению обменных процессов в организме, а, следовательно, к увеличению его физической и интеллектуальной активности. Живые организмы почти на 70% состоит из воды, в которой содержится 0,015% дейтерия. По количественному содержанию (в атомных процентах) дейтерий занимает 12-е место среди химических элементов, из которых состоят живые организмы, включая человека. В этом отношении дейтерий следует отнести к разряду микроэлементов. Содержание таких микроэлементов как медь, железо, цинк, молибден, марганец в живом мире в десятки и сотни раз меньше, чем дейтерия.
Из всех существующих изотопов дейтерий самый важный, поскольку содержание дейтерия является индикатором эволюции Вселенной и даёт нам представление о её эволюции.
Также много важной информации о ранних этапах эволюции Солнечной системы и ее химическом составе дают нам падающие на Землю метеориты и кометы (рис. 6).

Рис. 6. Кусок редкого метеорита - палласит, найденный в графстве Северный Йоркшир, выставлен на аукцион за 146 тысяч долларов, по данным Daily Mail. Фото метеорита с сайта mirf.ruМетеориты – это обломки давно существующих планет, определяющие их состав и движущиеся подобно малым планетам эллиптическим орбитам. По составу метеориты делятся на железные, каменные, железо-каменные и углистые с содержанием углерода от 3-7%. Наиболее распространёнными химическими элементами в метеоритах являются: Al, Fe, Ca, O, Si, Mg, Ni, S. Химический состав отдельных метеоритов может значительно отклоняться от среднего. Так, например, содержание Ni в железных метеоритах колеблется от 5 до 30% и даже более. Среднее содержание в метеоритах драгоценных металлов и редких элементов (в г на 1 т вещества метеорита): Ru10, Rh5, Pd10, Ag5, Os3, lr5, Pt20, Au5. Установлено, что содержание некоторых химических элементов тесно связано с содержанием других элементов. Так, оказалось, что чем выше содержание Ni в метеоритах, тем меньше в нём Ga, и т.п. Изотопный состав многих химических элементов элементов в метеоритах оказался тождественным изотопному составу тех же элементов земного происхождения. Наличие в метеоритах радиоактивных химических элементов и продуктов их распада позволило определить возраст вещества, слагающего метеориты, который оказался равным 4,5 млрд. лет. В межпланетном пространстве метеориты подвергаются воздействию космических лучей, и в них образуются стабильные и нестабильные космогенные изотопы. По их содержанию определён космический возраст метеоритов, т. е. время их самостоятельного существования, составляющее для разных экземпляров от немногих миллионов до сотен миллионов лет.
В составе метеоритов также обнаружен ряд неизвестных или очень редко встречающихся на Земле минералов таких как шрейберзит, добреелит, ольдгамит, лавренсит, меррилит и др., которые присутствуют в метеоритах в незначительных количествах. За последние годы в метеоритах открыто несколько десятков новых, ранее неизвестных минералов, многие из которых названы по имени метеоритологов, например: фаррингтонит, юриит, найнинджерит, криновит и др. Наличие этих минералов указывает на своеобразие условий образования метеоритов, отличающихся от условий, при которых образовались земные горные породы. Наиболее распространёнными в метеоритах минералами являются: никелевое железо оливин, пироксены - безводные силикаты (энстатит, бронзит, гиперстен, диопсид, авгит) и иногда плагиоклаз.
Некоторые специфические метеоритные минералы, например лавренсит, очень нестойки в условиях Земли и быстро вступают в соединения с кислородом воздуха. В результате на метеоритах появляются продукты окисления в виде ржавых пятен. В некоторых редких типах метеоритов присутствует кристаллическая космическая вода (до 20%), а в других, столь же редких метеоритах встречаются мелкие зёрна алмаза. Кроме этого, в метеоритах были выделены разные газы, встречающиеся в разных количественных соотношениях, органические соединения – углеводороды, азотистые соединения, карбоновые и жирные кислоты, азотистые соединения, аминокислоты и др.
Самый известный метеорит – “Мерчисон”, упал в Австралии в 1969 году близ города Мерчинсон. Этот необычный метеорит – носитель неземных органических соединений, состоял из углистого хондрита. При исследовании в нем были обнаружены 18 аминокислот неземного происхождения.
В других углистых метеоритах (Orgueil, Mighei) обнаруживаются фоссилизированные «организованные элементы» — микроскопические (5-50 мкм) «одноклеточные» образования, имеющие явно выраженные двойные стенки (рис. 7 и рис. 8). Характерной особенностью этих образований является также их многочисленность: на 1 грамм вещества углистого метеорита приходится примерно 1800 «организованных элементов». Пока ничего нельзя сказать определённого о происхождении этих загадочных элементов в метеоритах, имеющих много общих черт с одноклеточными организмами. Исследователи анализировали организованные элементы методом электронного микрозонда и нашли, что эти структуры минерализованы соединениями железа, хлора и некоторыми другими соединениями, что свидетельствует о том, что формирование этих элементов происходило в водной, низкотемпературной среде.
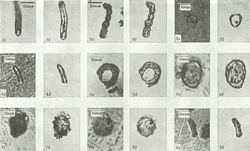
Рис. 7. Микрофотографии “организованных элементов ” из метеорита Orgueil. Источник M. G. Rutten. The Origin of life by natural causes. Elsevier Publishich Comp., N.Y., 1971.Еще в прошлом веке ученые, подвергая химическому анализу углистые хондриты, пытались найти в них воду, без которой жизнь невозможна. Однако прошло не одно десятилетие, прежде чем эти поиски увенчались успехом.
В 1944 году академик А. Заварицкий обнаружил в найденном в 1930 году в Оренбурской области метеорите "Старое Борискино" "космическую" воду.
Впоследствии следы воды находили и в ряде других углистых метеоритов. Подсчитано, что содержание воды в них иногда достигает двадцати процентов.

Рис. 8. Микрофотографии “организованных элементов ” из метеорита Mighei. Источник M. G. Rutten. The Origin of life by natural causes. Elsevier Publishich Comp., N. Y., 1971.По мнению некоторых исследователей, другими носителями органических соединений, от которых произошла земная жизнь, могли быть и кометы, точнее их газовые "хвосты", состоящие из кристалликов льда и частиц пыли. Они образуют оболочку кометы, а с приближением её к Солнцу часть из них — под давлением солнечных лучей и солнечного ветра — переходит в хвост. Ядро кометы сформировано из обычного льда с небольшими включениями углекислых и метановых льдов, а также частичек пыли.
Земля, обращаясь вокруг Солнца, за всю историю много раз пересекала "хвосты" многих комет. Когда комета сближается с Солнцем, происходит частичное испарение внешних слоев ледянистого ядра. В результате этого, внешние слои ледянистого ядра испаряются, благодаря чему вокруг него образуется водяное облако из кристалликов льда и частичек пыли, которое становится "хвостом" кометы, в котором могут находиться органические молекулы. Так, в 2005 году в комете Темпел была обнаружена аминокислота глицин – основная составляющая протеина.
Данные научные достижения доказывают, что „кирпичики” жизни существовали еще до зарождения Солнечной системы и планеты Земля. На нашей планете органические молекулы из метеоритов могли попасть в водную среду для их последующей эволюции в ранние формы жизни.
Жизнь зародилась в воде. За последние десятилетия учёные, используя самые разные виды энергии, получили в лабораторных условиях самые разнообразные "органические" вещества. Во всех этих опытах моделировались условия первичной бескислородной атмосферы. Было установлено, что первичной бескислородной атмосфере древней Земли был возможен синтез "органических" молекул за счет энергии коротковолнового ультрафиолетового излучения Солнца, энергии электрических разрядов и за счет других геотермальных источников энергии.
Первые эксперименты по неорганическому синтезу "органических" веществ в условиях первобытной Земли, провел в 1959 году С. Миллер (Miller S. L., 1959). Сконструированный им прибор заполнялся водой и смесью газов - водородом, метаном и аммиаком; свободный кислород в колбу не допускался. В верхней части колбы непрерывно создавались сильные электрические разряды. Внизу нагревалась до кипения вода, создавая циркуляцию пара и воды (рис. 9).
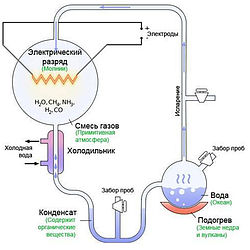
Рис. 9. Эксперимент Миллера, в котором под действием искрового разряда из водорода, метана, воды и аммиака в отсутствии кислорода образуются органические соединения.В качестве источника энергии сначала использовался искровой разряд. Поскольку разряд дает меньше энергии, чем ультрафиолет, в последующих экспериментах использовали ультрафиолет. При этом из метана, аммиака и водорода синтезировались органические соединения – альдегиды и аминокислоты.
Опыты обнаружили, что 10—15 % углерода перешло в органическую форму. Около 2 % углерода оказались в виде аминокислот, причём самым распространённым из них оказался глицин. В реакционной смеси также были обнаружены сахара, липиды и предшественники нуклеиновых кислот - нуклеозиды. Первичный анализ показал наличие в конечной смеси 5 аминокислот. Однако, более точный повторный анализ, опубликованный в 2008 году, показал, что эксперимент привёл к образованию 22 аминокислот.
См. ссылку: www.o8ode.ru/article/planetwa/voda_i_proichogdenie_gizni.htm
Оригинальные эксперименты Миллера вызвали большой интерес среди учёных всего мира. К аналогичным опытам приступили другие исследователи.
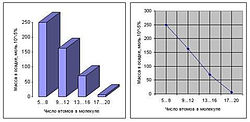
Гистограмма 2. Распределение соединений, полученных в опытах Миллера, по массе и числу атомов в молекуле (диаграммы построены по данным С. Миллера)В 1960 году Уилсон, добавив в исходный раствор серу, получил более крупные молекулы полимеров, содержащие по 20 и более атомов углерода (Wilson A. T., 1960). В смеси полимеров образовались тонкие пленки размером около 1 см, представляющие собой поверхностно-активные вещества, скопившиеся на поверхности раздела газ - жидкость (см. рис. 10). Считается, что эти пленки молекул, синтезировавшихся на границе между разными фазами, играли важную роль на ранних стадиях возникновения жизни. Катализатором образования подобных пленок служила, по-видимому, сера, которая была широко распространена на первобытной Земле в форме зерен сульфидов, например, в пиритовых песках.

Рис. 10. Плоские плёнки органических макромолекул, образующихся при искровых разрядах в смеси аммиака, сероводорода, паров воды и золы пекарских дрожжей. Источник M. G. Rutten. The Origin of life by natural causes. Elsevier Publishich Comp., N. Y., 1971.В 1969 году Поннамперума и сотр. провели эксперименты, подобные экспериментам Миллера, используя в качестве источника энергии ультрафиолетовый свет (Ponnamperuma C., 1969). Хотя по теоретическим соображениям синтезы, идущие под действием ультрафиолета, не должны принципиально отличаться от тех, которые вызываются электрическим разрядом, важно было получить экспериментальное подтверждение этого факта, поскольку в условиях первичной атмосферы гораздо больше энергии поступало с ультрафиолетовым излучением.
Исследователи не только смогли синтезировать аминокислоты и пурины, т. е. строительные блоки белков и нуклеиновых кислот, но также смогли синтезировать из этих блоков полимеры. Оказалось, что в присутствии цианистого водорода аминокислоты полимеризуются, образуя пептидные цепи. Причём, при добавлении фосфорной кислоты получались различные нуклеотиды.
Интересные результаты получил в 1965 году американский учёный Дж. Оро и сотр., показавший, что более крупные "органические" молекулы можно синтезировать и без помощи ультрафиолета, просто нагревая реакционную смесь (Oro J., 1965).
Известно, что в условиях восстановительной атмосферы малые "органические" молекулы могли синтезироваться за счет энергии ультрафиолетового излучения Солнца. Однако условия на Земле в эпоху примитивной атмосферы были для ранней жизни не менее опасными, чем они оказались бы для современной. Хотя первые организмы в бескислородной атмосфере не подвергалась окислению, ничто не защищало их от губительного воздействия жесткого ультрафиолетового излучения. Поэтому надо учитывать, что в те времена, возможно, использовались другие источники энергии. Например, свободные радикалы и малые "органические" молекулы могли синтезироваться за счет высокоэнергетического ультрафиолетового излучения Солнца, а для синтеза из малых молекул других, более сложных соединений могли служить и менее мощные геотермальные источники энергии (рис. 11). Так, в растворах формальдегида с гидроксиламином, формальдегида с гидразином и в растворах, содержащих цианистый водород, в конце опыта обнаруживались аминокислоты (Oro J., 1965). В других экспериментах эти продукты полимеризовались в пептидные цепи - большой шаг к неорганическому синтезу белка. В системе с раствором цианистого водорода в водном аммиаке также появлялись более сложные соединения - пурины и пиримидины (азотистые основания, входящие в состав нуклеиновых кислот).
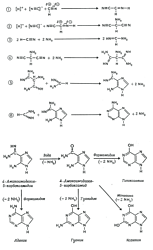
Рис. 11. Предполагаемые механизмы образования пуринов из водной смеси аммиака и цианистого водорода (вверху) и аденина из водной смеси аммиака и цианистого водорода (внизу). По данным Oro J., 1965Все эти эксперименты указали возможный путь перехода от синтеза малых "органических" молекул за счет энергии ультрафиолетового солнечного излучения Солнца к более сложным "органическим" молекулам, образующимся при менее жестких воздействиях.
Как известно, молекулы протеинов построены из одной или нескольких полипептидных цепей, а те в свою очередь состоят из большого числа разных аминокислот. После того как образовались аминокислоты, может произойти следующий важный этап - их конденсация в полипептидные цепи. Учёные считают, что выделение молекулы воды, сопровождающее реакцию конденсации двух молекул аминокислот - факт большой важности. Поскольку реакция поликонденсации сопровождается дегидратацией, скорость превращения будут выше при удалении воды из системы. Это соображение привело учёных к выводу, что раннее развитие жизни должно было происходить вблизи действующих вулканов, поскольку в ранние периоды геологической истории вулканическая деятельность шла более активно, чем в последующие времена. Однако дегидратация сопровождает не только полимеризацию аминокислот, но и объединение других строительных блоков в более крупные "органические" молекулы. Такое объединение всегда связано с реакцией конденсации, при которой от одного блока "отщепляется" атом водорода, а от другого - гидроксильная группа.
Первым возможность проведения реакций конденсации-дегидратации в условиях "первичного бульона" доказал в 1965 году американский учёный Кальвин (Calvin M., 1965). Из всех соединений лишь синильная кислота способна связывать молекулы воды "первичного бульона". Присутствие в "первичном бульоне" синильной кислоты доказано также первыми экспериментами Миллера.
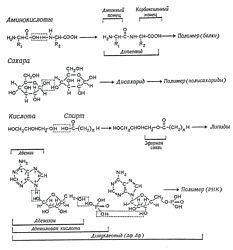
Рис. 12. Реакции конденсации с дегидратацией, приводящие к образованию из отдельных строительных блоков более крупных "органических" молекул. Верхние три уравнения: конденсация и последующая полимеризация аминокислот в протеины, сахаров в полисахариды и кислот и спиртов в липиды. Нижнее уравнение - конденсация аденина с рибозой и фосфорной кислотой, в результате чего образуется нуклеотид. Полимеризация нуклеотидов в цепь нуклеиновой кислоты также представляет собой реакцию конденсации и протекает с выделением молекул воды.Далее, обнаружилось, что два других, несколько более сложных соединения - цианамид и дицианамид HN(C=N)2 - обладают ещё большей дегидратирующей способностью. Реакции с ними более сложны, их механизм еще не выяснен окончательно. В присутствии синильной кислоты и цианамидов конденсация отдельных блоков, сопровождаемая дегидратацией, может идти при нормальных температурах в сильно разбавленных водных растворах.
Интересные выводы сделал в 1966 году Эйбелсон, установивший, что реакции поликонденсации с синильной кислотой сильно зависят от кислотности водных растворов, в которых они протекают (Abelson Ph. H., 1966). Эти реакции не идут в кислых средах, тогда как щелочные условия (рН = 8-9) им благоприятствуют. До сих пор идут дискуссии - мог ли первичный океан имел такой состав, но вполне вероятно, что именно таким рН обладала озерная вода, соприкасавшаяся с базальтом, и эти реакции вполне могли происходить при контакте с базальтовыми породами.
Также были проведены эксперименты, в которых безводную смесь аминокислот подвергали воздействию температур до 170 0С. Оказалось, что наилучшие результаты по поликонденсации получаются со смесями, содержащими аспарагиновую и глутаминовую кислоты. Именно эти две аминокислоты относятся к числу важнейших аминокислот, встречающихся в современных организмах.
В ходе описанного выше термического синтеза в реакционной смеси образовывались соединения, названные протеиноидами (по аналогии с природными белками), сходные с природными белками. Так, они состояли из крупных молекул с молекулярной массой до 300000, сложенных из тех же блоков, что и природный белок. Они содержали 18 из 23 аминокислот, обычно встречающихся у современных организмов. Таким образом, они отвечали общему определению белка. С природным белком они сходны и по ряду других важных свойств, например по связыванию полинуклеотидов, по пригодности в пищу бактериям и крысам, по способности вызывать реакции, сходные с теми, которые катализируются ферментами в организмах. Так, эти искусственно синтезированные органические соединения способны каталитически разлагать глюкозу.
Другое важное свойство протеиноидных соединений - их "ограниченная гетерогенность". Это значит, что последовательность аминокислот в их пептидных цепях не совершенно случайна, а, напротив, более или менее закономерна. Однако, в то время было невозможно провести строгое сравнение этих искусственных соединений с природными белками, так как молекулы белков настолько сложны, что структура большинства из них еще не определена с достаточной точностью. Стремясь подчеркнуть сходство этих искусственных белковоподобных соединений с природными белками, Фокс назвал их протеиноидами. Поскольку они были синтезированы под действием тепла, в дальнейшем их стали называть "термическими протеиноидами".
С тех пор многое изучено в получении было сделано для изучения протеиноидов. Самое важное то, что промывая горячую смесь протеиноидов водой или водными растворами солей в водной среде образуются элементарные мембраноподобные микросферы – коацерваты (Rutten M. G., 1963). Размер микросфер очень мал, их диаметр составляет около 2 мкм. Внешне они напоминают мембрану клетки. Морфологические особенности протеноидных коацерватов показаны на рис. 13 и рис. 14.
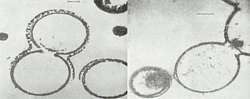
Рис. 13. Электронные микрофотографии срезов протеноидных коацерватов. Источник M. G. Rutten. The Origin of life by natural causes. Elsevier Publishich Comp., N. Y., 1971.Коацерваты довольно стабильны. Если их помещают в растворы иной концентрации, чем концентрация раствора, в котором они образовались, то они реагируют на внешние условия. В слишком концентрированных растворах они сморщиваются, в разбавленных набухают, т. е. их реакция на изменение осмотического давления сходна с реакцией живых клеток. Это объясняется наличием у них полупроницаемой наружной оболочки, сходной с мембраной клетки, которая может быть также и двойной.
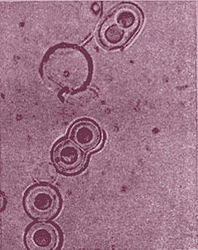
Рис. 14. Протеноидные коацерваты, сдвоенные при увеличении рН среды. Источник M. G. Rutten. The Origin of life by natural causes. Elsevier Publishich Comp., N. Y., 1971.Образование коацерватов из смеси искусственных протеинов важно потому, что оно дает нам материал для суждения о том, как мог произойти следующий шаг в развитии жизни. Это шаг от разрозненных "органических" молекул к группам организованных молекул, собранным в отдельные структуры и отделенным от окружающего мира примитивной мембраной, что было продемонстрировано нашим соотечественником академиком А.И. Опариным.
С учётом вышесказанного происхождение жизни выглядит так: Первым этапом живой эволюции, по-видимому, было образование при очень высоких температурах аминокислот и азотистых соединений – аналогов нуклеиновых кислот. Такой синтез вполне возможен наряду с другими, т. е. при воздействии электрических разрядов, ультрафиолетового излучения и высокой температуры. Возможность такого термического синтеза экспериментально доказана опытами многих исследователей (Fox S. W., 1965). Следующий этап - поликопденсация полученных аминокислот при температуре 170 или 65 С (в последнем случае в присутствии некоторых фосфатов). Реакция поликонденсации происходит, если в смеси имеется достаточно аспарагиновой и глутаминовой кислот. В смеси протеиноидов при воздействии на нее водой или кислыми водными растворами (дождем) образуются коарцерваты – предшественники клеток. Способность протеиноидов к выполнению некоторых функций, сходных с функциями ферментов живых организмов, выражается в том, что они могут в присутствии гидрата окиси цинка расщеплять нуклеотид АТФ, т. е. обладают слабой ферментативной активностью.
В настоящее время есть много способов экспериментального получения "органических" молекул неорганическим путем в условиях, моделирующих первичную атмосферу. Но, результаты этих экспериментов с геологической точки зрения не являются удовлетворительными, поскольку довольно трудно моделировать геологическое прошлое. Для появления первых древнейших форм жизни естественным путем существенно важны два условия. Во-первых, атмосфера должна быть бескислородной, во-вторых, должно иметься все необходимое для построения "органических" молекул - атомы углерода, азота, неорганические катализаторы и вода. Если эти условия будут выполнены, немедленно начнется образование "органических" соединений.
Но это означает, что формирование жизни - процесс, свойственный не только нашей Земле. В принципе, на любой планете, отвечающей двум вышеизложенным требованиям, находилась она в нашей Солнечной или в любой другой системе, могут идти аналогичные процессы. Ведь бескислородная атмосфера, содержащая нужные для синтеза "органических" соединений атомы и молекулы, - обычное для Вселенной явление. Остается одно главное условие для образования жизни - наличие жидкой воды. Таким образом, образование "органических" соединений из неорганических в водной среде - распространенный космический процесс.
Биологические эксперименты с дейтерием дают возможность прогнозировать и моделировать условия, при которых зародилась жизнь. Маловероятно, что жизнь могла возникнуть в хаотической неинформационной воде. Живые организмы и вода являются сложными, самоорганизующимися системами с характерной структурой. Самыми благоприятными для зарождения жизни признаны теплые и горячие минеральные воды, взаимодействующие с СаСО3, и поэтому имеющие щелочной показатель pH, а затем морские воды. Циркулируя в полостях, микротрещинах и каналах, воды карстовых источников обогащаются Са(HCO3)2, активно взаимодействующим с органическим веществом и могут содержать информацию о жизни в более поздние геологические периоды. При этом самоорганизация первичных органических соединений в водной среде поддерживалась термальной энергией магмы, вулканической деятельностью и солнечной активностью.
Нами были проведены эксперименты по исследованию минеральной, морской и горной воды из Болгарии ИК-спектроскопией и методом дифференциально неравновесного энергетического спектрального анализа (ДНЭС) относительно контроля — деионизированной воды (рис. 15, кривые 1–5). В ходе эксперименты были исследованы образцы воды из карстовых источников. Также методом ДНЭС были исследованы спектры сока кактуса (рис. 15, кривая 1). Кактус был выбран в качестве модельной системы, потому что растение содержит ~90 масс.% воды. Полученные данные продемонстрировали, что наиболее близким к спектру сока кактуса являлся спектр минеральной воды, контактирующей с СаСО3 (рис. 15, кривая 2). Аналогичный спектр имеют карстовые воды (рис. 15, кривая 4). При этом наиболее близкий к спектру сока кактуса (рис. 15, кривая 1) имел спектр карстовых вод, взаимодействующих с минеральной водой. Так, спектры растительного сока, минеральная вода и вода карстовых источников, взаимодействующих с CaCO3, имели значения пиков локальных максимумов в спектрах при –0,1112; –0,1187; –0,1262; –0,1287 и –0,1387 эВ. Подобные пики в спектре между растительным соком, горной и морской водой детектировались при –0,1362 эВ. Спектр контрольного образца деионизированной воды (рис. 15, кривая 5) существенно отличался от спектра морской минеральной и горной воды.
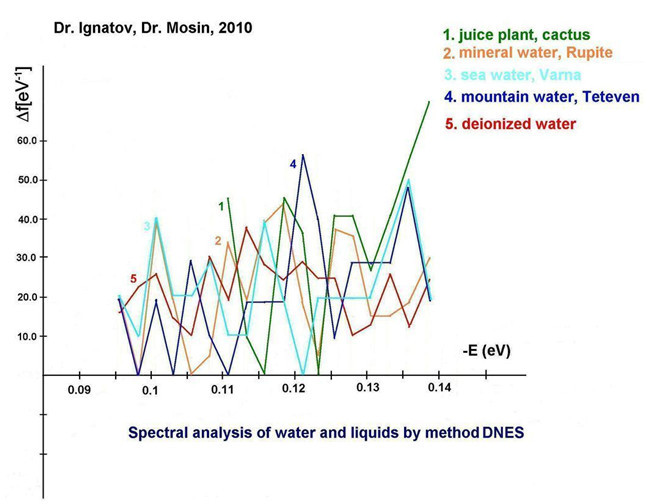
Рис. 15. Дифференциальные неравновесные энергетические спектры (ДНЭС) образцов воды различного происхождения: 1 — сок кактуса; 2 — минеральная вода местечка Рупит (Болгария); 3 – морская вода (курорт Варна, Болгария); 4 – горная вода (Тетевен, Болгария); 5 — деионизированная вода (контроль). По оси абсцисс показана энергия водородных H...O связей между молекулами H2O — E (эВ), по оси ординат — функция распределения молекул Н2О по энергиям –D f (эВ-1).
Как следует из вышеприведенных данных, более всего к ДНЭС-спектру сока кактуса приближался ДНЭС-спектр минеральной воды из местечка Рупите) Болгария), ИК-спектр которой показан на рисунке 16. Спектры растительного сока и минеральной воды с концентрацией ионов HCO3- (1320-1488 мг/л), Ca2+ (29-36 мг/л) и показателем pH = 6,85-7,19, имеют локальные максимумы при длинах волн λ = 8,95; 9,67; 9,81; 10,47 и 11,12 мкм. Локальные максимумы в ИК-спектрах между растительным соком и морской водой детектируются при λ = 9,10 мкм. Локальные максимумы, полученные методом ИК-спектроскопии при λ = 9,81 мкм (1019 см-1) и λ = 8,95 мкм (1117 cм-1) расположены на спектральной кривой локального максимума при λ = 9,7 мкм (1031 cм-1). С помощью метода ДНЭС были получены следующие данные — 8,95; 9,10; 9,64; 9,83; 10,45; 11,15 мкм (длина волны, λ) или 897; 957; 1017; 1037; 1099; 1117 см-1 (волновое число, k) (таблица 2).
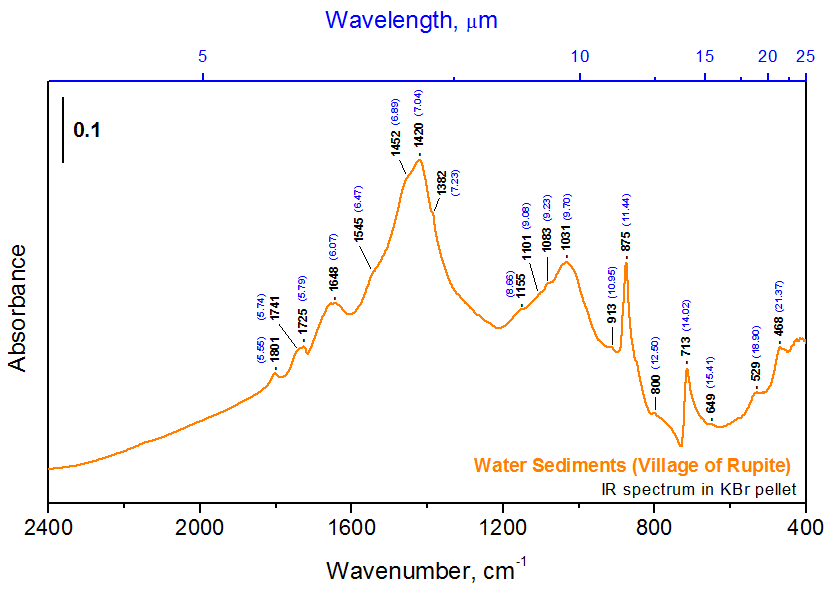
Рис. 16. ИК-спектр минеральной воды из местечка Рупите (Болгария). На нижней оси абсцисс показано волновое число (см-1); на верхней оси абсцисс — длина волны (мкм); на оси ординат — поглощение (усл. ед.)
Табл. 2. Характеристики спектров (ДНЭС-метод) воды различного происхождения*
- Энергия водородных связей, -E (эВ); Длина волны l, мкм; Волновое число k, cм-1
- Сок кактуса; Минеральная вода “Рупите”; Морская вода
- 0,1112; 0,1112; –; 11,15; 897
- 0,1187; 0,1187; –; 10,45; 957
- 0,1262; 0,1262; –; 9,83; 1017
- 0,1287; 0,1287; –; 9,64; 1037
- 0,1362; –; 0,1362; 9,10; 1099
- 0,1387; 0,1387; –; 8,95; 1117
* Примечание: Функция распределения молекул Н2О по энергиям (∆f) измеряется в электронвольтах (эВ-1). Показано при каких значениях энергии водородной связи (-E (эВ)) наблюдаются самые большие локальные максимумы этой функции.
Эти данные свидетельствуют о том, что возникновение жизни зависит как от структуры и свойств воды, так и от внешних факторов — температуры и показателя рН. Данным условиям наиболее лучше удовлетворяет взаимодействующая с CaCO3 теплая и горячая минеральная вода. Затем по качеству следует морская вода. В теплых и горячих минеральных водах пики в неравновесном энергетическом спектре более выражены по сравнению с пиками, полученными в той же воде с более низкой температурой. Это показывает на большую энергию для сохранения самоорганизованных структур во времени и интенсификацию биохимических реакций в условиях повышенных температур. Спектральный диапазон исследованных образцов воды находился в среднем ИК-диапазоне от 8 до 14 мкм. Предполагается, что в этом диапазоне существует “окно” прозрачности земной атмосферы для электромагнитной радиации. В этом интервале энергия излучается от Солнца к Земле, и от Земли в окружающее пространство.
Полученные данные свидетельствуют о наиболее большей вероятности происхождения жизни в теплой и горячей воде с показателем pH 9-10. Нам кажется маловероятным, что жизнь могла возникнуть в “хаотичной” водной среде. Живые организмы — высокоорганизованные структуры. При рассмотрении природных процессов самоорганизации существует интересный феномен, найденный в карстовых источниках местечка Златна Панега, Тетевен (Болгария). Обитающие там сине-зеленые водоросли окружены пузырьками диаметром 3-5 мм, время существования которых составляет от нескольких часов до дней. Вода, ДНЭС-спектр которой аналогичен ДНЭС-спектру растительного сока, имеет тенденцию сохранять самоорганизацирующие структуры. При добавлении к раствору пектинов катионов Ca2+, раствор принимает желатинизорованную структуру, поскольку катионы Ca2+ обладают способностью связывания с молекулами пектина с формированием металло-органических комплексов. Очевидно, эти комплексы играют существенную роль в объединении различных компонентов клеточной мембраны и влияют на ее компактность и прочность.
В этой связи важны следующие реакции, протекающие в водных растворах :
CO2 + 4H2S + O2 = CH2O + 4S + 3H2O (1)
СаСО3+ HOH + СО2 = Ca(HCО3)2 (2)
CO2 + ОН- = HCО3- (3)
2HCO3- + Ca2+ = CaCO3 + CO2 + H2O (4)
Уравнение (1) показывает, что некоторые хемосинтетические бактерии в анаэробных условиях в присутствии СО2 используют энергию, полученную в результате окисления H2S до S. Уравнение (2) связано с одним из самых распространëнных процессов в природе — формированием Ca(HCО3)2 из CaCO3 в присутствии Н2О и СО2. При наличии в водной среде гидроксил-ионов СО2 превращается в HCО3- (уравнение (3)). Уравнение (4) демонстрирует процессы, сопровождающие формирование строматолитов — древнейших известковых (доломитовых) ископаемых докембрийского периода, которые строили свой скелет из извести.
Вероятнее всего первые органические формы жизни возникли в горячей минеральной воде с повышенным содержанием дейтерия, поскольку как было показано нами раннее, в условиях первичной бескислородной атмосферы, лишенной озонового слоя, под воздействием геотермальной энергии, коротковолнового излучения Солнца и мощных искровых разрядов, в первичной гидросфере могли образовываться и накапливаться некоторые количества HDO. Эти данные также могут служить подтверждением возможного пути перехода от синтеза малых органических молекул за счет энергии УФ-излучения Солнца и температуры к более сложным органическим молекулам протеинов и нуклеиновых кислот. Молекулы протеинов построены из одной или нескольких полипептидных цепей, состоящие из большого числа различных α-аминокислот, связанных друг с другом посредством пептидной (–CO–NH–) связи. Их последующая конденсация в полипептидные цепи может произойти в определенных условиях, после их образования. Важным фактором в реакции конденсации двух молекул аминокислот является выделение молекулы Н2О. Поскольку реакция поликонденсации аминокислот сопровождается дегидратацией, при удалении Н2О из системы скорость химической реакции увеличивается. Этот факт свидетельствует о том, что раннее развитие жизни происходило вблизи действующих вулканов, поскольку в ранние периоды геологической истории вулканическая деятельность происходила более активно, чем в последующие геологические времена. Дегидратация сопровождает не только полимеризацию аминокислот, но и объединение других блоков в более крупные органические молекулы, а также полимеризацию нуклеотидов в нуклеиновой кислоты. Такое объединение всегда связано с реакцией конденсации, при которой от одного блока “отщепляется” протон Н+, а от другого — гидроксильная группа ОН- с образованием молекулы Н2О.
При этом самоорганизация первичных органических соединений в водных кластерах поддерживалась термальной энергией магмы, вулканической деятельностью и солнечной активностью. Так, циркулирующие в недрах по трещинам, пустотам, каналам и пещерам карстовые воды содержат карбонат кальция, активно взаимодействуют с живой материей и содержат информацию о жизни в более позднем геологическом периоде. При этом очень уникальна смесь из карстовой и минеральной воды из местечка Златной Панеги, Тетевенский край, Болгария. Она показывает нам спектр минеральной воды, взаимодействующей с карбонатом кальция из карстового источника. У исследованных д-ром Игнатовым более 30 источников с минеральной водой, содержащей кальциевые и карбонатные ионы, спектр похож на спектр воды из местечка Златной Панеги.
В природе существуют места с разной по составу и происхождению водой при одинаковых внешних условиях, но разных температурах от 10 0C до 12,5 0C и выше до 100 0С в геотермальных источниках. В местечке Златна Панега, Тетевенский край, Болгария в озере, образовавшемся от источника, вливаются три минеральных источника, чья средняя температура 21 0C. Река Вит находится только в нескольких км. Средняя температура реки около 15 0C. Фотографии на рис. 17 и рис. 18 показывают очевидную разницу между растительным миром в воде карстового источника и реки. Это является доказательством оптимально благоприятного места активной жизни водорослей при одинаковых внешних условиях. Единственная разница – в структуре воды. Минеральная вода, взаимодействующая с карбонатом кальция, а также и морская вода, являются щелочными.
См. ссылку: www.medicalbiophysics.dir.bg/ru/water_memory.html

Рис. 17. Карстовый и минеральный источник, растительность Златна Панега, Тетевенский край, Болгария фотограф: Александр Игнатов

Рис. 18. Река Вит, Тетевенский край, растительность в 3 км от источника Златна Панега фотограф: Александр Игнатов
С кальциево-силикатными породами связано и развитие древнейших форм жизни на Земле. Самые древние доказательства существования живых организмов со слоистой известковой структурой на Земле датируются 3,5 миллиардами лет. Эти древнейшие известковые (доломитовые) ископаемые докембрийского периода – строматолиты, которые строили свой скелет из известняка и диоксида кремния SiO2 (рис. 19-21).
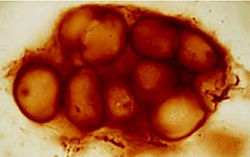
Рис. 19. Колониальная (хроококковая) форма из позднего Протерозоя Австралии (850 млн. лет назад)
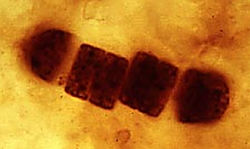
Рис. 20. Нитевидная форма Palaeolyngbya из того же местонахождения

Рис. 21. Строматолиты (Австралия)
Строматолиты формировались на дне неглубоких водоемов еще в архее в самую древнюю геологическую эпоху Земли — 2,5−3,5 млрд лет назад. Изучать эти образования очень важно и интересно, так как строматолиты хранят в себе сведения о зарождающейся жизни на Земле и органическом составе первых живых организмов – многочисленных колоний цианобактерий, сине-зелёных водорослей и нефтеперерерабатывающих бактерий, возникающих в толщах известняков и доломитов в жерлах погасших вулканов и термических источников. В качестве примера на фотографии на рис. 22 показаны многочисленные колонии сине-зеленых водорослей в области Рупите, Болгария. Место жизнеобитания находится в жерле погасшего древнего вулкана. При температуре 75 0C растительная жизнь развивается в полную силу.

Рис. 22. Водоросли, минеральная вода, 75 °C, Рупите, место Ванги фотограф: Александр ИгнатовВ самом начале эволюции на Земле наблюдалась усиленная вулканическая деятельность даже на дне первичного океана. В ту эпоху на Земле было больше кремния и соединений кремния, и он взаимодействовал с водой. По этой причине он абсорбировался в ранних живых организмах – диатомовых водорослях и радиоляриях. Эти планктонные формы обитают в верхних слоях морской воды вместе с другими организмами, обладающими известковыми (фораминиферы) и хитиновыми панцирями. Размер организмов с кремниевым скелетом достигает несколько десятков микрометров (рис. 23). После смерти эти организмы опускались на дно, причём их вещество химически взаимодействовало с морской водой. При этом карбонат кальция фораминифер и хитин других планктонных микроорганизмов растворялись в воде лучше, чем кремнезём диатомовых водорослей и радиолярий, формируя осадки кремнезёма. Кремнистые сланцы с отложениями этих кремнийсодержащих микроорганизмов формировались эпоху фанерозоя в глубоких океанских впадинах, на глубинах около 2-3 км. Временный расцвет организмом с кренезёмным скелетом мог привести к такому скоплению кремния в водах океана, что на дне смог образоваться гель кремниевой кислоты. Затем двуокись кремния могла кристаллизоваться вокруг рассеянных в известняке центров кристаллизации, постепенно замещая молекулы карбоната кальция. Позднее, организмы, обладающие известковыми панцирями фораминиферы стали абсорбировать кальций из известняковых пород.

Рис. 23. Организм с кремниевым скелетомСамый распространённый минерал земной коры кварц SiO2, по-видимому, играл большую роль в происхождении жизни. Кристалл кварца обладает тетраэдрической структурой, из которой складываются цепочечные силикатные структуры (рис. 24-28). Уникальность кварца заключается в том, что его кристаллы оптически активны, т.е. способны влиять на поляризованный свет. Но кристаллы кварца не просто воздействуют на проходящий через них свет, они также обладают оптически активными свойствами на поверхности кристалла (Терентьев, Клабуновский). Следовательно, на поверхности L- и D- энантиомерных кристаллов кварцев теоретически была возможна избирательная абсорбция L- и D-изомеров.
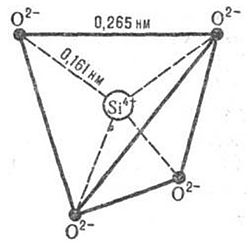
Рис. 24. Элементарный правильный кремне-кислородный тетраэдр SiO44-.
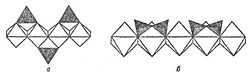
Рис. 25. Элементарные кремнекислородные единицы-ортогруппы SiO44- в структуре Mg-пироксена энстатите (а) и диортогруппы Si2 O7 6- в Са-пироксеноиде волластоните (б).
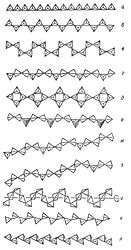
Рис. 26. Важнейшие типы кремнекислородных цепочечных анионных группировок (по Белову): а-метагерманатная, б - пироксеновая, в - батиситовая, г-волластонитовая, д-власовитовая, е-мелилитовая, ж-родонитовая, з-пироксмангитовая, и-метафосфатная, к-фторобериллатная, л - барилитовая.
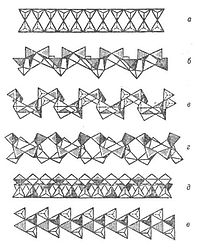
Рис. 27. Важнейшие типы ленточных кремнекислородных группировок (по Белову): а - силлиманитовая, амфиболовая, ксонотлитовая; б-эпидидимитовая; в-ортоклазовая; г-нарсарсукитовая; д-фенакитовая призматическая; е-эвклазовая инкрустированная.
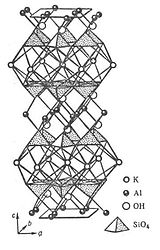
Рис. 28. Фрагмент (элементарный пакет) слоистой кристаллической структуры мусковита KAl2(AlSi3O10XOH)2, иллюстрирующий переслаивание алюмокремне-кислородных сеток с полиэдрическими слоями крупных катионов алюминия и калия, напоминает цепочку ДНК.
Другим интересным свойством кварца SiO2 является то, что его структура напоминает структуру самой воды. Еще первооткрыватели водородных связей Дж. Бернал и Р. Фаулер в 1932 г. сравнивали структуру жидкой воды с кристаллической структурой кварца, а ассоциаты воды рассматривались как тетрамеры 4Н20, в которых четыре молекулы воды соединены в компактный тетраэдр с двенадцатью внутренними водородными связями. В результате образуется четырёхгранная пирамида - тетраэдр.
По мнению некоторых исследователей (Ю.А. Колясников) водородные связи в этих тетрамерах могут образовывать как право- так и левовинтовую последовательности, подобно тому, как кристаллы кварца бывают право- и лево-вращательной кристаллической форм (рис. 29). Так как каждый такой тетрамер воды имеет еще и четыре незадействованные внешние водородные связи, то тетрамеры могут соединяться этими внешними связями в своего рода полимерные цепочки, наподобие молекулы ДНК. Поскольку внешних связей всего четыре, а внутренних - в 3 раза больше, то это позволяет тетрамерам в жидкой воде изгибать, поворачивать и даже надламывать эти ослабленные тепловыми колебаниями внешние водородные связи. Согласно этому предположению это и обуславливает текучесть воды.
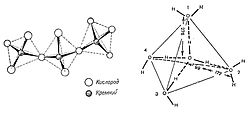
Рис. 29. Кристаллическая структура кварца (слева) и тетраэдрическая структура воды (справа).Предполагаемая структура воды могла быть обусловлена ее древней реологической связью с кварцем и другими кремнекислородными минералами, преобладающими в земной коре, из недр которой когда-то появилась вода на Земле. Как маленький кристаллик соли заставляет окружающий его раствор кристаллизоваться в подобные ему кристаллы, так кварц мог инициировать молекулы воды выстраиваться в тетраэдрические структуры, которые, энергетически наиболее выгодны.
Маловероятно, что жизнь возникла в “хаотической” воде. В настоящее время предложены теоретические модели, объясняющие структуру и свойства воды. Первые модели воды стали возникать в конце XIX века, когда накопилось много фактических данных об аномалиях воды. Во второй половине XX века Г. Немети и Х. Шаран предложили кластерную модель воды. В ней вода представлена в виде совокупности кластеров связанных водородными связями молекул воды, которые плавали среди свободных несвязанных молекул воды (рис. 30).
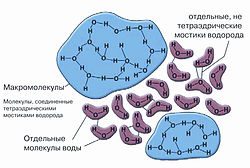
Рис. 30. Модель “мерцающих” кластеров.Современной наукой установлено, что особенности физических свойств воды и многочисленные короткоживущие водородные связи между соседними атомами водорода и кислорода в молекуле воды создают благоприятные возможности для образования особых структур-ассоциатов молекул воды (кластеров), способных воспринимать, хранить и передавать самую различную информацию о внутренних и внешних воздействиях.
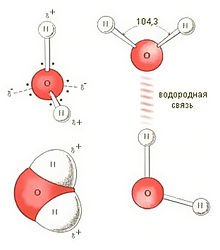
Рис. 31. Водородные связи между молекулами водыНепосредственной причиной образования водяных кластеров являются межмолекулярные диполь-дипольные взаимодействия и водородные связи между молекулами воды (рис. 31). Они возникают между ядрами водорода одних молекул и «сгущениями» электронной плотности у ядер кислорода других молекул воды. Водородные связи легко разрушаются под действием тепловых колебаний молекул и быстро восстанавливаются вновь, что делает структуру воды исключительно изменчивой. Именно благодаря этим связям в отдельных микрообъемах воды непрерывно возникают структурные элементы – кластеры воды. Возникновение и распад кластеров можно выразить схемой:
x·H2O↔ (H2O)x
Благодаря Рамановой электроскопии в 2005 г. коллектив учëных из университета Беркли, США – Гейслер, Сейкали и Смит, показали, что связи водорода между молекулами воды находятся в постоянном движении, постоянно разрываются и меняются. При каждом значении температуры в воде устанавливается свое динамическое равновесие в этом процессе. При нагревании воды часть теплоты затрачивается на разрыв водородных связей в кластерах. При этом на разрыв каждой связи расходуется 0,26-0,5 эВ. Этим и объясняется аномально высокая теплоемкость воды по сравнению с расплавами других веществ, не образующих водородных связей. При нагревании таких расплавов энергия расходуется только на сообщение тепловых движений их атомам или молекулам. Водородные связи между молекулами воды полностью разрываются только при переходе воды в пар. На правильность такой точки зрения указывает и то обстоятельство, что удельная теплоемкость водяного пара при 100°С практически совпадает с удельной теплоемкостью льда при 0°С.
Эти результаты коррелируют с квантово-механическими анализами неравновесного энергетического спектра (НЭС) воды проф. И. Игнатова. При этих анализах относительная стабильность кластеров зависит от внешних факторов. Вода отличается по своей структуре, и сходство в НЭС-спектре может наблюдаться при определëнных внешних условиях (Игнатов, 2005). Вода изменяет положение своих молекул в зависимости от энергии связей водорода. Анализы и результаты, достигнутые при помощи аппаратуры на наличие в воде кластеров, трудно могут быть восприняты. Сами кластерные формации динамичны, и «запоминание» информации зависит от целого ряда факторов. Первые результаты и анализы с помощью прибора проф. Антонова были получены в 1997 г.

Рис. 32. Результат Гейслера, Сейкали и Смита, полученный в Рамановой электроскопией при анализе движения молекул воды, Berkeley University, USAЭтот результат коррелирует с квантово-механическими анализами проф. И. Игнатова динамичного движения молекул воды в их попытке найти относительно стабильное состояние кластеров из порядка нанометров.
См: www.medicalbiophysics.dir.bg/ru/water_memory.html
Вода, таким образом, – это ассоциированная жидкость из множества множества молекул воды, связанных друг с другом межмолекулярными связями, диполь-дипольными взаимодействиями и водородными связями, которые постоянно рвутся и образуются вновь, что и объясняет многие аномальные свойства воды. Но классический полимер – это молекула, все атомы которой объединены ковалентными связями, а не водородными, которые до недавнего времени считались чисто электростатическими. Однако в 1999 г. было экспериментально показано, что водородная связь между молекулами воды во льду имеет частично (на 10%) ковалентный характер (Isaacs E. D., et al.,1999). Даже частично ковалентный характер водородной связи “разрешает”, по меньшей мере, 10% молекул воды объединяться в полимерные устойчивые ассоциаты.
В 1993 году американский химик Кен Джордан рассчитали варианты устойчивых “квантов воды”, состоящие из 6 молекул воды (рис. 33) (Tsai & Jordan, 1993). Эти кластеры могут объединяться друг с другом и со “свободными” молекулами воды за счет экспонированных на их поверхности водородных связей. Интересной особенностью этой модели является то, что из нее следует, что свободно растущие кристаллы воды в снежинках должны обладать 6-лучевой симметрией.
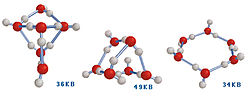
Рис. 33. Варианты устойчивых “квантов воды”, которые состоят из 6 её молекул (Tsai & Jordan, 1993).
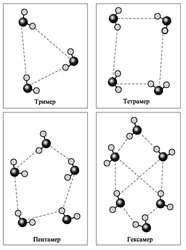
Рис. 34. Структуры триммера, тетрамера, пентамера и гексамера воды
В 1993 году группа исследователей из Калифорнийского университета (г. Беркли, США) под руководством доктора Р.Дж.Сайкалли расшифровала строение триммера воды, в 1996 г. – тетрамера и пентамера, а затем и гексамера воды. Все они цикличны, т. е. образуют довольно устойчивые «кольца».
В 2002 году группе д-ра Хэд-Гордона методом рентгеноструктурного анализа с помощью сверхмощного рентгеновского источника Advanced Light Source (ALS) удалось показать, что молекулы воды способны за счет водородных связей образовывать структуры - "истинные кирпичики" воды, представляющие собой топологические цепочки и кольца из множества молекул. Интерпретируя полученные экспериментальные данные, исследователи считают эти ассоциаты довольно долгоживущими элементами структуры воды.
Структуры кластеров воды были рассчитаны и теоретически, сегодняшняя вычислительная техника позволяет это сделать (рис. 35).
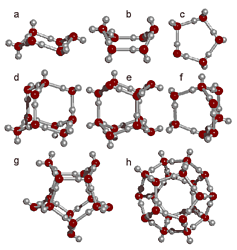
Рис. 35. Возможные кластеры воды.
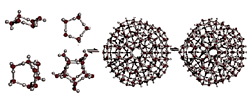
Объединяясь друг с другом, кластеры могут образовывать более сложные структуры:
Рис. 36. Формирование более крупных кластером из мелких кластеров
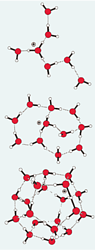
Кластеры, содержащие в своём составе 20 молекул воды оказались более стабильными (рис. 37).
Рис. 37. Формирование устойчивого кластера из 20 молекул H2O.
В 1998 году российский исследователь воды С.В. Зенин первым предложил, что кластеры воды представляют собой иерархию правильных объемных структур, в основе которых лежит кристаллоподобный "квант воды", состоящий из 57 молекул воды, взаимодействующих друг с другом за счет свободных водородных связей. При этом 57 молекул воды (квантов), образуют структуру, напоминающую тетраэдр. Тетраэдр в свою очередь состоит из 4 додекаэдров (правильных 12-гранников). При этом у каждой из молекул воды в простых тетраэдрах сохраняется способность образовывать водородные связи. За счет их простые тетраэдры могут объединяться между собой вершинами, ребрами или гранями, образуя различные кластеры со сложной структурой, например, в форме додекаэдра. 16 квантов воды, в свою очередь образуют структурный элемент, состоящий из 912 молекул воды, которые по модели Зенина практически не способны к взаимодействию за счет образования водородных связей. Вода по мнению С. Зенина на 80% состоит из таких элементов, 15% - кванты-тетраэдры и 3% - классические молекулы воды. Этим и объясняется, например, высокая текучесть жидкости, состоящей из громадных полимеров. Кластеры воды несут в себе информацию крайне высокой плотности. Порядковое число структурных элементов воды воды, по-видимому, так же высоко, как и порядковое число кристаллов. Таким образом, водная среда представляет собой иерархически организованный жидкий кристалл. Изменение положения одного структурного элемента в этом кристалле под действием любого внешнего фактора среды или изменение ориентации окружающих элементов под влиянием добавляемых веществ обеспечивает, согласно гипотезе Зенина, высокую чувствительность информационной системы воды. Такая модель позволяет Зенину объяснить "память воды" и ее информационные свойства (Зенин, 1997).
См. ссылку: www.o8ode.ru/article/learn/
В настоящее время существуют и другие модели воды, объясняющие её аномальные свойства. Так, профессор Мартин Чаплин из Лондонского университета (Martin Chaplin Professor of Applied Science Water and Aqueous Systems Research of the London South Bank University) рассчитал и предположил иную структуру воды, в основе которой лежит икосаэдр (рис. 38).
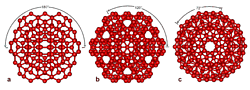
Рис. 38. Формирование икосаэдра воды. Модель М. Чаплина.Согласно этой модели вода состоит из 1820 молекул воды - это в два раза больше, чем в модели Зенина. Гигантский икосаэдр в свою очередь состоит из 13 более мелких структурных элементов. Причем, так же как и у C. Зенина, структура гигантского ассоциата базируется на более мелких образованиях.
См. ссылку: www.o8ode.ru/article/learn/mathmodel.htm
Структура воды свидетельствует о том, что жизнь зародилась в информационной водной среде и впоследствии смогла адаптироваться к самым жёстким внешним условиям. На фотографии 39 ниже показан один из камней с окаменелостями, которые обнаружил инж. Цоло Петков в местечке Стара Планина неподалеку от Шивачево. Показаны также камни с окаменелостями, которые нашeл проф. И. Игнатов на болгарском побережье Черного моря. Исследования, проведенные в лаборатории Евротест контроль, свидетельствуют, что минералы – органогенные. С точки зрения биофизики найденные окаменелости показывают, насколько устойчивым является живой организм даже при самых жестких внешних условиях.

Рис. 39. Фотографии с окаменелостями, инж. Петков, д-р ИгнатовВ Черном море наблюдается другой интересный феномен. На глубинах в воде присутствует сероуглерод (H2S), концентрации которого настолько высоки, что ниже 120-200 метров в Чёрном море жизни почти нет. Причиной наличия таких высоких концентраций сероводорода в водах Черного моря является деятельность особых бактерий Bacterium hydrosuifureurn Penticum, Vibro sulfureus и Microspira aestuaria, способных выделять сероводород при восстановлении сульфатов, солей, растворенных в морской воде. В начале эволюции некоторые хемосинтетические бактерии использовали и энергию, полученную в результате окисления сероводорода (H2S) до серы (S).
В разные геологические эпохи сероводородные зоны занимали различную площадь. Около 3,5 — 3,7 миллиарда лет назад (самый ранний докембрий), когда атмосфера Земли содержала крайне мало кислорода, причем небиологического происхождения (образовывавшегося, например, при остывании базальтовой магмы, по гипотезе геохимика В.И. Вгатова), воды океана были полностью сероводородными. И первая жизнь в океане тоже была анаэробной. Первые живые простейшие, вероятно, мало отличались от современных нам анаэробных бактерий. Даже при отсутствии или малом количестве органического вещества, как это было в первичном океане, анаэробные бактерии могли выделять сероводород. Потом, по мере того как состав атмосферы изменялся, в ней скапливался кислород, сероводородные зоны уменьшались. Этот процесс продолжался сотни миллионов лет. Вероятно, вода Черного моря “сохранила” память о том первичном океане.
Биогенное происхождение имеет также и кислород атмосферы Земли, который образовался за счет процесса фотосинтеза зелеными растениями. Жизнь на Земле, как подтверждают данные палеогеологии, возникла в докембрийскую эпоху. Так, в научной литературе сообщалось о находках ископаемых водорослей в Южной Африке, возраст которых 2,7 млрд. лет. Обнаружены также остатки органического происхождения в южноафриканской формации Фиг-Три, возраст которой приблизительно 3,5 млрд. лет. Академик Б.С. Соколов на основе имеющихся сведений о развитии жизни на нашей планете в раннем докембрии сделал вывод, что биогенные накопления кислорода в океане начались 3,0 — 3,5 млрд. лет назад, а в атмосфере - 2 млрд. лет тому назад.
По мере того как атмосфера Земли в процессе её эволюции эволюционировала из восстановительной в окислительную, постепенно стало происходить „очищение” водной среды – гидросферы от дейтерия. По мнению О.В. Мосина, в те времена существовало два очень важных процесса. В первичной атмосфере Земли не было защитного кислородно-озонового слоя, защищающего поверхность Земли от жёсткого коротковолнового излучения Солнца. Поэтому, вследствие вулканических геотермальных и электрических процессов могло происходить обогащение гидросферы Земли дейтерием. Кроме того под действием излучения мог происходить радиолиз и фотолиз воды (Мосин, 1996).
На более позднем этапе вода могла очищаться от дейтерия при помощи горных пород. Большую роль в этом процессе, по-видимому, играли карстовые породы. В настоящее время содержание дейтерия в карстовых источниках равняется 30-35 г/тонна. В морской воде его содержание 150-200 г/тонна. Очевидно, что когда в воде меньше дейтерия, эволюция происходит быстрее. Если на Земле не начался бы природный процесс очищения от дейтерия, эволюция могла „застыть” на очень низком уровне.
С годами температура Земли понижалась. На определенном этапе эволюции Земли, температура воды была на 10-15 0C выше теперешней. А когда температура снизилась до +3,8 0C, в первую очередь замерзала тяжёлая вода. Это означает, что лед сначала встраивает в свою кристаллическую решётку атомы дейтерия (Игнатов, 2010).
Кристаллическая структура льда напоминает структуру алмаза: каждая молекула Н2O окружена четырьмя ближайшими к ней молекулами, участвующих в формировании водородной связи и находящимися на одинаковых расстояниях от нее, равных 2,76 ангстрем и размещенных в вершинах правильного тетраэдра под углами, равными 109°28' (рис. 40). В связи с низким координационным числом структура льда является сетчатой, что влияет на его невысокую плотность. Природный лёд обычно значительно чище, чем вода, т.к. растворимость веществ (кроме NH4F) во льде крайне низкая. При плавлении льда его кристаллическая структура частично сохраняется в жидкой воде.
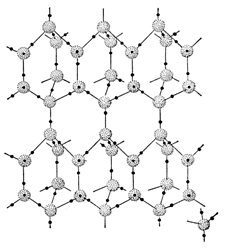
Рис. 40. Структура льда.В настоящее время известно 14 кристаллических модификаций воды, самая распространённая из которых – природный лёд I, имеет гексагональную структуру. Среди модификаций льда есть кристаллические и аморфные модификации, отличающиеся друг от друга взаимным расположением молекул воды и свойствами. Большинство из них образуются при очень низких температурах от -150 0С до -170 0С и высоких давлениях, когда углы водородных связей в молекуле воды искажаются и образуются системы, отличные от гексагональной. Такие условия приближены к космическим и не встречаются на Земле (Таблица).
Наиболее изученным является лёд I-й природной модификации, который распространён в природе в виде материкового, плавающего, подземного льда, а также в виде снега, инея и т.д. В отличие от природного льда льды II, III и V-й модификации могут существовать при очень низких температурах до -170 0С. При нагревании до температуры —150 0С образуется кубический лёд Ic. Лёд IV-й модификации является метастабильной фазой льда. Он образуется гораздо легче и особенно стабилен, если давлению подвергается тяжёлая вода. Кривая плавления льда V и VII исследована до давления 20 Гн/м2 (200 тыс. кгс/см2). При этом давлении лёд VII плавится при температуре 400°С. Лёд VIII является низкотемпературной упорядоченной формой льда VII. Лёд IX — метастабильная фаза, возникающая при переохлаждении льда III и по существу представляющая собой его низкотемпературную форму. Две последние модификации льда — XIII и XIV — открыли ученые из Оксфорда совсем недавно, в 2006 году. Предположение о том, что должны существовать кристаллы льда с моноклинной и ромбической решетками, было трудно подтвердить: вязкость воды при температуре –160°С очень высока, и собраться вместе молекулам переохлажденной воды в таком количестве, чтобы образовался зародыш кристалла, трудно. В лабораторных экспериментах этого удалось достичь с помощью катализатора — соляной кислоты, которая повысила подвижность молекул воды при низких температурах. В земной природе подобные модификации льда образовываться не могут, но они могут встречаться на замерзших спутниках других планет.
Табл. 3. Некоторые данные о структурах модификаций льда
Модификация
Кристаллическая структура
Длины водородных связей, Å
Углы Н—О—Н в тетраэдрах, 0
I
Ic
II
III
V
VI
VII
VIII
IX
Гексагональная
Кубическая
Тригональная
Тетрагональная
Моноклинная
Тетрагональная
Кубическая
Кубическая
Тетрагональная
2,76
2,76
2,75—2,84
2,76—2,8
2,76—2,87
2,79—2,82
2,86
2,86
2,76—2,8
109,5
109,5
80—128
87—141
84—135
76—128
109,5
109,5
87—141
* Примечание: 1 Å = 10-10 м
Природный лёд обычно значительно чище, чем вода, так как при кристаллизации воды в кристаллическую решётку встраиваются молекулы воды, а примеси вытесняются в жидкость. Растущий кристалл льда, тем самым, всегда стремится создать идеальную кристаллическую решетку и вытесняет посторонние вещества. В планетарном масштабе именно замечательный феномен замерзания и таяния воды играет роль гигантского очистительного процесса - вода на Земле постоянно очищает сама себя.
Значение льда для формирования и функционирования жизни трудно переоценить. Лёд оказывает большое влияние на условия обитания и жизнедеятельности растений и животных, на разные виды хозяйственной деятельности человека. Вследствие меньшей, чем у воды, плотности лёд образует на поверхности воды плавучий покров, предохраняющий реки и водоёмы от донного замерзания и сохраняющего жизнь подводному миру. Если бы плотность воды увеличивалась при замерзании, лед оказался бы тяжелее воды и начал тонуть, что привело бы к гибели всех живых существ в реках, озерах и океанах, которые замерзли бы целиком в толще льда, а Земля стала ледяной пустыней, что неизбежно привело бы к гибели всего живого на Земле.
Аналогично воде, кристалл льда способен хранить информацию. Группа ученых провела очень интересный эксперимент в Арктике. Было проведено зондирование во льду на глубине полкилометра. При этом отчётливо детектировались слои льда разных лет. Также был сделан изотопный анализ дейтерия и изотопов кислорода в составе Арктического льда. Согласно исследованиям, вода всегда успевала „запомнить” информацию соответствующего года. Оказалось, что самыми холодными были XV, конец XVII – го и начало XIX века. А самыми теплыми были 1550 и 1930 г.
Но самое удивительное в структуре льда заключается в том, что молекулы воды при низких отрицательных температурах и высоких давлениях внутри нанотрубок могут кристаллизоваться в форме двойной спирали, напоминающую ДНК. Это было доказано компьютерными экспериментами американских учёных под руководством Сяо Чэн Цзэна в Университете штата Небраска (США) (рис. 41).
Вода в моделируемом эксперименте "помещалась" в нанотрубки диаметром от 1,35 до 1,90 нм. под высоким давлением, варьирующимися в разных опытах от 10 до 40000 атмосфер. После этого задавали температуру, которая во всех экспериментах имела значение -23°C. Запас по сравнению с температурой замерзания воды делался в связи с тем, что с повышением давления температура плавления водяного льда понижается.
Рис. 41. Общий вид структуры воды в нанотрубках (изображение New Scientist)Молекулы воды связаны между собой посредством водородных связей, расстояние между атомами кислорода и водорода равно 96 пм, а между двумя водородами - 150 пм. В твёрдом состоянии атом кислорода участвует в образовании двух водородных связей с соседними молекулами воды. При этом отдельные молекулы H2O соприкасаются друг с другом разноимёнными полюсами. Таким образом, образуются слои, в которых каждая молекула связана с тремя молекулами своего слоя и одной из соседнего. В результате, кристаллическая структура льда состоит из шестигранных "трубок" соединенных между собой, как пчелиные соты.
Согласно данным компьютерного моделирования, при диаметре трубки в 1,35 нм и давлении в 40000 атмосфер водородные связи искривились, приведя к образованию спирали с двойной стенкой. Внутренняя стенка этой структуры является скрученной в четверо спиралью, а внешняя состоит из четырёх двойных спиралей, похожих на структуру молекулы ДНК.
Последний факт накладывает отпечаток не только на эволюцию наших представлений о воде, но и эволюцию ранней жизни и самой молекулы ДНК. Если предположить, что в эпоху зарождения жизни криолитные глинистые породы имели форму нанотрубок, возникает вопрос - не могла ли вода, сорбированная в них служить структурной основой – матрицей для синтеза ДНК и считывания информации? Возможно, поэтому спиральная структура ДНК повторяет спиральную структуру воды в нанотрубках. Как сообщает журнал New Scientist, теперь нашим зарубежным коллегам предстоит подтвердить существование таких макромолекул воды в реальных экспериментальных условиях с использованием инфракрасной спектроскопии и спектроскопии нейтронного рассеяния.
Такие исследования нанокристаллов льда были проведены в 2007 году в Центре нанотехнологий в Лондоне и Моргенштерн из университета им. Лейбница в Ганновере (рис. 42). Водяной пар охлаждался над поверхностью металлической пластины, находящейся при температуре 5 градусов Кельвина. Вскоре с помощью сканирующего туннельного микроскопа на пластине удалось наблюдать гексамер (шесть соединенных между собой молекул воды) - мельчайшую снежинку. Это самый маленький из возможных кластеров льда. Ученые наблюдали также кластеры, содержащие семь, восемь и девять молекул.
Рис. 42. Изображение гексамера воды, полученное с помощью сканирующего туннельного микроскопа Размер гексамера в поперечнике - около 1 нм. Фото London Centre for NanotechnologyРазработка технологии, позволившей получить изображение гексамера воды – само по себе важное научное достижение. Для наблюдения пришлось сократить зондирующий ток до минимума, что и позволило предохранить слабые связи между отдельными молекулами воды от разрушения вследствие процесса наблюдения. Помимо этого, в работе были использованы теоретические подходы квантовой механики. Комплексный подход дал впечатляющие результаты.
В отличие от кристаллического льда, где между всеми молекулами воды энергия связи одинакова, в нанокластерах есть чередование сильных и слабых связей (и соответствующих расстояний) между отдельными молекулами. Получены также важные результаты о способности молекул воды к распределению водородных связей и к их связи с поверхностью металла.
Теоретические анализы Опарина, эксперименты Миллера, Фокса и др. бесспорно доказывают, что в природе могут структурироваться органические молекулы из неорганических. Главным источником энергии в их экспериментах является тепло. В природе это солнечная радиация и энергия магмы. Другой очень существенный вывод – это, что зарождение первых органических форм жизни возможно происходило в щелочной среде. Во всех случаях наблюдается самоорганизация живой материи.
В XIX в. Пастер обратил внимание, что в неживой природе молекулы являются симметричными. А в живой природе наблюдается зеркальная ассиметрия молекул. Белки состоят из левовращающих аминокислот. Данное свойство определяется вращением молекулой плоскости поляризации света. Как объяснить феномен?
Возможно, наличие ассиметрии в органических молекулах проявилось, когда открытая система, предшествувающая биосфере, находилась в крайне неравновесном критическом состоянии.
Произошел скачкообразный эволюционный переход, что является характерной особенностью самоорганизации. Примером такого состояния являются эксперименты, где водные молекулы напоминают ДНК в нанотрубах. Переход из симметричных молекул неживой природы к ассиметричным биомолекулам живой мог произойти на начальном этапе химической эволюции, как самоорганизация материи. Проф. Антонов доказал, что вода тоже является открытой системой и обменивается энергией и веществом с окружающей средой (проф. Антонов, 1992).
Такие экстремальные условия наблюдаются при вулканической деятельности, разрядах в атмосфере молодой Земли. Минеральная вода, взаимодействуюшая с карбонатом кальция, а также морская вода, являются благоприятным спектром для сохранения самоорганизующихся структур. Эффект Кирлиана в лабораторных условиях создает селективный разряд, позволяющий наблюдать излучение света атомами или молекулами. При экспериментах Миллера также создаются неравновесные экстремальные условия с газовым разрядом.
Кирлиановая аура, газоразрядное свечение - плазменное свечение электрического разряда наблюдается на поверхности предметов, находящихся в переменном электрическом поле высокой частоты 10-100 кГц, при котором возникает поверхностное натяжение между электродом и исследуемым объектом от 5 до 30 кВ. Эффект Кирлиана наблюдается подобно молниям или статическому разряду на любых биологических, органических объектах, а также на неорганических образцах различного характера.
Для визуализации газоразрядного свечения на электрод подаётся высокое переменное напряжение с высокой частотой - от 1 до 40 киловольт при 200-15000 Герц. Другим электродом служит сам объект. Оба электрода разделены изолятором и тонким слоем воздуха, молекулы которого подвергаются диссоциации под действием сильного магнитного поля, возникающего между электродом и объектом. В этом слое воздуха, находящемся между объектом и электродом, происходит три процесса.
- Первый процесс заключается в ионизации и образовании атомарного азота;
- Второй процесс – ионизация молекул воздуха и образования ионного тока – коронного разряда между объектом и электродом. Форма короны свечения, её плотность и т.п. определяются собственным электромагнитным излучением объекта.
- Третий процесс - переход электронов с низших на высшие энергетические уровни и обратно. При этом переходе электронов происходит излучение кванта света. Величина перехода электрона зависит от собственного электромагнитного поля исследуемого объекта. Поэтому в различных точках поля, окружающего объект, электроны получают разные импульсы, т.е. перескакивают на разные энергетические уровни, что приводит к испусканию квантов света разной длины и энергии.
Последние регистрируются человеческим глазом или цветной фотобумагой в качестве различных цветов, которые в зависимости от объекта могут окрашивать корону свечения в различные цвета. Эти три процесса в своей совокупности дают общую картину Кирлиан-эффекта, который позволяет изучать электромагнитное поле объекта. Эффект Кирлиана, таким образом, связан с биоэлектрической аурой живого объекта.
См. ссылку: www.o8ode.ru/article/learn/kirlian.htm
В 2010 г. проф. Игнатов провел исключительно прецезионнный эксперимент. Им были сфотографированы Кирлиановые (электрические) фотографии водных капель различных видов воды (рис. 43 и рис. 44). Эксперимент доказал зависимость между электрической аурой и вращением плоскости поляризации водных молекул в соответствующей воде (д-р Игнатов, 2010 ).
Рис. 43. Цифровая Кирлиановая фотография водных капель : 1 капля – водопроводной воды; 2 капля горной воды, Тетевен, Болгария; 3 капля морской воды, Хамамет, Тунис; 4 капля – карстовая и минеральная вода, Златна Панега, Болгария; д-р Игнатов, инж. Яцевич, 2010
Рис. 44. Кирлиановая фотография водных капель на пленке: 1 капля – водопроводной воды; 2 капля горной воды, Тетевен, Болгария; 3 капля морской воды, Хамамет, Тунис; 4 капля – карстовая и минеральная вода, Златна Панега, Болгария; д-р Игнатов, инж. Яцевич, 2010
Молекулы воды являются полярными и ориентируются в зависимости от внешнего электрического поля. При Кирлиановом методе проводимость объекта не отражается на электрическом изображении. Его формирование зависит от распределения диэлектрической проницаемости (проф. Антонов, 1984).
Эффект Кирлиана связан и с биоэлектрической аурой живого объекта. При исследовании спектра водных капель, электрическая аура связана с полярностью водных молекул и их расположением в результате приложенного внешнего электрического поля.
Поляризация – явление, связанное с электромагнитными волнами. При нем электромагнитное поле осциллирует (колеблется) в одной определенной плоскости. С увеличением температуры уменьшается диэлектрическая проницаемость. У воды высокая диэлектрическая проницаемость и это важно для ее свойств как растворитель. Кирлиановые ауры трех водных капель указывают на то, что разная вода по разному взаимодействует с электрическим полем.
Фотографирование Кирлианового спектра является одним из физических методов, при которых изображение самого высокого качества получается на фотопленке. Эксперимент доказал, что в зависимости от различия воды получается различная электрическая аура (Д-р Игнатов, 2010).
См. ссылку: www.medicalbiophysics.dir.bg/ru/kirlian_effect.html
При исследованиях Кирлианом в 1996 году проф. Коротков указывает на интересный феномен. В 2008 г. проф. И. Игнатов подтвердил эксперимент. Кирлиановая аура сильно меняется при воздействии на воду биофизическими полями. По мнению Короткова, наблюдаемый эффект можно объяснить тем, что «Вода может сохранять, распространять и изменять информацию, которую получает».
Пики в неравновесном энергетическом спектре растительного сока и минеральной воды, взаимодействующей с карбонатом кальция, находятся при -0,1112, -0,1187, -0,1262, -0,1287 и -0,1387 еV.
Было проведено исследование контрольной пробы дейонизированной водой и той же самой водой после воздействия инж. Дроссинакиса (Dipl. Eng. Drossinakis, 2001, 2008) биофизическими полями.
См. ссылку: www.medicalbiophysics.dir.bg/en/kirlian_gallery.html#water_drops
Одновременно были сделаны цветные Кирлиановые фотографии двух проб. При сделанном спектральном анализе той же самой воды наблюдались следующие пики - при - 0,1112, -0,1187, -0,1262 и -0,1387 еV. График показывает статистически достоверный результат при биовоздействии на группу, состоящую из 30 человек. Анализы показывают биорезонансное взаимодействие между биофизическими полями и молекулами воды.
Детектируемые пики связаны с образованием относительно стабильных кластерных формаций. Полученный результат является очень важным, потому что доказывается возможность сохранить биологические структуры с помощью биофизических полей, на биорезонансном принципе. (Д-р Игнатов, 2005).
См. ссылку: www.medicalbiophysics.dir.bg/ru/water_memory.html
В процессе зарождения и эволюции живой материи молекулы воды, клетки и ткани генерируют слабые электромагнитые поля (Игнатов, 1998). Кластеры молекул воды – самые мелкие и нестабильные самоорганизующиеся системы в природе (Игнатов, 2005). Живые организмы, в том числе и человек, представляют собой сложные, самоорганизующиеся системы. Они открыты для непрерывного обмена веществами и энергией с окружающей средой. Изменения в открытых системах относительно устойчивы во времени. Устойчивое соотношение между компонентами в одной открытой системе называется диссипативной структурой (проф. Николис, проф. Пригожин, 1973). Экспериментально доказано, что вода также является самоорганизующейся системой (проф. Антонов, инж. Гылыбова, 1992). Предполагается, что изменения, происходящие в воде в результате внешних воздействий, также будут относительно устойчивы во времени. Определены амплитуды при биорезонансном взаимодействии биофизических полей с молекулами воды (д-р Игнатов, 2005). При этом чрезвычайно интересен вопрос «памяти» воды. Едва ли без этого ее качества, возможно, объяснить зарождение живой материи. Сам создатель биорезонансной теории в 1980 году проф. А.П. Дубров доказал реальность биорезонансного взаимодействия в живых организмах.
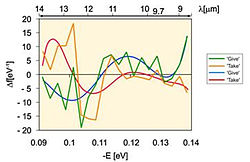
Рис. 45. Д-р И. Игнатов доказал, что главный биорезонансный пик биорезонансного взаимодействия между молекулами воды и биофизическими полями получается при 9,7 µm. Инж. ЯцевичПроведенные эксперименты с электрической аурой водных капель доказали самоорганизацию воды в результате поляризации водных кластеров с тенденцией к сохранению информации в живой клетке (рис. 49). Кирлиановое свечение связано в основном с диэлектрической проницаемостью и, соответственно, с поляризацией водных кластеров электрическим полем. Метод Кирлиана связан с электрическим разрядом. Результаты указывают на роль электрического разряда в зарождении живой материи в различной воде. При экспериментах Миллера, а также в первичной атмосфере Земли используется газовый разряд.
Водные молекулы структурированы лучше всего в минеральных водах, взаимодействующих сначала с карбонатом кальция, а затем в морской воде, в зависимости от их поляризации. Проведенный спектральный анализ с водой показал, что у воды с более выраженными электрическими аурами, сильнее выражены пики в спектре. В древней атмосфере существовали электрические разряды, и данные анализы доказывают тенденцию к раскладке и самоорганизации водных кластеров. (Д-р Игнатов, 2010).
См. ссылку: www.congress-euromedica.de/abstrakt2010/which-water-is-optimal-for-the-origin-generation-of-life-.html
В Калифорнии ревю указывается на проведенный эксперимент с водой, чей состав близок к составу термальных источников в первичном океане. В реакционный сосуд с водой, содержащей диоксид углерода и железо, нагретый до температуры 130 0С был добавлен хром и сульфид никеля. После этого наблюдалось образование маленьких мембраноподобных образований вокруг молекул. Эксперимент доказывает процесс образования в воде самоорганизующихся мембранных структур. Эксперимент базировался на основе гипотезы Ваштерхаузера (Wächtershäuse), связанной с возникновением жизни в условиях термальных источников. Однако, в составе термальной воды нет кальция и кремния, необходимых для формирования скелета живых организмов. Вероятно, живые формы, зародившиеся на ранних этапах эволюции впоследствии исчезли или эволюционировали до микроводорослей и других форм. Важным обстоятельством является то, что в этих внешних условиях наблюдается тенденция к самоорганизации живой материи. Авторы эксперимента указывают, что щелочная вода – один из факторов для структурирования мембран. Минеральная вода, взаимодействующая с карбонатом кальция, как и морская вода, являются щелочными.

Рис. 46. Пузырьки в карстовом источнике, Златна Панега, Тетевенский край, Болгария. фотограф: Александр ИгнатовКогда мы рассматриваем вопрос о самоорганизации в природе, наблюдается чрезвычайно интересный пример в карстовых источниках Златной Панеги, Тетевенский край. Водоросли окружены пузырьками размерами 3-5 мм. Пузырьки сохраняются достаточно долго – часами или даже днями. Сама вода, которая по спектру похожа на растения, «старается» сохранить самоорганизовавшиеся структуры. Во время исследования, температура окружающей среды была 5 0C. (рис. 46).
Ярким примером самоорганизованных структур является род подвижных колониальных микроорганизмов Вольвокс, относящийся к зелёным водорослям, в которых насчитывается от 200 до 50 тысяч клеток, соединённых протоплазматическими нитями, а полость заполнена жидкой слизью (рис. 47). Клетки Вольвокса образуют шаровидное тельце размером до 3 мм. От каждой клетки наружу отходят два жгутика, колебания которых обеспечивают подвижность Вольвокса. Благодаря движению жгутиков вольвокс перекатывается в воде. Каждая клетка выглядит как самостоятельное простейшее, но все вместе они образуют целую колонию, поскольку они соединены друг с другом. При размножении вольвокса некоторые клетки погружаются в глубь шарика, где они делятся, образуя несколько новых молодых колоний, которые выходят из старого вольвокса наружу.
Рис. 47. ВольвоксВольвокс – самый примитивный многоклеточный организм на Земле – он представляет сферу из соединенных между собой фотосинтезирующих клеток в слизистом матриксе. При этом, у такого простого многоклеточного организма уже имеется клеточная дифференциация: одни клетки выполняют роль соматических, а другие становятся репродуктивными. В свою очередь из репродуктивных клеток могут формироваться дочерние колонии. Как и у других водорослей, в жизненном цикле вольвокса имеется бесполое и половое поколение, то есть одни колонии получаются вегетативным путем (без оплодотворения), а другие — в результате слияния половых клеток (рис. 48).
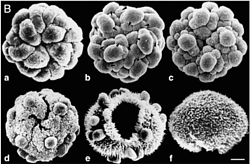
Рис. 48. Этапы развития Вольвокса. Из статьи D. L. Kirk (2005).Развитие вольвокса имеет ряд удивительных особенностей самоорганизации, усложнения, сохранения и обмен информации живой материи. Однако самым любопытным фактом, является то, что такое важное эволюционное событие, как появление многоклеточности, на протяжение эволюции происходило неоднократно у разных групп животных и растений. Однако, рекордсменом, достойным книги Гиннеса, является семейство водорослей, к которому принадлежит вольвокс: многоклеточность в нем возникала независимо не менее 9 раз.
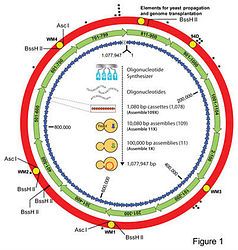
Рис. 49. Клетка с геномом другой клетки, К. Вентер, 2010В 2010 г. был осуществлён эксперимент американского учёного Крейга Вентера, который доказал способность передачи информации от одной клетки к другой. Он химическим путем модифицировал геном бактерии Mycoplasma mycoides и вставил его в клетку другого микроорганизма — Mycoplasma capricolum, из которой перед этим были удалены все гены (рис. 49). Полученный генный конструкт выжил, стал размножаться и повел себя как обычная бактерия Mycoplasma mycoides. Таким образом, впервые в мире удалось создать искусственный геном – своеобразный биокомпьютер и заставить живую клетку жить с этим генетическим кодом.
Человеку удалось создать гибридный организм из двух прокариот в отличие от природы, создавшей жизнь до уровня клетки из воды, атомов и молекул окружающей среды.
Так, на основе многочисленных исследований, доказательств и модельных экспериментов человеческий ум стремится постичь загадку происхождения и эволюции жизни, зародившейся в воде и покорившая впоследствии все природные стихии.
Авторы:
проф., д-р И. Игнатов (Болгария)
к.х.н. О. В. Мосин (Россия)
Литературные источники:
Денько Е.И. Влияние тяжелой воды D2O на клетки животных, растений и микроорганизмы // Успехи совр. биол., 1970, т. 20. № 1 (4). с. 41-85.
Лобышев В.Н., Калиниченко Л.П. Изотопные эффекты D2O в биологических системах. М.: Наука, 1978. – 215 с.
Ерёмин В.А., Чекулаева Л.Н. Выращивание бактерий Micrococcus Lysodeikticus на дейтерированной среде // Микробиология, 1978.
Бердышев Г.Д., Варнавский И.Н., Прилипенко В.Д. Аквабиотика – наука о роли воды в жизненных процессах. В кн.: Информоенергетика ІІІ-го тисячоліття: соціолого-синергетичні та медично-екологічні підходи. Київ – Кривий Ріг: ЗАТ “ЗТНВФ “Коло”, 2003, с. 22–28.
Варнавский И.Н., Бердышев Г.Д., Прилипенко В.Д. Целебная реликтовая вода – открытие третьего тысячелетия // Вопросы химии и химической технологии, 2002, № 5, с. 168 – 174.
Н. А. Заренков. Неевклидов Вольвокс, или Почему не следует преподавать вольвокса в курсе зоологии // Журнал общей биологии, 2006, т. 67, № 1, с. 53-61.
Calvin. М., Chemical evolution, Proc. Roy. Soc. (London), Ser. A, 288, 441-466 (1965).
Eck R.V., Lipincott E.R., Dayhoff M.O., Pratt Y.T. Thermodynamic equilibrium and the inorganic origin of organic compounds // Science, 153,628-633 (1966).
Fox S.W. A theory of macromolecular and cellular origins // Nature, 205, 328-340 (1965).
Fox S. W. Simulated natural experiments in spontaneous organization of morphological units from proteinoid. In: S. W. Fox (Editor), The Origins of Prebiological Systems, Academic Press, New York, N. Y., pp. 361-373, 1965.
Fox S.W. A new view of the "synthesis of life" // Quart. J. Florida Acad. Sci., 31, 1-15 (1968).
Fox S. W., WaehneldtT. F. The thermal synthesis of neutral and basic proteinoids // Biochim. Biophys. Acta, 160, 246-249 1968).
Harada I., Fox S. W. Thermal synthesis of natural ammo-acids from a postulated primitive terrestrial atmosphere // Nature, 201, 335-336 (1964).
Mathews C. N., Moser R. Peptide synthesis from hydrogen-cyanide and water // Nature, 215, 1230-1234 (1968).
Miller S. L., Formation of Organic Compounds on the Primitive Earth. In: Опарин А. И. (ред.), The Origin of Life on Earth, Pergamon, London, 123-135, 1959.
Опарин А.И. Пути начального формирования обмена веществ и искусственное моделирование этого формирования в коацерватных каплях. In: S. W. Fox (Editor), Origins of Prebiological Systems, Academic Press, New York, N. Y., 331-341, 1965 (Происхождение предбиологических систем, изд-во "Мир", стр. 335, М., 1966).
Оro J. Investigation of organo-chemical evolution. In: G. Marnikunian and М. Н. Briggs (Editors), Current Aspects of Exobiology, Pergamon,London, 13-76, 1965.
Оrо J. Prebiological organic systems. In: S. W. Fox (Editor), The Origin of Prebiological Systems, Academic Press, New York, N. Y., 137-162, 1965 (Происхождение предбиологических систем, изд-во "Мир", стр. 144, М., 1966).
Ponnamperuma C. Abiological synthesis of some nucleic acid constituents. In: S. W. Fox (Editor), The Origin of Prebiological Systems, Academic Press, New York, N. Y., 221-236.
Ponnamperuma С., Gabel N. Prebiological synthesis of organic compounds. In: A. Renbaum and R. F. Landell (Editors), Chemistry in Space Research, 1969.
Ponnamperuma C., Mack R. Nucleotide synthesis under possible primitive earth conditions, Science, 148, 1221-1223 (1965).
Steinman G., Smith A. E., Silver J. Synthesis of a sulfur-containing amino acid under simulated prebiotic conditions // Science, 159, 1108-1109(1968).
С.В. Зенин, Б.В. Тяглов. Гидрофобная модель структуры ассоциатов молекул воды. Ж.Физ.химии.1994.Т.68. №4.С.636-641.
С.В.Зенин, Б.В.Тяглов. Природа гидрофобного взаимодействия. Возникновение ориентационных полей в водных растворах. Ж.Физ.химии.1994.Т.68.№3.С.500-503.
Мосин О.В., Складнев Д.А., Швец В.И. Исследование процесса физиологической адаптации метилотрофных бактерий к 2H2O / Автотрофные микроорганизмы: Конф. памяти акад. РАН Е.Н.Кондратьевой. Москва: МГУ, 23-25 апреля, 1996. C. 113.
Мосин О.В., Складнев Д.А., Швец. Исследование физиологической адаптации бактерий на тяжёловодородной среде // Биотехнология. 1999. № 8.
Мосин О.В., Игнатов И. Осознание воды как субстанции жизни // // Сознание и физическая реальность. - М.: Изд. Фолиум, 2011. Т. 16. № 12. С. 9-21.
Мосин О.В., Игнатов И. Структура воды и физическая реальность. 2011. Т. 17. № 9. С. 16-31.
Мосин О.В., Игнатов И. Разделение тяжелых изотопов дейтерия (D), трития (T) и кислорода (18O) из воды // Чистая вода: Проблемы и решения. 2011. № 3-4. С. 69-78.
Мосин О.В. Вода и происхождение жизни // Биология. М: Изд. дом “Первое сентября”. 2011. № 15. С. 4-9.
Мосин О.В., Игнатов И. Биологические основы адаптации бактерий к тяжелой воде (D2O) // Сознание и физическая реальность. - М.: Изд. Фолиум, 2012. Т. 17. № 11. С. 18-29.
Игнатов И., Мосин О.В. Загадки ледяных кристаллов // Сознание и физическая реальность. - М.: Изд. Фолиум, 2012. Т. 17. № 5. С. 21-31.
Игнатов И., Мосин О.В. Изотопный состав воды и ее исследование в процессах моделирования первичной гидросферы // Сознание и физическая реальность. - М.: Изд. Фолиум, 2013. Т. 18. № 4. С. 26-32.
Мосин О.В., Игнатов И. Загадки льда // Природа и человек. 2013. № 12. С. 30-33.
Мосин О.В., И. Игнатов. Изотопные эффекты дейтерия в клетках бактерий и микроводорослей при росте на тяжелой воде (D2O) // Вода: химия и экология. 2012. № 3. C. 83-94.
Ignatov I., Mosin O.V. Cellular Adaptation to Deuterium Oxide (2H2O) / Das Internationale Symposium “Okologishe, Technologishe und Rechtliche Aspekte der Lebensversorgung” Euro-Eco, 29-30 November 2012, Hannover: Europäische akademie für naturwissenschaften, P. 62-63, www.eu-eco.eu/tl_files/downloads/brosurECO2012.pdf.
Ignatov I., Mosin, O.V. Isotopic Composition of Water and its Temperature in Modeling of Primordial Hydrosphere Experiments / Das Internationale Symposium “Okologishe, Technologishe und Rechtliche Aspekte der Lebensversorgung” Euro-Eco, 29-30 November 2012, Hannover: Europäische akademie für naturwissenschaften, P. 63-64, www.eu-eco.eu/tl_files/downloads/brosurECO2012.pdf.
Ignatov I., Mosin O.V. Hot Mineral Water with Deuterium Molecules for the Origin of Life and Living Matter / in: Congress “Science, Information, Consciousness”. Saint-Petersburg Technical University. 2012. P. 137-149.
Mосин О.В., Игнатов И. Адаптация к тяжелой воде. Фенотипический или генотипический феномен? // Сознание и физическая реальность. 2012. Т. 17. № 4. С. 25-36.
Mосин О.В., Игнатов И. Структура воды // Химия. Москва: издат. Первое сентября. 2012. № 11. С. 24-27.
Mосин О.В., Игнатов И. Исследование изотопных эффектов тяжелой воды в биологических системах на примере клеток прокариот и эукариот //Биомедицина. 2012. № 1. (1-3). С. 31-50.
Мосин О.В., Игнатов И. Изотопный состав воды и происхождение жизни // Биология в школе. 2013. № 3. С. 5-16.
Игнатов И., Мосин О.В. Изотопный состав воды и долголетие // Вестник развития науки и образования. Издательство: Издательский дом Наука образования (Москва)ISSN: 1991-9484. 2013. № 2. С. 3-13.
Игнатов И., Мосин О.В. Математические модели, описывающие наноструктуру воды и нанокластеры // Вестник развития науки и образования. 2013. Издательство: Издательский дом Наука образования (Москва)ISSN: 1991-9484. № 3. С. 3-30.
Игнатов И., Мосин О.В. // Нано- и микросистемная техника. 2014. № 3. С. 47-56.
Игнатов И., Мосин О.В. // Нано- и микросистемная техника. 2014. № 8. С. 8-15.
Игнатов И., Мосин О.В. Математические модели, описывающие наноструктуру воды и нанокластеры // Наноинженерия. 2013. № 8. С. 23-34.
Игнатов И., Мосин О.В. Цветной коронный спектральный анализ Кирлиана в моделировании неравновесных условий с газовым электрическим разрядом, имитирующих первичную атмосферу // Наноинженерия. 2013. № 12. С. 40-51.
Игнатов И., Мосин О.В. Структурные модели воды, описывающие циклические нанокластеры // Наноматериалы и наноструктуры – XXI Век. 2013. № 4. C. 25-34.
Игнатов И., Мосин О.В., Великов Б., Бауэр Э., Тыминский Г. Горная вода как главный фактор долголетия в исследовании феномена долголетия в горных районах Болгарии // Вопросы биологической, медицинской и фармацевтической химии. 2014. № 10. С. 27-41.
Игнатов И., Мосин О.В. Биологическое воздействие дейтерия на клетки прокариот и эукариот // Технологии живых систем. 2014. № 2. С. 21-33.
Мосин О.В., Игнатов И. Биологическое воздействие дейтерия на клетки прокариот и эукариот // Астраханский вестник экологического образования. Издательство: Нижневолжский экоцентр (Астрахань)ISSN: 2304-5957. 2013. №3 (25). С. 124-138.
Игнатов И., Мосин О.В. (2013) Изотопный состав воды и долголетие // Астраханский Вестник экологического образования. Издательство: Нижневолжский экоцентр (Астрахань) ISSN: 2304-5957. 2013. № 2. С. 127-136.
Игнатов И., Мосин О.В. Изотопный состав воды и ее температура в процессе эволюционного развития жизни и живой материи // Астраханский Вестник экологического образования. Издательство: Нижневолжский экоцентр (Астрахань) ISSN: 2304-5957. 2013. № 1 (23). С. 113-127.
Игнатов И., Мосин О.В. Изотопный состав воды и ее исследование в процессах моделирования первичной гидросферы // Сознание и физическая реальность. Издательство: ООО Фолиум (Москва)ISSN: 1027-4359. 2013. №4. С. 26-32.
Игнатов И., Мосин О.В. Изотопный состав воды и долголетие // Сознание и физическая реальность. Издательство: ООО Фолиум (Москва) ISSN: 1027-4359. 2013. № 1. С. 26-32.
Игнатов И., Мосин О.В. Математические модели, описывающие нанокластеры воды // Сознание и физическая реальность. Издательство: ООО Фолиум (Москва)ISSN: 1027-4359. 2013. № 9. С. 20-32.
Мосин О.В., Игнатов И. Биологическое воздействие дейтерия на клетки прокариот и эукариот // Разработка и регистрация лекарственных средств. Издательство: Фармконтракт (Москва) ISSN: 2305-2066. 2014. № 2(7). С. 122-131.
Игнатов И., Мосин О.В. Изотопный состав воды как основной фактор долголетия // Разработка и регистрация лекарственных средств. Издательство: Фармконтракт (Москва) ISSN: 2305-2066. 2014. № 4(9). С. 146-155.
Mosin O.V., Ignatov I. Biological influence of deuterium on procariotic and eukaryotic cells // European Journal of Molecular Biotechnology. Издательство: Научный издательский дом Исследователь (Сочи) ISSN: 2310-6255. 2014. Vol 1. № 3. С. 11-24.
Ignatov I., Mosin O.V. Kirlian Effect in Modeling of Non-Equilibrium Conditions With the Gas Electric Discharge, Simulating Primary Atmosphere // Nanotechnology Research and Practice. Издательство: Научный издательский дом Исследователь (Сочи)ISSN: 2310-6255. 2014. Vol.(3). № 3. P. 127-140.
Ignatov I., Mosin O.V. Structural Mathematical Models Describing Water Clusters // Nanotechnology Research and Practice. Издательство: Научный издательский дом Исследователь (Сочи) ISSN: 2310-6255. 2014. Vol.(3). № 3. P. 141-158.
Ignatov I., Mosin O.V. Kirlian Effect in Modeling of Non-Equilibrium Conditions With the Gas Electric Discharge, Simulating Primary Atmosphere // Nanotechnology Research and Practice. Издательство: Научный издательский дом Исследователь (Сочи)ISSN: 2310-6255. 2014. Vol.(3). № 3. P. 127-140.
Игнатов И., Мосин О.В. Изотопный состав воды и долголетие // Вода: Гигиена и экология. 2013. № 3-4 (1). С. 22-32.
Ignatov I., Mosin O.V. Possible processes for origin of life and living matter with modeling of physiological processes of bacterium Bacillus subtilis in heavy water as model system // Journal of Natural Sciences Research. 2013. V. 3(9). P. 65-76.
Ignatov I., Mosin O.V. Modeling of possible processes for origin of life and living matter in hot mineral and seawater with deuterium // Journal of Environment and Earth Science. 2013. V. 3(14). P. 103-118.
Ignatov I., Mosin O.V. Structural mathematical models describing water clusters // Journal of Mathematical Theory and Modeling. 2013. V. 3(11). P. 72-87.
Игнатов И., Мосин О. В. Изотопный состав воды и ее температура в процессе эволюционного происхождения жизни и живой материи // Научное обозрение. 2013 № 1. С. 17-27.
Ignatov I., Mosin O.V. Isotopic composition of water and its temperature in modeling primodial hydrosphere experiments / Mat. VIII Miedzynarodowej naukowi-praktycznej konferencji “Perspektywiczne opracowania sa nauka i technikami – 2012”. 07-15 listopada 2012. Vol. 15. Nauk biologicznych Weterynaria. Przemysl: Nauka i studia. 2012. P. 41-49.
Мосин О.В., Игнатов И. Биологическое воздействие дейтерия на клетки различных микроорганизмов / Материали за IX международна научна практична конференция “Настоящи изследвания и развитие - 2013”. 17-25 януари 2013. София: Бял ГРАД-БГ. 2013. Том 24. С. 80-86.
Игнатов И., Мосин О.В. Представления о возникновении жизни в свете изучения свойств природной воды // Химия. Изд. Первое сентября. 2013. № 10. С. 3-9: 4 ил. - Библиогр.: с. 9 (25 назв.).
Игнатов И., Мосин О.В. Изотопный состав воды и долголетие // Химия - Первое сентября. 2013. № 4. С. 12-16.
Игнатов И., Мосин О.В., Великов Б. Математические модели, описывающие наноструктуру воды // Интернет-журнал «Науковедение». 2013. № 3. С. 1-25 [Электронный ресурс] - М.: Науковедение, 2013. - Режим доступа: naukovedenie.ru/PDF/04tvn313.pdf.
Игнатов И., Мосин О.В. Цветной коронный (Кирлиановый) спектральный анализ в моделировании неравновесных условий с газовым электрическим разрядом, имитирующих первичную атмосферу. Эксперименты С. Миллера // Интернет-журнал «Науковедение». 2013. № 3. С. 1-15. [Электронный ресурс] - М.: Науковедение, 2013. - Режим доступа: naukovedenie.ru/PDF/05tvn313.pdf.
Игнатов И., Мосин О.В. Возможные процессы возникновения жизни и живой материи в обогащенной дейтерием горячей минеральной воде // Интернет-журнал «Науковедение». 2013. № 3. [Электронный ресурс] - М.: Науковедение, 2013. - Режим доступа: С. 1-12. naukovedenie.ru/PDF/97tvn313.pdf.
Игнатов И. (Ignatov I), Мосин О.В. (Mosin O.V.) Structure of water for origin of life and living matter // Интернет-журнал «Науковедение». 2013. № 2. С. 1-16. [Электронный ресурс] - М.: Науковедение, 2013. - Режим доступа: naukovedenie.ru/PDF/05tvn213.pdf.
Игнатов И. (Ignatov I), Мосин О.В. (Mosin O.V.) Origin of life and living matter in hot mineral water // Интернет-журнал «Науковедение». 2013. № 2. С. 1-19 [Электронный ресурс] - М.: Науковедение, 2013. - Режим доступа: naukovedenie.ru/PDF/04tvn213.pdf.
Игнатов И., Мосин О.В. Изотопный состав воды и ее температура в процессе эволюционного происхождения жизни и живой материи // Интернет-журнал «Науковедение». 2013. № 1. С. 1-16 [Электронный ресурс] - М.: Науковедение, 2013. - Режим доступа: naukovedenie.ru/PDF/42tvn113.pdf.
Игнатов И., Мосин О.В. Структурные модели воды, описывающие циклические нанокластеры // Нанотехника. 2013. № 3. С. 46-55.
Ignatov I., Mosin O.V., Velikov B., Bauer E. Tyminski G. Longevity Factors and Mountain Water as Factor. Research in Mountain and Fields Areas in Bulgaria // Civil and Environmental Research. 2014. Vol. 30. № 4. P. 51-60.
Mosin O.V., Ignatov I. Biological Influence of Deuterium on Prokaryotic and Eukaryotic Cells // Journal of Medicine, Physiology, Biophysics. 2014. Vol. 1. P. 52-72.
Ignatov I., Mosin O.V. Research of Isotopic Effects of Deuterium in Cells of Microorganisms in the Presence of D2O in IR Spectra in Hot Mineral Water for Origin of Life // Journal of Medicine, Physiology and Biophysics. 2014. Vol. 4. P. 45-57.
Ignatov I., Mosin O.V. Nature of Hydrogen Bonds in Liquids and Crystals. Ice Crystal Modifications and Their Physical Characteristics // Journal of Medicine, Physiology and Biophysics. 2014. Vol. 4. P. 58-80.
Ignatov I., Mosin O.V. Modeling of Possible Conditions for Origin of First Organic Forms in hot Mineral Water // European Journal of Molecular Biotechnology. 2014. Vol.(6). № 4. P. 169-179.
Mosin O.V., Ignatov I., Skladnev D., Shvets V. Studying of Phenomenon of Biological Adaptation to Heavy Water // European Journal of Molecular Biotechnology. 2014. Vol.(6). № 4. pp. 180-209.
Мосин О.В., Игнатов И.И. Феномен клеточной адаптации к тяжелой воде / Мат. VIII Межд. Научно-практической конференции “Теория и практика современной науки”. 26-27 декабря 2012. Москва: Спецкнига. Т. II. С. 28-35.
Мосин О.В., Игнатов И.И. Математические модели воды / XIII Международная конференция “Современные проблемы гуманитарных и естественных наук”. 21–22 декабря 2012. Москва: Спецкнига. Т. 1. С. 47-54, www.tezis.info/1/13.zip.
Ignatov I., Mosin O.V. Isotopic Composition of Water and its Temperature in Modeling of Primordial Hydrosphere Experiments / VIII Int. Conference Perspectives of the Development of Science and Technique, Biochemistry and Biophysics, 2012. V. 15, P. 41-49. www.rusnauka.com/30_NNM_2012/Geographia/3_119057.doc.htm