Формирование кластеров воды
К.х.н. О. В. Мосин
КАК ФОРМИРУЮТСЯ КЛАСТЕРЫ ВОДЫ?
Если совершить краткий экскурс в школьный курс химии мы вспомним, что две электронные пары образуют полярные ковалентные связи между атомами водорода и кислорода, а оставшиеся две электронные пары остаются свободными и называются неподеленными. Молекула воды имеет угловое строение, угол Н–О–Н составляет 104,5 градусов.

Рис. Молекула воды
Поскольку у атома кислорода больше электронов (химики говорят, что атом кислорода более электроотрицательный), чем у атома водорода, электроны двух атомов водорода сдвигаются в сторону более электроотрицательного атома кислорода, приводя к тому, что два положительных заряда атомов водорода компенсируются равным по величине двум атомов водорода отрицательным зарядом атома кислорода. Поэтому электронное облако имеет неоднородную плотность. Около ядер водорода имеется недостаток электронной плотности, а на противоположной стороне молекулы, около ядра кислорода, наблюдается избыток электронной плотности. Это приводит к тому, что молекула воды представляет собой маленький диполь, содержащий положительный и отрицательный заряды на полюсах. Именно такая структура и определяет полярность молекулы воды. Если соединить прямыми линиями эпицентры положительных и отрицательных зарядов получится объемная геометрическая фигура - правильный тетраэдр. Но такой тетраэдр – это только самый первый базовый уровень строения воды.
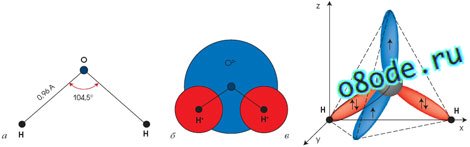
Рис. Структура молекулы воды: а) угловая; б) шаровая; в) тетраэдрическая
Второй уровень химической организации воды определяется возможностью тетраэдров воды образовывать особые связи, названные водородными связями, которые связывают отдельные молекулы друг с другом в ассоциаты.
Водородная связь имеет глобальное значение в химии межмолекулярных взаимодействий и обусловлена в основном слабыми электростатическими силами и воздействиями. Она возникает при взаимодействии обедненного электронами атома водорода одной молекулы воды с неподеленной электронной парой атома кислорода соседней молекулы воды.
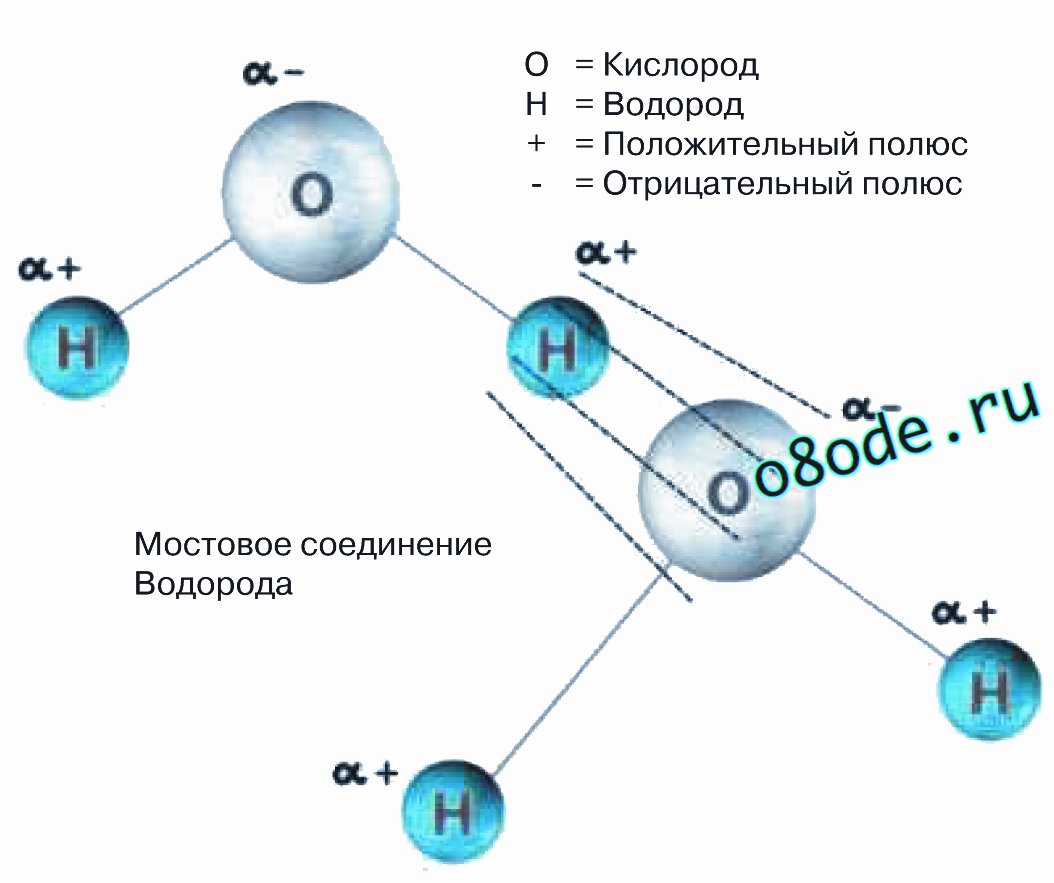
Рис. Образование водородной связи
Водородная связь намного слабее ковалентной связи, тем не менее играет очень важную роль во внутримежмолекулярных взаимодействиях. Водородные связи во многом обусловливают аномальные физические свойства воды. Например, если рассматривать воду как простую совокупность молекул Н2О, то оказывается, что её удельный вес должен составлять 1,84 г/см3, а температура её кипения будет равна 63,5°С. Но, как известно, при нормальной температуре и давлении удельный вес воды равен 1 г/см3, а кипит вода при 100°С. Исходя из этого, следует предположить, что внутри воды должны быть пустоты, где нет молекул Н2О, то есть воде присуща особая структура. Это принципиальное открытие было сделано английским физиком Берналом. С тех пор в этой области проведено множество исследований, но полной ясности в этом вопросе еще нет.
Отличительная черта водородной связи – сравнительно низкая прочность, ее энергия в 5–10 раз ниже, чем энергия химической связи. По энергии она занимает промежуточное положение между химическими связями и Ван-дер-ваальсовыми взаимодействиями, теми, что удерживают молекулы в твердой или жидкой фазе.
Поскольку каждая молекула воды имеет четыре центра образования водородной связи (две неподелённые электронные пары у атома кислорода и два атома водорода), то каждая молекула воды способна образовывать водородные связи с четырьмя молекулами воды, образуя ажурный сетчатый каркас в молекуле льда.
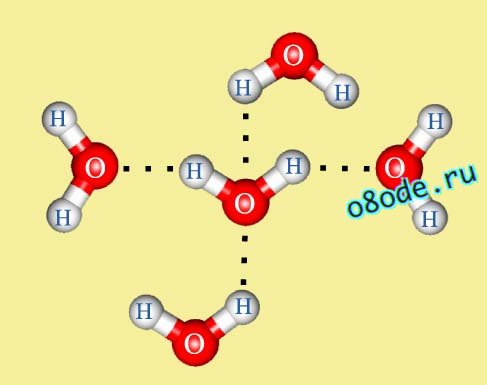
Рис. Каждая молекула воды способна образовывать водородные связи с четырьмя соседними молекулами
В кристаллической структуре льда каждая молекула участвует в 4 водородных связях, направленных к вершинам тетраэдра. В центре этого тетраэдра находится атом кислорода, в двух вершинах — по атому водорода, электроны которых задействованы в образовании ковалентной связи с кислородом. Две оставшиеся вершины занимают пары валентных электронов кислорода, которые не участвуют в образовании внутримолекулярных связей.

Рис. Водородные связи в кристаллической решётке льда
В отличие от льда, в жидкой воде водородные связи легко разрушаются и быстро восстанавливаются, что делает структуру воды исключительно изменчивой. Именно благодаря этим связям в отдельных микрообъемах воды непрерывно возникают своеобразные ассоциаты воды - её структурные элементы. Всё это приводит к неоднородности в структуре воды.
Первым идею о том, что вода неоднородна по своей структуре, высказал Уайтинг в 1884 году. Его авторство цитирует Э.Ф. Фрицман в монографии “Природа воды. Тяжёлая вода”, изданной в 1935 году. После неё появилось множество работ, в которых воду рассматривали как смесь ассоциатов разного состава (“гидролей”).
Когда в 20-е годы определили структуру льда, оказалось, что молекулы воды в кристаллическом состоянии образуют трёхмерную непрерывную сетку, в которой каждая молекула имеет четырёх ближайших соседей, расположенных в вершинах правильного тетраэдра. В 1933 году Дж. Бернал и П. Фаулер предположили, что подобная сетка существует и в жидкой воде. Поскольку вода плотнее льда, они считали, что молекулы в ней расположены не так, как во льду, то есть подобно атомам кремния в минерале тридимите, а так, как атомы кремния в более плотной модификации кремнезёма — кварце. Увеличение плотности воды при нагревании от 0 до 4°C объяснялось присутствием при низкой температуре тридимитовой компоненты. Таким образом, модель Бернала — Фаулера сохранила элемент двухструктурности, но главное их достижение — идея непрерывной тетраэдрической сетки. Тогда появился знаменитый афоризм И. Ленгмюра: „Океан — одна большая молекула“.
Только в 1951 году Дж. Попл создал модель непрерывной сетки, которая была не так конкретна, как модель Бернала — Фаулера. Попл представлял воду как случайную тетраэдрическую сетку, связи между молекулами в которой искривлены и имеют различную длину. Модель Попла объясняет уплотнение воды при плавлении искривлением связей. Когда в 60–70-е годы появились первые определения структуры льдов II и IX, стало ясно, как искривление связей может приводить к уплотнению структуры. Модель Попла не могла объяснить немонотонность зависимости свойств воды от температуры и давления так хорошо, как модели двух состояний. Поэтому идею двух состояний ещё долго разделяли многие учёные.
Рис. Модель непрерывной сетки
Во второй половине XX века помимо „континуальных“ моделей (модель Попла), возникли две группы „смешанных“ моделей: кластерные и клатратные. В первой группе вода представала в виде кластеров из молекул, связанных водородными связями, которые плавали в море молекул, в таких связях не участвующих. Модели второй группы рассматривали воду как непрерывную сетку водородных связей - каркас, которая содержит пустоты; в них размещаются молекулы, не образующие связей с молекулами каркаса.
Среди кластерных моделей наиболее яркой оказалась модель Г. Немети и Х. Шераги, предложенные ими картинки, изображающие кластеры связанных молекул, которые плавают в море несвязанных молекул, вошли во множество монографий.
Другая модель воды, предложенная в 1957 г. Фрэком и Уэном – модель мерцающих кластеров. Эта модель очень близка современным представлениям о структуре воды. В этой модели водородные связи в воде непрерывно образуются и рвутся, причем эти процессы протекают кооперативно в пределах короткоживущих групп молекул воды, названных “мерцающими кластерами”. Их время жизни оценивают в диапазоне от 10-10 до 10-11 с. Такое представление правдоподобно объясняет высокую степень подвижности жидкой воды и ее низкую вязкость. Считается, что благодаря именно таким свойствам вода служит одним из самых универсальных растворителей.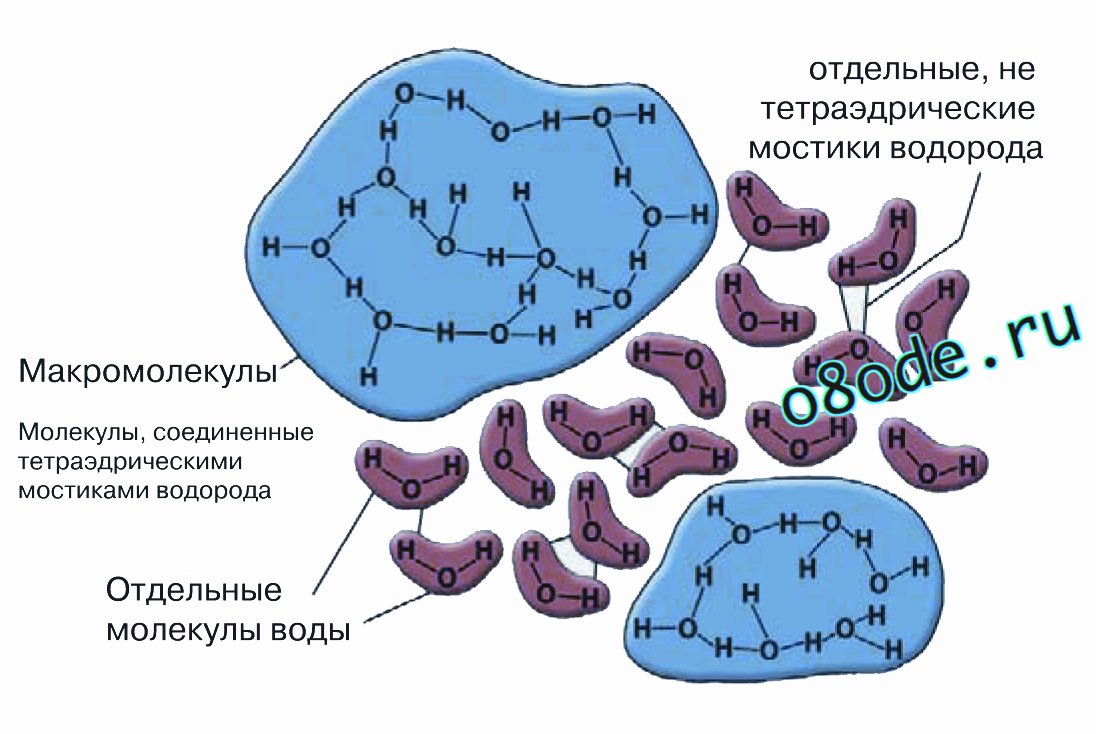
Рис. Модель мерцающих кластеров воды. На рисунке представлены как отдельные кластерно-ассоциативные структуры молекул воды, так и отдельные молекулы воды, не связанные водородными связями.
«Водяные кристаллы» могут иметь самую разную форму, как пространственную, так и двухмерную (в виде кольцевых структур). В основе же всего лежит тетраэдр. Именно такую форму имеет молекула воды. Группируясь, тетраэдры молекул воды образуют разнообразные пространственные и плоскостные структуры. И из всего многообразия структур в природе базовой является гексагональная (шестигранная) структура, когда шесть молекул воды (тетраэдров) объединяются в кольцо. Такой тип структуры характерен для льда, снега и талой воды.

Рис. Кристаллическая структура льда
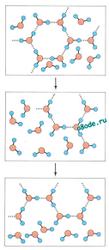
Рис. справа - Структура жидкой воды. В воде кластеры периодически разрушаются и образуются снова. Время перескока составляет 10-12 секунд.
Изучить строение этих образующихся ассоциатов оказалось довольно сложно, поскольку вода – смесь различных полимеров, которые находятся в равновесии между собой.
Сталкиваясь друг с другом, полимеры переходят один в другой, разлагаются и вновь образуются.
Разделить эту смесь на отдельные компоненты тоже практически невозможно.
Лишь в 1993 году группа исследователей из Калифорнийского университета (г. Беркли, США) под руководством доктора Р.Дж.Сайкалли расшифровала строение триммера воды, в 1996 г. – тетрамера и пентамера, а затем и гексамера воды. К этому времени уже было установлено, что жидкая вода состоит из полимерных ассоциатов (кластеров), содержащих от трех до шести молекул воды.
Более сложным оказалось строение гексамера. Самая простая структура – шесть молекул воды в вершинах шестиугольника, – как выяснилось, не столь прочна, как структура клетки.
Более того, структуры призмы, раскрытой книги или лодки тоже оказались менее устойчивыми. В шестиугольнике может быть только шесть водородных связей, а экспериментальные данные говорят о наличии восьми. Это значит, что четыре молекулы воды связаны перекрёстными водородными связями.
Структуры кластеров воды были найдены и теоретически, сегодняшняя вычислительная техника позволяет это сделать. В 1999 г. Станислав Зенин провёл совместно с Б. Полануэром (сейчас в США) исследование воды в ГНИИ генетики, которые дали интереснейшие результаты.
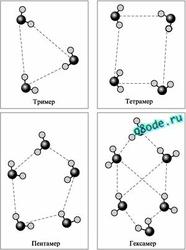
Применив современные методы анализа - рефрактометрию, протонный резонанс и жидкостную хроматографию им удалось обнаружить ассоциаты молекул воды - кластеры.
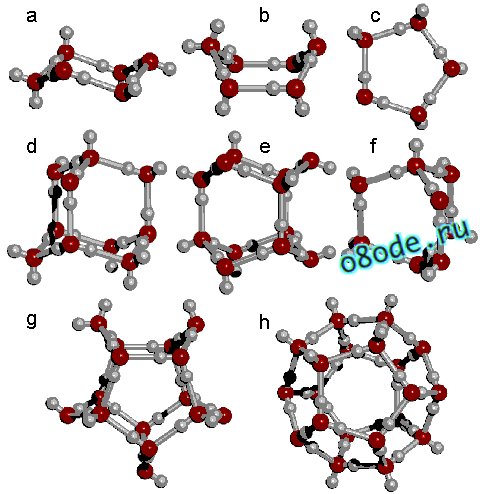
Рис. Возможные кластеры водыРис. Формирование кластера из 20 молекулы воды.
Объединяясь друг с другом, кластеры могут образовывать более сложные структуры:
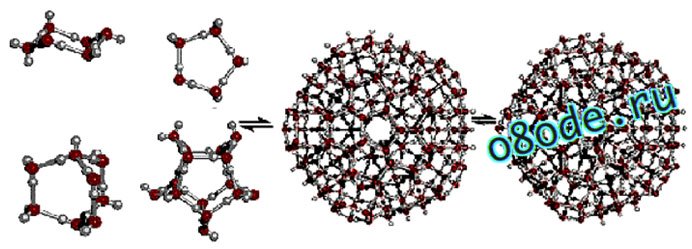
Рис. Более сложные ассоциаты кластеров воды

Анализируя полученные данные С.В. Зенин предложил, что вода представляет собой иерархию правильных объемных структур "ассоциатов" (clathrates), в основе которых лежит кристаллоподобный "квант воды", состоящий из 57 ее молекул, которые взаимодействуют друг с другом за счет свободных водородных связей. При этом 57 молекул воды (квантов), образуют структуру, напоминающую тетраэдр. Тетраэдр в свою очередь состоит из 4 додекаэдров (правильных 12-гранников). 16 квантов образуют структурный элемент, состоящий из 912 молекул воды. Вода на 80% состоит из таких элементов, 15% - кванты-тетраэдры и 3% - классические молекулы Н2О. Таким образом, структура воды связана с так называемыми платоновыми телами (тетраэдр, додекаэдр), форма которых связана с золотой пропорцией. Ядро кислорода также имеет форму платонова тела (тетраэдра).
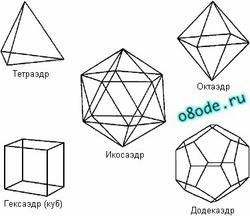
Элементарной ячейкой воды являются тетраэдры, содержащие связанные между собой водородными связями четыре (простой тетраэдр) или пять молекул Н2О (объемно-центрированный тетраэдр).

Рис. Тетраэдр
При этом у каждой из молекул воды в простых тетраэдрах сохраняется способность образовывать водородные связи. За счет их простые тетраэдры могут объединяться между собой вершинами, ребрами или гранями, образуя различные кластеры со сложной структурой, например, в форме додекаэдра.

Рис. Додекаэдр
Таким образом, в воде возникают многочисленные кластеры, которые несут в себе очень большую энергию и информацию крайне высокой плотности. Порядковое число таких структур воды так же высоко, как и порядковое число кристаллов (структура с максимально высоким упорядочением, которую мы только знаем), потому их также называют «жидкими кристаллами» или «кристаллической водой». "Кванты воды" могут взаимодействовать друг с другом за счет свободных водородных связей, торчащих наружу из вершин “кванта” своими гранями. При этом возможно образование уже двух типов структур второго порядка. Их взаимодействие друг с другом приводит к появлению структур высшего порядка. Последние состоят из 912 молекул воды, которые по модели Зенина практически не способны к взаимодействию за счет образования водородных связей. Этим и объясняется, например, высокая текучесть жидкости, состоящей из громадных полимеров. Таким образом, водная среда представляет собой как бы иерархически организованный жидкий кристалл.
Рис. справа - Формирование отдельного кластера воды (компъютерное моделирование)
Изменение положения одного структурного элемента в этом кристалле под действием любого внешнего фактора или изменение ориентации окружающих элементов под влиянием добавляемых веществ обеспечивает, согласно гипотезе Зенина, высокую чувствительность информационной системы воды. Если степень возмущения структурных элементов недостаточна для перестройки всей структуры воды в данном объеме, то после снятия возмущения система через 30-40 мин возвращается в исходное состояние. Если же перекодирование, т. е. переход к другому взаимному расположению структурных элементов воды оказывается энергетически выгодным, то в новом состоянии отражается кодирующее действие вызвавшего эту перестройку вещества [Зенин, 1994]. Такая модель позволяет Зенину объясненить "память воды" и ее информационные свойства [Зенин, 1997].
К.х.н. О. В. Мосин
Cписок литературы:
Г.Г. Маленков. Успехи физической химии, 2001
С.В.Зенин, Б.М. Полануер, Б.В. Тяглов. Экспериментальное доказательство наличия фракций воды. Ж. Гомеопатическая медицина и акупунктура. 1997.№2.С.42-46.
С.В. Зенин, Б.В. Тяглов. Гидрофобная модель структуры ассоциатов молекул воды. Ж.Физ.химии.1994.Т.68.№4.С.636-641.
С.В. Зенин Исследование структуры воды методом протонного магнитного резонанса. Докл.РАН.1993.Т.332.№3.С.328-329.
С.В.Зенин, Б.В.Тяглов. Природа гидрофобного взаимодействия. Возникновение ориентационных полей в водных растворах. Ж.Физ.химии.1994.Т.68.№3.С.500-503.
С.В. Зенин, Б.В. Тяглов, Г.Б.Сергеев, З.А. Шабарова. Исследование внутримолекулярных взаимодействий в нуклеотидамидах методом ЯМР. Материалы 2-й Всесоюзной конф. По динамич. Стереохимии. Одесса.1975.с.53.