Министерство путей сообщения Российской Федерации
Дальневосточный государственный университет путей сообщения
Г.И. Воловник М.И. Коробко
ЭЛЕКТРОХИМИЧЕСКАЯ ОЧИСТКА ВОДЫ
Учебное пособие
Рекомендовано Дальневосточным
региональным учебно-методическим центром
в качестве учебного пособия для студентов вузов региона,
обучающихся по направлениям: 653500 – Строительство;
специальность 290800 – Водоснабжение и водоотведение;
550100 – Строительство, магистерские программы;
550112 – Водоснабжение городов и промышленных предприятий; 550113 – Водоотведение и очистка сточных вод
Хабаровск
Издательство ДВГУПС
2002
Рецензенты:
Кафедра “Гидравлика и водоснабжение” Хабаровского государственного технического университета (доктор технических наук, заведующий кафедрой, профессор М.Н. Шевцов)
Кандидат технических наук, директор Дальневосточного предприятия “Росводоканал” А.Д. Лернер
В пособии приведены сведения о различных способах электрохимической очистки природных и сточных вод, рассмотрены конструкции электрохимических аппаратов, вопросы их эксплуатации.
Учебное пособие предназначено для студентов специальности 2908 “Водоснабжение и водоотведение” всех форм обучения.
СОДЕРЖАНИЕ
ВВЕДЕНИЕ
1. ЭЛЕКТРОЛИЗ
1.1. Общие положения
1.2. Основные параметры процесса
1.3. Конструкция электролизера
1.4. Эксплуатация электролизеров
2. ЭЛЕКТРОФЛОТАЦИЯ
2.1. Общие положения
2.2. Конструкция электрофлотаторов
2.3.Технологический расчет электрофлотатора
2.4. Эксплуатация электрофлотаторов
3. ЭЛЕКТРОКОАГУЛЯЦИЯ
3.1. Основные положения
3.2. Конструкции электрокоагуляторов
3.3. Технологический расчет электрокоагулятора
3.4. Эксплуатация электрокоагуляционных установок
3.5. Применение электрокоагуляции в технологии очистки воды
3.5.1. Электрокоагуляционная обработка природных вод
3.5.2. Электрокоагуляционная обработка сточных вод
4. ДЕСТРУКТИВНЫЯ ЭЛЕКТРОХИМИЧЕСКАЯ ОЧИСТКА
4.1. Общие положения
4.2. Технологические расчеты установок для электрохимической очистки
4.3. Примеры применения деструктивной электрохимической очистки
ЗАКЛЮЧЕНИЕ
СПИСОК ЛИТЕРАТУРЫ
Введение
Электрохимическая обработка – один из видов физико-химической очистки воды. Прохождение постоянного электрического тока через слой воды сопровождается процессами, в результате которых происходит деструкция (разрушение) водных загрязнений, коагуляция коллоидов, флокуляция грубодисперсных примесей и их флотация.
Электрохимическая обработка применима для осветления и обесцвечивания природных вод, для их умягчения, очистки от мышьяка, удаления кремния, фтора, кислорода, для очистки сточных вод, содержащих нефтепродукты, органику, красители, СПАВ, фенол; она позволяет корректировать значения водородного показателя рН и окислительно-восстановительного потенциала Еh, от чего зависит возможность тех или иных химических процессов; повышает ферментивную активность активного ила в аэротенках; уменьшает удельное сопротивление и улучшает условия обезвоживания органических осадков.
Таким образом, электрохимическая обработка достаточно универсальна и может быть альтернативой многих механических, биохимических и химических технологий улучшения качества воды.
Установки электрохимической очистки (электрофлотаторы, электрокоагуляторы, аппараты для электрохимической деструкции и др.) компактны, безотказны, просты в эксплуатации, легко автоматизируются. Их применение наиболее целесообразно для локальной очистки природных, а также бытовых и производственных сточных вод.
1. ЭЛЕКТРОЛИЗ
1.1. Общие положения
Установка для электрохимической обработки воды состоит из блока подготовки воды, электролизера, блока обработки воды после электрохимической очистки (рис. 1.1).
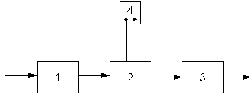
Рис. 1.1. Схема установки для электрохимической обработки воды: 1 – блок подготовки воды; 2 – электролизер; 3 – блок доочистки; 4 –выпрямитель тока
В некоторых случаях предусматривается предварительная механическая очистка, уменьшающая опасность засорения электролизера грубодисперсными примесями с большой гидравлической крупностью, корректировка рН и солевого состава воды. Чаще всего возникает необходимость в предварительном увеличении солесодержания воды с целью уменьшения ее электрического сопротивления.
Блок для последующей очистки необходим, если в результате электрохимической обработки вода насыщается грубодисперсными примесями, например хлопьями гидрооксидов металлов после электрокоагуляции. Основной элемент установки – электролизер, состоящий из электродных ячеек (рис. 1.2).
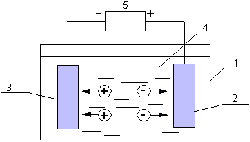
Рис.1.2.Схема электродной ячейки:
1 – корпус; 2 – анод; 3 – катод; 4 – межэлектродное пространство; 5 – источник постоянного тока
Ячейка образована двумя электродами, присоединенными к разным полюсам источника постоянного тока. Межэлектродное пространство заполнено водой, всегда являющейся электролитом, т.е. проводником второго рода.
Перенос электрических зарядов через слой воды – результат электрофореза, т.е. миграции полярных частиц, носителей зарядов, к электродам, имеющим противоположный знак: к аноду перемещаются частицы – носители отрицательного, к катоду – положительного заряда. У электродов полярные частицы теряют заряд, деполяризуются.
В электрофорезе участвуют частицы различной дисперсности, включая и грубодисперсные (эмульгированные частицы, пузырьки газов), но главную роль в переносе электрохимических зарядов играют ионы, обладающие наибольшей подвижностью. К полярным частицам относятся и молекулы воды, что объясняется их особой структурой. Входящий в состав молекулы атом кислорода, имеющий большую электроотрицательность, чем атомы водорода, оттягивает на себя электроны, придает молекуле асимметричность и, как следствие, полярность (рис. 1.3). На электродах происходят основные процессы электролиза, в которых участвуют как молекулы воды, так и полярные частицы из числа водных примесей.
Продуктами электродных реакций являются обезвреженные водные примеси, газообразный водород и кислород, образующиеся при разрушении молекул воды, катионы металлов в случае применения растворимых металлических анодов, молекулярный хлор и др.
Электродную ячейку можно рассматривать в качестве генератора этих продуктов, некоторые из которых, вступая затем в химическое взаимодействие между собой и с водными загрязнениями в межэлектродном пространстве, обеспечивают дополнительную химическую очистку воды. Эти вторичные процессы в отличие от первичных (электродных) называются объемными. Повышение температуры воды при электролизе и увеличение рН при катодном разрушении молекул воды инициируют объемные реакции.
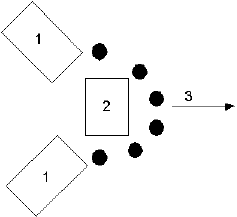
Рис. 1.3. Структура молекулы воды: 1 – атом водорода; 2 – атом кислорода; 3 – электроны
По закону Фарадея теоретическое количество вещества, прореагировавшего на электродах при пропускании постоянного электрического тока, прямо пропорционально его силе и продолжительности процесса:
, (1.1)
где А – электрохимический эквивалент вещества, г/А ч; Icur – сила тока, А; t – продолжительность процесса, ч.
Электрохимический эквивалент элемента определяется по формуле
, (1.2)
где М – атомная масса элемента или соединения, г; z – его валентность.
Значения электрохимических эквивалентов некоторых элементов приведены в табл. 1.1.
Таблица 1.1
Электрохимические эквиваленты некоторых элементов
Элемент
Электрохимический эквивалент вещества А
л/А ч
г/А ч
Водород
0,41
0,0376
Кислород
0,205
0,289
Железо двухвалентное
–
1,042
Железо трехвалентное
–
0,695
Алюминий
–
0,336
Хром трехвалентный
–
0,647
Хром шестивалентный
–
0,324
Медь двухвалентная
–
1,186
Цинк
–
1,22
Хлор
–
1,324
Кальций
–
0,748
Фактическое количество вещества, генерируемого при электролизе, меньше теоретического, рассчитанного по формуле (1.1), так как часть электроэнергии затрачивается на нагревание воды, электродов и на другие нужды. Поэтому при расчетах учитывается коэффициент использования тока h < 1, величина которого определяется экспериментально.
Электродные процессы заключаются в обмене заряженными частицами между электродом и электролитом. Для этого в установившихся стабильных и равновесных условиях необходимо создание электрического потенциала, минимальная величина которого зависит от вида реакции и от температуры воды. При температуре +25 ° С потенциалы называются нормальными (табл. 1.2).
Таблица 1.2
Нормальные электродные потенциалы
Электродная
реакция
Потенциал
[В]
Электродная реакция
Потенциал
[В]
Al ® Al3+ + 3` e
Zn ® Zn2+ + 2` e
1,66
0,763
Cu ® Cu2+ + ` e
4OH-® 2H2O + O2 + 4` e
+ 0,345
+ 0,401
Fe ® Fe2+ + 2` e
Cd ® Cd2+ + 2` e
H2® 2H + 2` e
0,44
0,403
0,00
2H2O ® O2 + 4H+ + 4` e
2Cl- ® Cl2 + 2` e
Cl- + H2O ® HClO + H+ + 2` e
+ 1,23
+ 1,36
+ 1,49
Напряжения, создаваемые в электродной ячейке, должны быть достаточными для возникновения требуемой по условиям обработки электродной реакции и для преодоления влияния различных тормозящих факторов. С этой целью создается перенапряжение на электродах (см. табл. 1.2), влияющее на интенсивность электродного процесса. Необходимое перенапряжение связано с такими условиями, как ионный состав воды, присутствие некоторых примесей, например СПАВ, плотность тока (его сила отнесенная к единице площади электрода) и др.
Перенапряжение характеризует электрохимическую активность материала электрода по отношению к конкретной реакции. При прочих равных условиях задача выбора электродного материала заключается в том, чтобы для прохождения реакции, являющейся основной в соответствующем технологическом процессе, требуемое перенапряжение оказалось минимальным, так как это позволяет снизить затраты электроэнергии.
Некоторые электродные реакции протекают одновременно и взаимно тормозят друг друга, т.е. являются конкурирующими. Рассмотрим в качестве примера условия выделения на нерастворимых анодах ОРТА кислорода и молекулярного хлора, причем регулирование процесса производится за счет изменения напряжений в электродной ячейке. Как следует из табл. 1.2, нормальный потенциал реакции образования молекулярного кислорода составляет + 0,401 в или + 1,23 в; при увеличении напряжения до + 1,36 в (нормальный потенциал реакции образования молекулярного хлора) на аноде будет выделяться только кислород, а при дальнейшем увеличении потенциала – одновременно и кислород, и хлор, причем выделение хлора будет происходить с недостаточной интенсивностью. При напряжении около 4–5 в выделение кислорода практически прекратится, а ячейка будет генерировать только хлор.
1.2. Основные параметры процесса
К основным параметрам электролиза относятся сила и плотность тока, напряжение в пределах электродной ячейки, а так же скорость и продолжительность пребывания воды в межэлектродном пространстве.
Сила тока Icur – величина, определяемая в зависимости от требуемой производительности по генерируемому продукту, А, определяется по формуле
. (1.3)
Формула получена путем преобразования формулы (1.1) с учетом коэффициента использования тока h .
Плотность тока – его сила, отнесенная к единице площади электрода, А/м2, например анода, определяется из выражения
, (1.4)
где Fan – площадь анода, м2.
Плотность тока оказывает определяющее влияние на электролиз: с увеличением плотности тока интенсифицируются электродные процессы и уменьшается требуемая площадь электродов, но одновременно возрастают напряжение в пределах ячейки, энергоемкость процесса [1].
Как следует из рис. 1.4, с увеличением плотности тока усиливается пассивация электродов. Необоснованное увеличением плотности тока интенсифицирует выделение электролизных газов, приводящее иногда к бурлению и измельчению нерастворимых продуктов очистки воды.
Плотность тока должна назначаться минимальной по условиям устойчивого протекания требуемого технологического процесса. При больших производительностях следует учитывать также технико-экономические показатели, связанные с ограничением площади электродов.
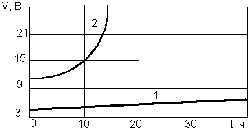
Рис. 1.4. Графики изменения напряжений в процессе эксплуатации: 1 – для i аn=20 А/м2; 2 – для i аn=100 А/м2
Напряжение в электродной ячейке, В, определяется по формуле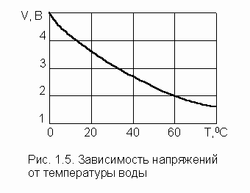
, (1.5)
где i an – плотность тока, А/м2; D – расстояние между электродами (ширина межэлектродного канала), м; c R– удельная электропроводность воды, 1/(Ом м); Кг – коэффициент газонаполнения межэлектродного пространства, Кг = 1,05–1,2.
Формула не учитывает электрических сопротивлений электрода в связи с малостью, но при пассивации эти сопротивления оказываются значительными. Ширина межэлектродного канала принимается минимальной (3–20 мм) по условиям незасорения.
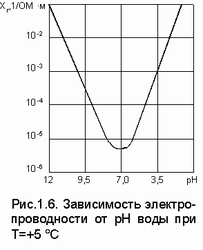
Удельная электропроводность воды зависит от ряда факторов, среди которых наиболее существенны температура, рН, ионный состав и концентрация ионов. С увеличением температуры электропроводность увеличивается, а напряжение уменьшается (рис. 1.5) [1]. Минимальное значение электропроводности при рН = 7. В процессе электролиза происходит повышение температуры и рН воды. Если первоначально рН > 7, то можно ожидать уменьшения c R, а при первоначальных значениях рН < 7 электропроводность возрастает (рис. 1.6) [2].
Удельная электропроводность природных вод средней минерализации менее 0,001–0,005 1/(Ом м), городских сточных вод 10–0,01 1/(Ом м). Удельная электропроводность при электролизе принимается более 0,1–1,0 1/(Ом м).
В том случае, если исходная вода имеет недостаточную электропроводность, следует увеличить солесодержание (рис. 1.7) [2]. Обычно для этого используют поваренную соль NaCl, дозы которой определяются экспериментально и чаще всего составляют 500–1500 мг/л (8–25 мг-экв/л).
Поваренная соль не только удобна по условиям применения (хранение, приготовление раствора и т.д.), но в ее присутствии замедляется пассивация электродов.
Пассивация заключается в блокировании электродов поверхностными отложениями, что увеличивает электрические сопротивления в электродных ячейках и тормозит электродные реакции.
Аноды пассивируются в результате образования на их поверхностях тонких и малозаметных окисных пленок, при сорбции на анодах кислорода и других компонентов, которые, в свою очередь, сорбируют частицы водных примесей. На катодах образуются карбонатные отложения, особенно в случае обработки воды с повышенной жесткостью [1].
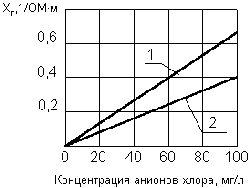
Рис. 1.7. Зависимость электропроводности от концентрации анионов хлора : 1 - при Т= +25 0С; при Т= +5 0С
Диссоциируясь, поваренная соль насыщает воду анионами хлора и катионами натрия. Хлор-ионы имеют небольшие размеры и проникая через пассивирующие отложения к поверхности анода разрушают эти отложения. В присутствии других анионов, особенно SO42-, депассивирующее влияние хлор-инов уменьшается. Считается, что устойчивая работа электролизера возможна в случае, если хлор-ионы составляют не менее 30 % от общего количества анионов. Катионы натрия в результате электрофореза перемещаются к катодам, на которых генерируются гидроксид-ионы ОН-, и, взаимодействуя с последними, образуют едкий натрий, растворяющий карбонатные отложения на катодах.
Потребляемая мощность, Вт, электролизера определяется по зависимости
, (1.6)
где h э – коэффициент полезного действия электролизера, h э = 0,7–0,8; Vэ – напряжение на электролизере, в.
Размерности силы тока – А, напряжения – В.
Продолжительность пребывания воды в межэлектродном пространстве ограничивается временем, необходимым для генерации нужного количества продуктов электролиза, а также продолжительностью соответствующих объемных реакций, и определяется экспериментально.
Скорость движения воды в межэлектродных каналах назначается с учетом условий выноса из электролизера продуктов электролиза и других примесей; кроме того, от скорости зависит турбулентное перемешивание, что влияет на ход объемных реакций. Как и продолжительность, скорость выбирается на основании экспериментов.
1.3. Конструкция электролизера
Электролизеры (при электрокоагуляции – электрокоагуляторы) представляют собой камеры различных конфигураций, в которых размещены электроды. Камеры футируются листовым винипластом или текстолитом для защиты от воздействия хлора, его кислородных соединений и других окислителей.
Электролиз сопровождается выделением пены и электролизер оборудуется устройствами для ее удаления.
В целях защиты электродных каналов от засорения пеной и нерастворимыми продуктами электролиза предусматриваются устройства для очистки межэлектродного пространства путем продувки сжатым воздухом или при помощи специальных диэлектрических щеток. Щетки предназначаются и для механической депассивации электродов. Одна из таких конструкций приведена в [3]. Электроды имеют форму круглых пластин с центральным отверстием, через которое проходит вал с жестко закрепленными на нем скребками (щетками), заведенными в межэлектродные зазоры. При повороте вала межэлектродные каналы очищаются от отложений.
Если вода содержит грубодисперсные примеси с большой гидравлической крупностью, предусматривается иловая камера для накопления выпадающих осадков (рис.1.8).
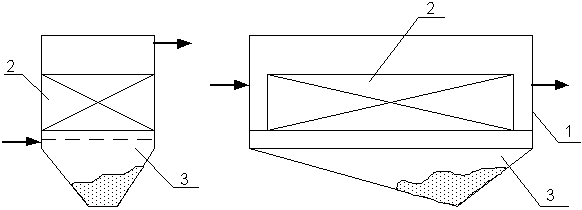
Рис. 1.8. Схемы электролизеров с осадконакопителями: 1 – корпус; 2 – блок электродов; 3 – осадконакопитель
В зависимости от направления движения воды электролизеры бывают горизонтального или вертикального типов (рис. 1.9). Вертикальная установка занимает меньшую площадь, но имеет большую высоту, что усложняет высотную схему сооружения.

Рис. 1.9. Схемы электродных камер: а – горизонтальная прямоугольная;
б – вертикальная прямоугольная или круглая; в – то же с горизонтальным расположением электродов; 1 – корпус; 2 – электроды; 3 – распределительная решетка; 4 – шина электропитания; 5 – анод; 6 – катод в виде сетки
Электроды выполняются в виде стрежней, дисков, сеток и т.д., чаще всего представляют собой пластины толщиной от 3 до 10 мм. Во избежание коробления их размеры ограничены (не более 1,5–1,8 м). Пластины собираются в пакеты при помощи диэлектрических стягивающих шпилек либо устанавливаются в пазы специальных рам из диэлектриков (рис.1.10, 1.11).
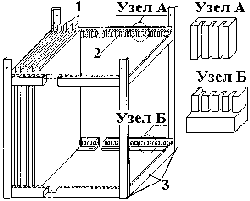
Рис. 1.10. Схема электродной системы пазного типа. 1 – электроды; 2 – пазы;
3 – рама
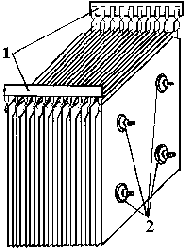
Рис. 1.11. Схема электродной системы пакетного типа:
1 – токораспределительные пластины;
2 – стягивающие шпильки
По условиям монтажа и ремонтопригодности вес пластин или пакетов пластин – не более 50–100 кг. Поэтому при необходимости в корпусе электролизера может размещаться несколько пакетов пластин.
Электроды присоединяются к источнику электропитания по монополярной или по биполярной схеме (рис. 1.12).
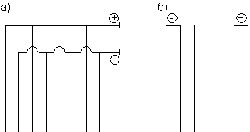
Рис.1.12. Схемы соединения электродов: а – монополярная; б – биполярная
В последнем случае каждый электрод работает одной поверхностью как анод, а другой – как катод. Биполярная схема требует меньшего количества присоединений электродов к источнику питания, но при этом увеличивается напряжение на электролизере. Если при монополярном присоединении оно равно напряжению в пределах одной электродной ячейки, т.е. Vэ = Vя, то при биполярной
Vэ = n Vя, (1.7)
где n – количество ячеек, шт.
Ограничения Vэ30–50 в связаны с условиями эксплуатации. Материал электрода должен обладать рядом обязательных свойств: химической устойчивостью и инертностью к среде, в которой производится электролиз; благоприятными электрохимическими характеристиками по отношению к тем реакциям, которые должны осуществляться в электролизере; механической прочностью и долговечностью. Как указывалось, одним из основных показателей электрохимической активности электродного материала к данной реакции является перенапряжение. Для одной и той же реакции, но при разном материале электрода, перенапряжение оказывается различным. С уменьшением перенапряжения уменьшаются и затраты электроэнергии.
Аноды (за исключением установок для электрокоагуляции) не должны растворяться при электролизе. Нерастворимые аноды выполняются титановыми с защитными покрытиями из платины, оксидов свинца, оксидов кобальта (ОКТА), диоксида марганца (ТДМА), оксидов рутения и титана (ОРТА). Возможно применение анодов из графита или графитизированного угля, но эти материалы недостаточно прочны и долговечны. В электрокоагуляторах аноды выполняются растворимыми из алюминия и его сплавов, а также из железа.
В процессе электролиза всегда генерируется водород и кислород. Смесь этих газов взрывоопасна, а смесь водорода с воздухом обладает взрывоопасностью при концентрации водорода более 4 % по объему. По условиям безопасности электролизеры оборудуются системами вытяжной вентиляции (вытяжные зонты, бортовые отсосы и др.), обеспечивающими разбавление выделяющегося водорода воздухом до концентрации менее 0,4 %, т.е. в 10 раз ниже порога взрывоопасности.
Производительность вентиляции для электролизеров непрерывного действия, м3/ч,
, (1.8)
где Т – температура обрабатываемой воды, ° С.
Если электролизер периодического действия, то
, (1.9)
где Wel – полезная вместимость электродной камеры, м3; t – продолжительность обработки, ч.
В случаях, когда применяется открытый электролизер и генерируемый водород поступает непосредственно в помещение, кратность воздухообмена, 1/ч, в последнем должна быть не менее
, (1.10)
где W – объем помещения, м3.
Электролиз всегда сопровождается выделением тепла и нагревом обрабатываемой воды, что может повлиять на условия ее последующего использования или выпуска в систему водоотведения.
Расход выделяющегося тепла, кДж/ч, равен
, (1.11)
где D V – напряжение разложения поваренной соли. При i an = 200 А/м2, D V = 2,1 В.
Соответствующее повышение температуры воды, 0С
, (1.12)
где С – теплоемкость воды объемная, кДж/(л град.); qw – расчетный расход воды, м3/ч.
Источник:
edu.dvgups.ru/METDOC/ITS/GIDRA/V_O_S_V/METOD/KOROBKO/UP.HTM