Вода и жизнь
К.х.н. О. В. Мосин, май 2010 года
ВОДА И ЖИЗНЬ

Кроме того, вода имеет множество аномальных свойств, без которых невозможно зарождение жизни. Именно поэтому в воде зародилась жизнь. За последние десятилетия учёные, используя самые разные виды энергии в водной среде, получили в лабораторных условиях самые разнообразные "органические" вещества. В этих опытах моделировались условия первичной бескислородной атмосферы древней Земли, в которой происходил синтез "органических" молекул из неорганических за счет энергии коротковолнового ультрафиолетового излучения Солнца, энергии электрических разрядов молний или за счет других геотермальных источников энергии.
Первые эксперименты по неорганическому синтезу "органических" веществ в условиях первобытной Земли, осуществил С. Миллер. Для этого он использовал очень простой прибор - колбу, в которой создаются электрические разряды. Прибор заполнялся водой и смесью газов - водородом, метаном и аммиаком, которые присутствовали в избытке в атмосфере древней Земли; свободный кислород в колбу не допускался. В верхней части колбы непрерывно создавались сильные электрические разряды. Внизу нагревалась до кипения вода, обеспечивая циркуляцию пара и воды. В ходе экперимента из метана, аммиака и водорода синтезировались органические соединения – альдегиды и аминокислоты.
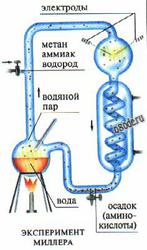
Рис. Эксперимент Миллера, в котором под действием искрового разряда из водорода, метана, воды и аммиака в отсутствии кислорода образуются органические соединения.
Эксперименты Миллера вызвали большой интерес среди учёных всего мира. К сходным опытам приступили мировые многие, среди них американцы [3, 28, 29, 31], немцы [19] и наши соотечественники [27].
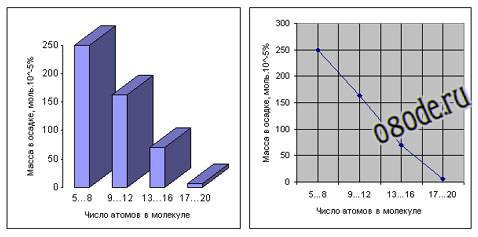
Рис. Распределение соединений, полученных в опытах Миллера, по массе и сложности (диаграммы построены по данным С. Миллера).
В 1960 году Уилсон [43], добавив в исходный раствор серу, получил более крупные молекулы полимеров в виде плёнок размером 1 см., содержащие по 20 и более атомов углерода (см. фото). Они представляли собой поверхностно-активные вещества, сконцентрированные на поверхности раздела газ - жидкость в виде тонких пленок. Катализатором образования полимерных пленок служила сера, широко распространённая в то время в форме зерен сульфидов (например, в пиритовых песках). По-видимому, эти пленки молекул, синтезировавшихся на границе между разными фазами, играли важную роль на ранних стадиях возникновения жизни.

Фото. Плоские плёнки органических макромолекул, образующихся при искровых разрядах в смеси аммиака, сероводорода, паров воды и золы пекарских дрожжей (Из книги М. Руттен “Происхождение жизни, ред. А. И. Опарина, Москва, Мир, 1973”).
В условиях восстановительной атмосферы малые "органические" молекулы могли также синтезироваться и за счет энергии ультрафиолетового излучения Солнца. Однако условия на Земле в эпоху примитивной атмосферы были для зарождения жизни довольно жёсткими. Хотя первые органические молекулы в бескислородной атмосфере не подвергались окислению, ничто не защищало их от губительного воздействия жесткого ультрафиолетового излучения. Поэтому в этот период молекулярной эволюции могли использоваться и другие источники энергии. Например, свободные радикалы и малые "органические" молекулы могли создаваться за счет высокоэнергетического ультрафиолетового излучения Солнца, а для синтеза из малых молекул других, более сложных соединений могли служить и менее мощные источники энергии.
Поннамперума и сотр. [31] проводили эксперименты, аналогичные экспериментам Миллера, но с использованием в качестве источника энергии ультрафиолетового света. Хотя по теоретическим соображениям синтезы, идущие под действием ультрафиолета, не должны принципиально отличаться от тех, которые вызываются электрическим разрядом, важно было получить экспериментальное подтверждение этого факта. Ведь в условиях первичной атмосферы гораздо больше энергии поступало с ультрафиолетовым излучением.
При обработке водной реакционной смеси водорода, аммиака и метана ультрафиолетом синтезировались не только аминокислоты и пурины, т. е. строительные блоки белков и нуклеиновых кислот, но и, используя особые условия, также синтезировались из этих блоков полимеры. Оказалось, что в присутствии цианистого водорода аминокислоты полимеризуются, образуя небольшие пептидные цепи. Причём при добавлении фосфорной кислоты формировались различные нуклеотиды [31, 33-36, 39]. Позже было доказано, что более крупные "органические" молекулы можно синтезировать и без помощи ультрафиолета, просто нагревая реакционную смесь [28, 29]. Так, в растворах формальдегида с гидроксиламином, формальдегида с гидразином и в растворах, содержащих цианистый водород, в конце опыта были обнаружены аминокислоты. В других экспериментах эти продукты полимеризовались в пептидные цепи – важный шаг к неорганическому синтезу белка. В системе с раствором цианистого водорода в водном аммиаке даже появлялись более сложные соединения - пурины и пиримидины (азотистые основания, входящие в состав нуклеиновых кислот) (см. рис. ниже).

Рис. Предполагаемый механизм образования пуринов из водной смеси аммиака и цианистого водорода: промежуточные продукты - 4-аминоимидазол-5-карбокоамидин (АИКАМ) и 4-аминоимидазол-5-карбоксамид (АИКА)-были найдены в растворе (Из книги М. Руттен “Происхождение жизни, ред. А. И. Опарина, Москва, Мир, 1973”).
Эти эксперименты указали возможный путь перехода от синтеза малых "органических" молекул за счет энергии ультрафиолетового солнечного излучения Солнца к более сложным "органическим" молекулам, образующимся при менее жестких воздействиях.
Совершенно другим путем в попытках синтезировать неорганическим путем большие молекулы белков пошёл американский учёный Фокс [8, 9, 15]. Как известно, молекулы протеинов построены из одной или нескольких полипептидных цепей, а те в свою очередь состоят из большого числа разных аминокислот. После того как образовались аминокислоты, может произойти следующий важный этап - их конденсация в полипептидные цепи. Выделение молекулы воды, сопровождающее реакцию конденсации двух молекул аминокислот - факт большой важности. Поскольку реакция поликонденсации сопровождается дегидратацией, скорость превращения будут выше при удалении воды из системы. Это соображение привело исследователей к выводу, что раннее развитие жизни должно было происходить вблизи действующих вулканов, поскольку в ранние периоды геологической истории вулканическая деятельность шла более активно, чем в последующие времена.
Дегидратация сопровождает не только полимеризацию аминокислот, но и объединение других строительных блоков в более крупные "органические" молекулы. Такое объединение всегда связано с реакцией конденсации, при которой от одного блока "отщепляется" атом водорода, а от другого - гидроксильная группа.
Первым возможность проведения реакций конденсации-дегидратации в условиях "первичного бульона" доказал американский учёный Кальвин. Дело в том, что из всех соединений лишь синильная кислота способна связывать молекулы воды "первичного бульона". Присутствие в "первичном бульоне" синильной кислоты доказана уже первыми экспериментами Миллера.
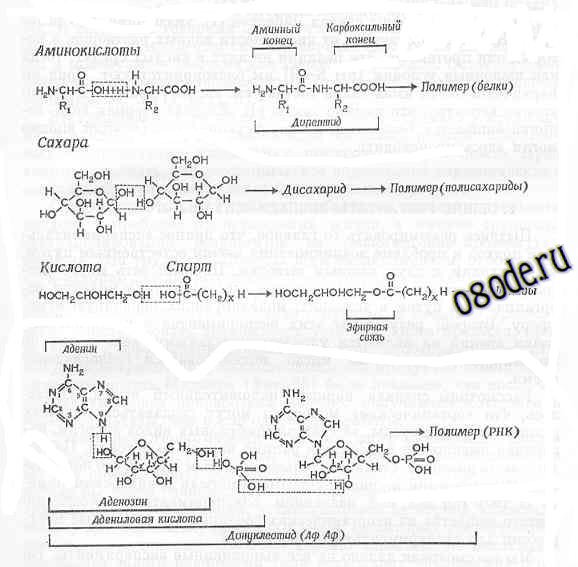
Рис. Реакции конденсации с дегидратацией, приводящие к образованию из отдельных строительных блоков более крупных "органических" молекул (Из книги М. Руттен “Происхождение жизни, ред. А. И. Опарина, Москва, Мир, 1973”).
Верхние три уравнения: конденсация и последующая полимеризация аминокислот и в белки, сахаров в полисахариды и кислот и спиртов в липиды. Нижнее уравнение - конденсация аденина с рибозой и фосфорной кислотой, в результате чего образуется нуклеотид. Полимеризация нуклеотидов в цепь нуклеиновой кислоты также представляет собой реакцию конденсации и протекает с выделением молекул воды.
В последствии оказалось, что два других, несколько более сложных соединения - цианамид и дицианамид HN(C = N)2 - обладают ещё большей дегидратирующей способностью. Реакции с ними более сложны, их механизм еще не выяснен окончательно [22]. В присутствии синильной кислоты и цианамидов конденсация отдельных блоков, сопровождаемая дегидратацией, может идти при нормальных температурах в сильно разбавленных водных растворах [24].
Интересные выводы сделал Эйбелсон [1], установивший, что реакции с синильной кислотой сильно зависят от кислотности водных растворов, в которых они протекают. Эти реакции не идут в кислых средах, тогда как щелочные условия (рН 8-9) им благоприятствуют. Учёные до сих пор спорят мог ли первичный океан имел такой состав, но вполне вероятно, что именно таким рН обладала вода, соприкасавшаяся с базальтом, и эти реакции вполне могли происходить при контакте с базальтовыми породами.
Исследователи провели эксперименты, в которых безводную смесь аминокислот подвергали воздействию температур до 170 С. Оказалось, что наилучшие результаты по поликонденсации получаются со смесями, содержащими аспарагиновую и глутаминовую кислоты. Почему это так, до сих пор непонятно. Важно, что именно эти две аминокислоты относятся к числу важнейших аминокислот, встречающихся в современных организмах. Интересно, что при этом образовывались соединения, названные протеиноидами, сходные с природными белками. Они состояли из крупных молекул с молекулярной массой до 300000, сложенных из тех же блоков, что и природный белок и содержали 18 из 23 аминокислот, обычно встречающихся у современных организмов. С природным белком они сходны и по ряду других важных свойств, например по связыванию полинуклеотидов [41], по пригодности в пищу бактериям и крысам, по способности вызывать реакции, сходные с теми, которые катализируются ферментами в организмах. Например, эти искусственно синтезированные "органические" соединения способны каталитически разлагать глюкозу. Активность их, правда, мала, но, как указывается в сообщении об этом [14], "...первым белкам достаточно было проявлять хотя бы слабую активность". Кроме того, эти вещества могут оказывать действие, аналогичное действию меланоцитстимулирующего гормона [16].
Другое важное свойство протеиноидных соединений - их гетерогенность. Это значит, что последовательность аминокислот в их пептидных цепях не совершенно случайна, а, напротив, более или менее закономерна. Но в то время было невозможно провести строгое сравнение этих искусственных соединений с природными белками, так как молекулы белков настолько сложны, что структура большинства из них еще не определена с достаточной точностью. Стремясь подчеркнуть сходство этих искусственных белковоподобных соединений с природными белками, Фокс назвал их протеиноидами. Поскольку они были синтезированы под действием тепла, в дальнейшем их стали называть "термическими протеиноидами".
Способность протеиноидов к выполнению жизненно-важных функций, сходных с функциями молекул живых организмов, выражается в том, что они могут в присутствии гидрата окиси цинка расщеплять нуклеотид АТФ, т. е. обладают элементарной ферментативной активностью.
В последствие было показано, что протеиноиды могут образовывать особые сферические микросферы, аналоги клеточных мембран - коорцерваты. Искусственные микросферы получают, промывая горячую смесь искусственных полимеров водой или водными растворами солей. Микросферы очень малы, их диаметр - около 2 мкм. Морфологические особенности микросфер показаны на фото ниже.
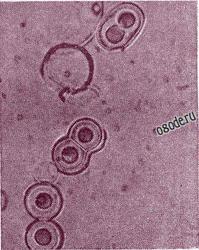
Фото. Протеноидные микросферы, сдвоенные при увеличении рН среды (Из книги М. Руттен “Происхождение жизни, ред. А. И. Опарина, Москва, Мир, 1973”).
В водных растворах микросферы довольно стабильны. Если их помещают в растворы иной концентрации, чем концентрация раствора, в котором они образовались, то можно наблюдать их реакцию. В слишком концентрированных растворах они сморщиваются, в разбавленных набухают, т. е. их реакция на изменение осмотического давления сходна с реакцией живых клеток. Видимо, это объясняется наличием у них полупроницаемой наружной оболочки, сходной с мембраной, которая может быть и двойной.
Образование микросфер из термических протеиноидов важно потому, что оно дает исследователям материал для суждения о том, как мог произойти следующий шаг в развитии жизни. Это шаг от разрозненных "органических" молекул к группам таких молекул, собранным в отдельные структуры и отделенным от окружающего мира своеобразной примитивной мембраной – коорцерватам, что было продемонстрировано нашим соотечественником А.И. Опариным. Так, начиная синтезом первых аминокислот и нуклеотидов, через образование кооцерватов происходила эволюция жизни. Такой синтез возможен наряду с другими, при воздействии на смесь воды, аммиака и метана электрических разрядов, ультрафиолетового излучения и высокой температуры. Затем происходила поликопденсация полученных аминокислот при температуре 170 или 65 С (в присутствии некоторых фосфатов) в протеиноиды. При воздействии на смесь протеиноидов воды или кислых водных растворов (дожди) образовывались микросферы - коорцерваты.
В настоящее время имеются много экспериментальных данных получения "органических" молекул неорганическим путем в условиях, моделирующих первичную атмосферу. Но, результаты этих экспериментов с геологической точки зрения не являются удовлетворительными, поскольку довольно трудно моделировать геологическое прошлое. Для появления первых древнейших форм жизни естественным путем существенно важны два условия. Во-первых, атмосфера должна быть бескислородной, во-вторых, должно иметься все необходимое для построения "органических" молекул - атомы углерода, азота, неорганические катализаторы, вода и т. д. При выполнении этих условий начинается образование "органических" соединений. Но это означает, что формирование жизни - процесс, свойственный не только нашей Земле. В принципе, на любой планете, отвечающей двум вышеизложенным требованиям, находится она в нашей Солнечной или в любой другой системе, могут идти аналогичные процессы. Ведь бескислородная атмосфера, содержащая нужные для синтеза "органических" соединений атомы и молекулы, - обычное для Вселенной явление. Остается одно главное условие для образования жизни - наличие воды.
Многие вопросы происхождения жизни остаются открытыми до сих пор, например, изотопный состав первичного бульона. Дело в том, что в условиях первичной атмосферы и гидросферы в условиях геотермальной активности и искровых разрядах в водной среде могли образовываться и накапливаться незначительные количества тяжёлой воды.
Учёные считают, что гравитационное поле Земли – недостаточно сильно для удержания водорода, и наша планета постепенно теряет водород в результате его диссоциации в межпланетное пространство. Водород улетучивается быстрее тяжелого дейтерия. Поэтому в течение геологического времени должно происходить накопление дейтерия в атмосфере и в поверхностных водах. Тяжёлая вода улетучивается медленнее, чем обычная вода, а конденсируется быстрее.
На нашей планете осуществляется гигантский испарительно-конденсационный процесс разделения воды и обогащения её из туч и облаков, в то время как тяжёлая вода накапливается в закрытых водоёмах.
Можно предположить, что в те времена в условиях безкислородной атмосферы в условиях сильного ультрафиолетового излучения и интенсивной вулканической деятельности, происходило интенсивное накопление тяжёлой воды в гидросфере и синтез первых органических соединений происходил в её присутствии. Связи С-D более стабильны чем связи С-Н. По теории абсолютных скоростей разрыв С-Н-связей может происходить быстрее, чем C-D-связей, подвижность дейтерия D+ меньше, чем подвижность протия Н+, константа ионизации тяжёлой воды в 5 раз меньше константы ионизации обычной воды. Всё это может наложить отпечаток на кинетику химико-ферментативных реакций в условиях зарождения жизни и молекулярной эволюции (О. В. Мосин).
Вода – это самое загадочное вещество на планете Земля. Способность молекул воды образовывать за счёт водородных связей ассоциативные структуры в виде колец и цепочек позволяет видеть аналогию структуры воды со структурой ДНК.
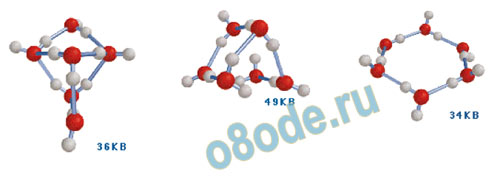
Рис. Варианты кластеров воды, состоящих из 6 молекул.
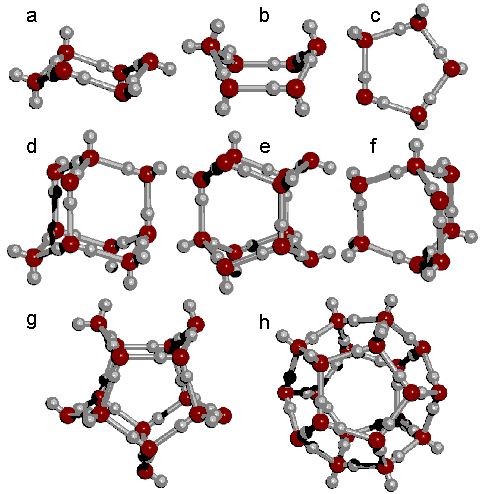
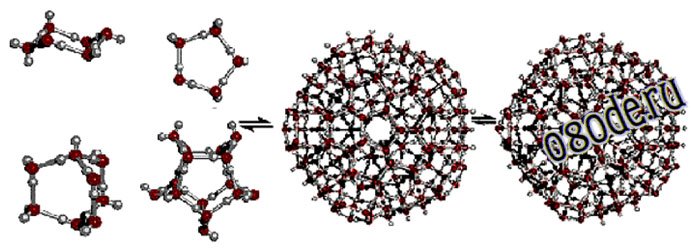
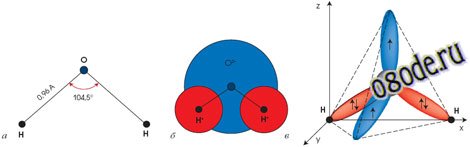
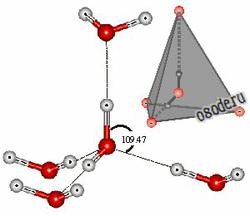
Рис. Тетраэдр воды из пяти молекул воды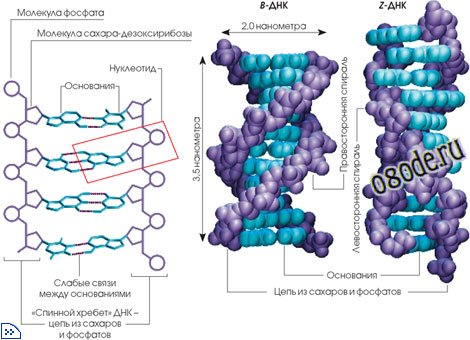
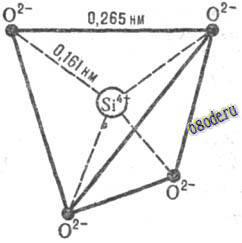
Рис. Элементарный кремне-кислородный тетраэдр SiO44-.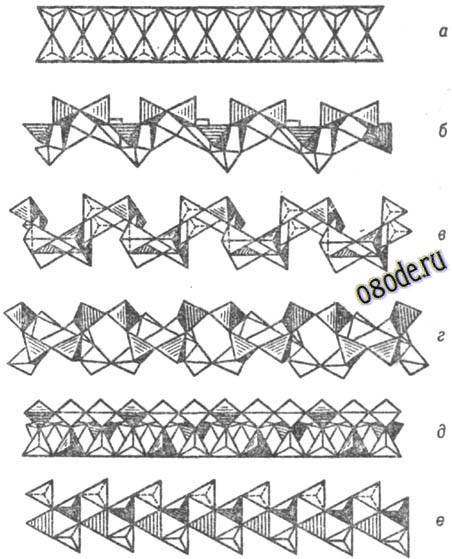

Рис. Более сложные ассоциаты воды
Объединяясь друг с другом, кластеры могут образовывать более сложные структуры:
Рис. Более сложные ассоциаты кластеров воды
Еще первооткрыватели водородных связей Дж. Бернал и Р. Фаулер в 1932 г. сравнивали структуру жидкой воды с кристаллической структурой кварца, а те ассоциаты - это в основном тетрамеры 4Н20, в которых четыре молекулы воды соединены в компактный тетраэдр с двенадцатью внутренними водородными связями. В результате образуется четырёхгранная пирамида - тетраэдр.
Рис. Структура молекулы воды: а) угловая; б) шаровая; в) тетраэдрическая
«Водяные кристаллы» могут иметь самую разную форму, как пространственную, так и двухмерную (в виде кольцевых структур). В основе же всего лежит тетраэдр. Именно такую форму имеет молекула воды. Группируясь, тетраэдры молекул воды образуют разнообразные пространственные и плоскостные структуры. И из всего многообразия структур в природе базовой является гексагональная (шестигранная) структура, когда шесть молекул воды (тетраэдров) объединяются в кольцо. Такой тип структуры характерен для льда, снега и талой воды.
Кандидат геолого-минералогических наук Ю. А. Колясников выдвинул гипотезу спиральной воды, т.е. структуры, напоминающей структуру молекулы носителя информации - ДНК.
Рис. Строение молекулы носителя информации – дезоксирибонуклеиновой кислоты (ДНК)
По Ю. А. Колясникову, водородные связи в тетрамерах воды могут образовывать как правотак и левовинтовую последовательности, подобно тому, как кристаллы кварца (Si02), тоже имеющие тетраэдрическую структуру, бывают правои лево-вращательной кристаллической форм. Поскольку каждый такой тетрамер воды имеет еще и четыре незадействованные внешние водородные связи (как у одной молекулы воды), то тетрамеры могут соединяться этими внешними связями в своего рода полимерные цепочки, наподобие молекулы ДНК. А поскольку внешних связей всего четыре, а внутренних - в 3 раза больше, то это позволяет тяжелым и прочным тетрамерам в жидкой воде изгибать, поворачивать и даже надламывать эти ослабленные тепловыми колебаниями внешние водородные связи. Это и обуславливает текучесть воды.
Такую структуру вода, по мнению Ю. А. Колясникова, имеет только в жидком состоянии и, возможно, частично в парообразном. А вот во льду, кристаллическая структура, которого хорошо изучена, тетрагидроли соединены между собой негибкими равнопрочными прямыми водородными связями в ажурный каркас с большими пустотами в нем, что делает плотность льда меньше плотности воды.

Рис. Важнейшие типы кремнекислородных цепочечных анионных группировок (по Белову): а-метагерманатная, б - пироксеновая, в - батиситовая, г-волластонитовая, д-власовитовая, е-мелилитовая, ж-родонитовая, з-пироксмангитовая, и-метафосфатная, к-фторобериллатная, л - барилитовая.
Рис. Важнейшие типы ленточных кремнекислородных группировок (по Белову): а - силлиманитовая, амфиболовая, ксонотлитовая; б-эпидидимитовая; в-ортоклазовая; г-нарсарсукитовая; д-фенакитовая призматическая; е-эвклазовая
Такая тетраэдрально-винтовая структура воды может быть обусловлена ее древней реологической связью с кварцем и другими кремнекислородными минералами, преобладающими в земной коре, из недр которой когда-то появилась вода на Земле. Как маленький кристаллик соли заставляет окружающий его раствор кристаллизоваться в подобные ему кристаллы, так и кварц заставил молекулы воды выстраиваться в тетраэдрические структуры, которые, энергетически наиболее выгодны.
Более подробно читайте об этом в статье к.х.н. О. В. Мосина “Вода и ДНК” /article2268voda_i_dnk.htm
Рис. Компьютерное моделирование кластеров воды (С. Зенин)
Другой главный вопрос эволюции жизни – структура самой воды, участвующей в образовании жизни. Как показал известный болгарский исследователь воды доктор И. Игнатов, в процессе зарождения и эволюции живой материи молекулы воды, клетки и ткани обмениваются между собой биофизическими полями (Игнатов, 1998). В зависимости от энергетических состояний живые организмы могут или получать энергию от окружающей среды (режим «отдачи»), или наоборот терять ее (режим «отнятия») (Игнатов, Антонов, Гылыбова, 1998). По мнению доктора И. Игнатова в этих двух режимах «отдачи» и «отнятия» происходит перераспределение молекул воды по энергиям. При этом максимальный период сохраняемой водой информации – 4 месяца. Таким образом, передача биологической информации может осуществляться за счет «памяти» воды.
Более подробно читайте статью доктора И. Игнатова «Память» воды и зарождение живой материи. Биорезонансные эффекты www.medicalbiophysics.dir.bg/ru/water_memory.html
К.х.н. О.В. Мосин
Литературные источники
1. Abelson Ph. Я., Chemical events on the"primitive earth,"Proc. Natl. Acad. Sci. U. S., 55, 1365-1372 (1966).
2. Bernal J. D., The Origin of Life, Weidenfeld and Nicolson, London, 345, 1967 Джон Бериал, Возникновение жизни, изд-во "Мир", М., 1969).
3. Calvin. М., Chemical evolution, Proc. Roy. Soc. (London), Ser. A, 288, 441-466 (1965).
4. Calvin M., Chemical Evolution, Clarendon, Oxford, 278 pp., 1969 (М. Кальвин, Химическая эволюция, изд-во "Мир", М., 1971).
5. Craford В., Jr., Chemical analysis by infrared, Sci. Am., 189, 8 pp. (1953).
6. Eck R. V., Lipincott E. R., Dayhoff M. O., Pratt Y. T.t Thermodynamic equilibrium and the inorganic origin of organic compounds, Science, 153,628-633 (1966).
7. Eglinton G., Calvin M., Chemical fossils, Sci. Am., 216 (1), 32-43 (1967).
8. Fox S. W., A theory of macromolecular and cellular origins, Nature, 205, 328-340 (1965).
9. Fox S. W., Simulated natural experiments in spontaneous organization of morphological units from proteinoid. In: S. W. Fox (Editor), The Origins of Prebiological Systems, Academic Press, New York, N. Y., pp. 361-373, 1965 (Происхождение предбиологических систем, изд-во "Мир",М., 1966).
10. Fox S, Experiments suggesting evolution to protein. In: V. Bryson and H. J. Vogel (Editors), Evolving Genes and Proteins, Academic Press, New York, N. Y., 359-70, 1965.
11. Fox S., Self-assembly of the protocell from a self-ordered polymer, J. Sci. Ind. Res., 27, 267-274 (1968).
12. Fox S. W., A new view of the "synthesis of life", Quart. J. Florida Acad. Sci., 31, 1-15 (1968).
13. Fox S. W., Spontaneous generation, the origin of life and self assembly, Currents Modern Biol., 2, 235-240 (1968).
14. Fox S. W., Krampitz G., Catalytic decomposition of glucose in aqueous solution by thermal proteinoids, Nature, 203, 1362-1364 (1964).
15. Fox S. W., WaehneldtT. F., The thermal synthesis of neutral and basic proteinoids, Biochim. Biophys. Acta, 160, 246-249 1968).
16. Fox S. W., Wang С. Т., Mclanocytestimulating hormone: Activity in thermal polymers of alpha-ammo acids, Science, 160, 547-548 (1968).
17. Fruton J. S., Simmonds L., General Biochemistry, 2nd ed., Wiley, New York, N. Y., 1077 pp., 1958.
18. Gray G. W., Electrophoresis, Sci. Am., 185, 11 (1951).
19. Groth W., von Weyssenhoff H., Photochemische Bildung organischer Verbindungen aus Mischungen einfacher Gase, Ann. Ehys., 4, 69-77 (1959).
20. Haggis G. H. (Editor), Molecular Biology, Wiley, New York, N. Y.,401, 1964.
21. Harada I., Fox S. W., Thermal synthesis of natural ammo-acids from a postulated primitive terrestrial atmosphere, Nature, 201, 335-336 (1964).
22. Huntress W. Т., Jr., В aldesch wieler J. Z., Ponnamperuma C., Ion-molecule reactions in hydrogen cyanide, Nature, 223, 468-471 (1969).
23. Keller R. A., Gas chromatography, Sci. Am., 205, 11 (1961).
24. Mathews C. N., Moser R., Peptide synthesis from hydrogen-cyanide and water, Nature, 215, 1230-1234 (1968).
25. Miller S. L., Formation of Organic Compounds on the Primitive Earth. In: Опарин А. И. (ред.), The Origin of Life on Earth, Pergamon, London, 123-135, 1959
26. Meister, Biochemistry of the Ammo Acids, 2nd ed., Academic Press,New York, N. Y., 1, 119, 1965 (перевод 1-го издания: А. Майстер, Биохимия аминокислот, ИЛ, М., 1961).
27. Опарин А. И., Пути начального формирования обмена веществ и искусственное моделирование этого формирования в коацерватных каплях. In: S. W. Fox (Editor), Origins of Prebiological Systems, Academic Press, New York, N. Y., 331-341, 1965 (Происхождение предбиологических систем, изд-во "Мир", стр. 335, М., 1966).
28. Оro, Investigation of organo-chemical evolution. In: G. Marnikunian and М. Н. Briggs (Editors), Current Aspects of Exobiology, Pergamon,London, 13-76, 1965.
29. Оrо J., Prebiological organic systems. In: S. W. Fox (Editor), The Origin of Prebiological Systems, Academic Press, New York, N. Y., 137-162, 1965 (Происхождение предбиологических систем, изд-во "Мир", стр. 144, М., 1966).
30. Pauling L., College Chemistry, 3rd ed.,Freeman, San Francisco, Calif., 832 pp., 1964.
31. Ponnamperuma C., Abiological synthesis of some nucleic acid constituents. In: S. W. Fox (Editor), The Origin of Prebiological Systems, Academic Press, New York, N. Y., 221-236, 1965 Происхождение предбиологических систем, изд-во "Мир", стр. 224, М., 1966)
32. Ponnamperuma С., Gabel N., Prebiological synthesis of organic compounds. In: A. Renbaum and R. F. Landell (Editors), Chemistry in Space Research, 1969.
33. Ponnamperuma C., Mack R., Nucleotide synthesis under possible primitive earth conditions, Science, 148, 1221-1223 (1965).
34. Ponnamperuma C., Peterson E., Peptide synthesis from amino acids in aqueous solution, Science, 147, 1572-1573 (1965).
35. Rabinowitz J. S., Chang S., Ponnamperuma C., Phosphorylation of inorganic phosphate as a potential prebiotic process, Nature, 218, 442-443(1968).
36. Schwartz A., Ponnamperuma C., Phosphorylation of adenosine with linear polyphosphate salts in aqueous solution, Nature, 218, 443 (1968).
37. Stein W., Moore S., Chromatography, Sci. Am., 184, 9 pp. (1951).
38. Steinman G., Sequence generation in prebiological peptide systems, Arch. Biochem. Biophys,, 121, 533-539 (1967).
39. Steinman G., Smith A. E., Silver J., Synthesis of a sulfur-containing amino acid under simulated prebiotic conditions, Science, 159, 1108-1109(1968).
40. Supina W. R., Henley R. S., Gas chromatography-snooper par excellence,Chemistry, 37, 12-17 (1964).
41. Waehneldt T, V., Fox S. W., The binding of basic proteinolds with organismic or thermally synthesized polynucleotides, Biochem. Biophys. Acta,160, 239-245 (1968).
42. Willard Н. Я., Merrit L. L., Dean J. A., Instrumental methods of analysis, 3rd ed., Van Nostrand, Princeton, N. J., 626 pp., 1958.
43. Wilson А. Т., Synthesis of macromoleculcs, Nature, 188, 1007-1009(1960).
44. Young R. S., Ponnamperuma C., Early evolution of life, B. S. C. S. Pamphlets, Heath, Boston, 11, 29, 1964.
45. О.В. Мосин, Д.А. Складнев, В.И. Швец. Биотехнология, 2001.