К.х.н. О. В. Мосин
ЭЛЕКТРОМАГНИТНОЕ ПОЛЕ И ОПРЕСНЕНИЕ ВОДЫ
(часть 1 - начало дискуссии)
Продолжение - смотрите следующие статьи этого раздела
Опреснение воды - способ её обработки с целью снижения концентрации растворённых солей до 1 г/л, при которой вода становится пригодной для питьевых и хозяйственных целей. Во всём мире находится в эксплуатации около 1000 крупных стационарных опреснительных установок суммарной производительностью около 1,8 млн. м3/сут пресной воды. Наиболее крупные из них имеют производительность 160 тыс. м3/сут,

В каждой кубической миле морской воды содержится 1,5 -1011 кг растворенных твердых веществ. Океан столь огромен, что если концентрация какого-либо вещества в морской воде составляет всего 1 миллиардную долю по весу, то его содержание в мировом океане исчисляется в 5-109 кг. Тем не менее океан еще мало используется как источник сырьевых материалов, поскольку стоимость извлечения необходимых веществ из воды слишком высока. Лишь три вещества получают из морской воды в промышленно широких масштабах: хлорид натрия, бром и магний. Но наиболее ценной составной частью морской воды является пресная вода. Нехватка пресной воды все больше ощущается даже в таких странах, как Соединенные Штаты, где с ежегодным уровнем осадков дело обстоит совсем неплохо. Во многих областях Соединенных Штатов потребность в пресной воде для бытовых нужд, сельского хозяйства и промышленности превышает ее имеющиеся запасы. В таких странах, как Израиль или Кувейт, где уровень осадков очень низок, запасы пресной воды совершенно не соответствуют потребностям в ней, которые; возрастают в связи с модернизацией хозяйства и приростом населения. В конце концов все человечество окажется перед необходимостью рассматривать океаны как источник воды.
Под соленостью морской воды понимают массу (в граммах) сухих солей в 1 кг морской воды. В пределах мирового океана соленость колеблется от 33 до 37, в среднем ее можно считать равной 35. Это означает, что в морской воде содержится приблизительно 3,5% растворенных солей. Перечень элементов, содержащихся в морской воде, очень велик, однако концентрация большинства из них очень низка. В таблице 1 указаны 11 ионных частиц, присутствующих в морской воде в концентрациях, превышающих 0,001 г/кг, т.е. 1 миллионную долю (млн. д.) по весу. Среди веществ, содержащихся в морской воде в несколько меньших, концентрациях (от 1 млн. д. до 0,01 млн. д.), имеются элементы азот, литий, рубидий, фосфор, йод, железо, цинк и молибден. В морской воде обнаружено не менее 50 других элементов в еще более низких концентрациях.
ТАБЛИЦА 1. Ионные вещества, содержащиеся в морской воде в концентрации выше 0,001 г/кг (1 млн.д.) по весу
- Ионное вещество Содержание, г/кг морской; Концентрация, моль/л
- воды
- Хлорид-ион С1-; 19,35; 0,55;
- Ион натрия Na +; 10,76; 0,47;
- Сульфат-ион SoiS2-; 2,71; 0,028;
- Ион магния Mg2+; 1,29; 0,054;
- Ион кальция Са2+; 0,412; 0,010;
- Ион калия К +; 0,40; 0,010;
- Диоксид углерода; 0,106; 2,3 10-3;
- Бромид-ион Вr-; 0,067; 8,3 10-4;
- Борная кислота; ; ;
- Н3ВО3; 0,027; 4,3 10 -4;
- Ион стронция Sr2+; 0,0079; 9,1 10-5;
- Фторид-ион F-; 0,001; 7 10-5;
Высокая концентрация солей делает морскую воду непригодной для питья и для большинства других целей. В Соединенных Штатах содержание солей в водопроводной воде, согласно требованиям органов здравоохранения, не превышает 0,05%. Это намного меньше по сравнению с их 3,5%-ным содержанием в нормальной морской воде или по сравнению с 0,5%-ным или около того содержанием в солоноватых подземных водах. Снижение содержания солей в морской воде или солоноватых водах до уровня, при котором вода становится пригодной к использованию, называется опреснением воды.
Существует множество способов опреснения воды, и на основе любого из них могут быть построены большие производственные предприятия. Проблема заключается в том, чтобы проводить опреснение с минимальной затратой энергии и минимальными расходами на оборудование. Это требование важно потому, что нация, которая вынуждена в большей мере полагаться на опресненную воду, должна выдерживать экономическую конкуренцию с другими нациями, располагающими более обильными и дешевыми источниками пресной воды. Такая небольшая страна, как Кувейт, расположенная на берегу Персидского залива и почти не располагающая природными источниками пресной воды, может позволить себе роскошь зависеть от опресненной воды только потому, что она извлекает большие доходы от продажи нефти.
Опреснением морской воды люди занимаются несколько столетий. За это время разработаны десятки промышленных технологий опреснения, основанных на физико-химических процессах парообразования, замораживания, диализа, ионного обмена и обратного осмоса. Важнейшей из них является дистилляция воды под воздействием тепла. В разных странах мира действуют более 800 крупных дистилляционных опреснительных установок общей мощностью более 7 млн. м3 в сутки.
Опреснение воды может быть осуществлено как с изменением агрегатного состояния воды (дистилляция, замораживание), так и без изменения её агрегатного состояния (электродиализ, гиперфильтрация, или обратный осмос, ионный обмен, экстракция воды органическими растворителями, экстракция воды в виде кристаллизационной воды кристаллогидратов, нагрев воды до определённой температуры, сорбция ионов на пористых электродах, биологический метод - с использованием способности некоторых водорослей поглощать соли на свету и отдавать их в темноте и др.). В соответствии со способами Опреснение воды существуют различные типы ОУ. Дистилляционные ОУ (однокорпусные и многокорпусные, по способу опреснения - парокомпрессионные и солнечные) применяются при опреснении морской воды и солёных вод. Опреснение воды электродиализом и гиперфильтрацией (обратным осмосом) экономично при солесодержании 2,5-10 г/л, ионным обменом - менее 2,5 г/л. Из всего объёма получаемой в мире опреснённой воды 96% приходится на долю дистилляционных ОУ, 2,9% - электродиализных, 1% - гиперфильтрационных и 0,1% - на долю замораживающих и ионообменных ОУ. В зависимости от производительности ОУ состоит из одного или нескольких включенных параллельно опреснителей.
Существуют следующие методы опреснения морской воды:
ОПРЕСНЕНИЕ ПУТЕМ ДИСТИЛЛЯЦИИ (ПЕРЕГОНКИ)
Воду можно отделить от растворенных в ней солей дистилляцией (перегонкой). Этот процесс основан на том принципе, что вода представляет собой летучее вещество, а соли являются нелетучими веществами. Принцип дистилляции довольно прост, но с его промышленным использованием связано много проблем. Например, по мере выпаривания пресной воды из сосуда, в котором находится морская вода, раствор соли становится все более концентрированным, и в конце концов соль осаждается. Это приводит к образованию накипи, что в свою очередь ухудшает теплопроводность стенок сосуда, засоряет трубы и т.п. Напрашивается такое решение этой проблемы, при котором морскую воду после дистилляции из нее некоторого количества пресной воды необходимо сбрасывать, а вместо нее набирать новую порцию морской воды. Но это следует делать аккуратно, чтобы не потерять весь запас тепла, накопленный в нагретой морской воде, и чтобы не пришлось подводить дополнительное тепло к вновь набираемой холодной морской воде. Потери тепла связаны с тепловым загрязнением окружающей среды и удорожанием процесса. Следует также учесть, что, если дистилляцию проводить при атмосферном давлении, воду надо нагревать до 100°С; при более низком давлении температура кипения воды понижается, и, следовательно, дистилляция требует меньших тепловых затрат.
Одна из наиболее успешных попыток обойти ряд таких трудностей привела к разработке процесса многостадийной флеш-дистилляции, который схематически изображен на рисунке ниже. В камеру А поступает подогретая морская вода, которая называется рассолом. Рассол прокачивают под давлением через витки теплообменника в камеру В, затем в камеру С и, наконец, в камеру D, причем в каждой камере его температура становится все выше. Теплота поступает к рассолу от водяного пара, конденсирующегося на витках теплообменника каждой камеры. Сконденсировавшийся пар, являющийся пресной водой, собирают и откачивают из установки. В камере Е разогретый рассол нагревают еще сильнее паром, который пропускают через витки теплообменника; пар, используемый в этой камере, приносит с собой большую часть полной энергии, вводимой в систему. Из камеры Е горячий рассол поступает в камеру D, где поддерживается пониженное давление. Поскольку давление в этой камере понижено, часть рассола испаряется и после конденсации превращается в пресную воду. Для испарения воды требуется энергия. Когда вода испаряется с поверхности нашего тела, происходит охлаждение этой поверхности. Точно так же остающийся после испарения некоторой части воды рассол тоже охлаждается. Затем он поступает в камеру С, где давление еще ниже, чем в камере D. Здесь происходит испарение еще некоторого количества воды, а оставшийся рассол еще больше охлаждается. На каждой последующей стадии рассол становится все более концентрированным и все более охлаждается. На последней стадии часть рассола, который содержит теперь приблизительно 7% солей по весу, смешивается с вновь поступающей морской водой. Другая часть рассола сбрасывается в море, чтобы предотвратить слишком большое повышение концентрации солей.

Рис. Схема процесса многостадийной флеш-дистилляции для опреснения воды.
На следующем рисунке показана большая промышленная установка по опреснению морской воды методом многостадийной флеш-дистилляции. Такая установка способна вырабатывать ежедневно около 9 миллионов литров пресной воды. Эффективность работы установки многостадийной флеш-дистилляции ограничена главным образом возникновением накипи в системе циркуляции горячего рассола. Главными причинами образования накипи являются карбонат кальция и гидроксид магния. Чтобы воспрепятствовать их образованию и тем самым сделать возможной эксплуатацию системы при более высоких температурах, применяются различные добавки. Однако при высоких температурах возникает проблема, связанная с осаждением сульфата кальция.

Рис. Установка для опреснения воды методом многостадийной флеш-дистилляции. Такая установка может ежедневно вырабатывать приблизительно 9 миллионов литров пресной воды (компания «Аква-Кем» в г. Милуоки, США). Рисунок из книги Т. Брауна “Химия в центре наук”, М, Мир, 1983.
Современные дистилляционные опреснители бывают одноступенчатые, многоступенчатые с трубчатыми нагревательными элементами, или испарителями, многоступенчатые с мгновенным вскипанием и парокомпрессионные. Многоступенчатый испаритель состоит из ряда последовательно работающих испарительных камер с трубчатыми нагревательными элементами. Нагреваемая солёная вода движется внутри трубок нагревательного элемента, греющий пар конденсируется на внешней их поверхности. Нагрев и испарение воды в первой ступени осуществляются паром котла, работающего на дистилляте; греющим паром следующей ступеней служит вторичный пар предыдущей испарительной камеры. В опреснителях с мгновенным вскипанием солёная вода проходит последовательно, от последнего к первому, через конденсаторы, встроенные в испарительные камеры, нагреваясь за счёт тепла конденсации, поступает в головной подогреватель, нагревается выше температуры кипения воды в первой испарительной камере, где вскипает. Затем пар конденсируется на поверхности трубок конденсатора, а конденсат стекает в поддон и насосом откачивается потребителю. Неиспарившаяся вода перетекает через гидрозатвор в следующую камеру с более низким давлением, где она снова вскипает, и т.д. Расход тепла на получение 1 кг пресной воды в одноступенчатом дистилляционном опреснителе составляет около 2400 кдж; рекуперация тепла фазового перехода в многоступенчатом опреснителе позволяет снизить расход тепла на 1 кг пресной воды до 250-300 кдж.
Основная часть затрат при осуществлении любого варианта процесса дистилляции связана с большими потребностями в тепловой энергии. Для типичной установки многостадийной флеш-дистилляции стоимость пара составляет приблизительно 40% от стоимости получаемой пресной воды. В связи с этим предложено множество других способов опреснения воды, которые не связаны с необходимостью ее испарения. В одном из способов пресную воду удаляют из морской воды путем ее замораживания. При образовании льда из морской воды растворенные в ней соли не попадают в него. Однако, процесс замораживания тоже требует затрат энергии. В настоящее время проводятся испытания крупномасштабных установок по опреснению воды, в которых используется принцип замораживания.
ОПРЕСНЕНИЕ ВОДЫ МЕТОДОМ ОБРАТНОГО ОСМОСА
При опреснении воды методом обратного осмоса пресную воду отделяют от растворенных в ней солей при помощи мембраны, проницаемой для воды, но непроницаемой для солей. Для этого необходимо наличие селективной мембраны, пропускающей только воду, но задерживающей растворенные в ней вещества. Такие мембраны изготавливаются из различных материалов, например, полиамида или ацетат целлюлозы и выпускаются в виде полых волокон или рулонного типа. Через микроскопически малые поры этих мембран может практически проникать только чистая вода и растворенные в ней газы, в то время как соль, микроорганизмы, органические соединения и т.д. в основном задерживаются мембраной. Эффект опреснения и связанная с ним производительность по опресненной воде зависит от различных факторов, прежде всего от общего солесодержания сырой воды, а также солевого состава, давления и температуры.
Если поместить такую мембрану между рассолом и пресной водой, тенденция к выравниванию концентраций по обе стороны мембраны заставит воду проникать через мембрану в рассол. Этому процессу можно воспрепятствовать, прикладывая давление со стороны рассола. При достаточно большом давлении проникновение воды через мембрану в рассол прекратится. Давление, необходимое, чтобы воспрепятствовать просачиванию воды через мембрану в раствор, называется осмотическим. Для морской воды при нормальных условиях осмотическое давление составляет приблизительно 25 атм.
Если прикладываемое к рассолу давление превысит осмотическое, то вода будет проходить через мембрану в обратном направлении, другими словами, пресная вода будет выдавливаться из рассола через мембрану. Этот процесс, называемый обратным осмосом, схематически показан на рис. Морскую или солоноватую воду накачивают под высоким давлением в камеры, стенки которых изготовлены из полупроницаемых мембран. При прохождении воды через мембраны локальная концентрация солей у стенки мембраны повышается, что приводит к повышению осмотического давления и уменьшению потока пресной воды. Чтобы воспрепятствовать этому, через камеру нужно непрерывно прокачивать морскую воду. Поток пресной воды через мембрану пропорционален прикладываемому давлению. Но максимальное давление, которое можно приложить к мембране, определяется ее собственными характеристиками. При слишком высоком давлении мембрана может разорваться, забиться присутствующими в воде примесями или пропускать слишком большое количество растворенных солей.
Эффект опреснения и связанная с ним производительность по опресненной воде зависит от различных факторов, прежде всего от общего солесодержания сырой воды, а также солевого состава, давления и температуры.

Рис. Схема процесса опреснения воды методом обратного осмоса. Давление, создаваемое насосом высокого давления, превышает осмотическое давление соленой воды относительно пресной. Благодаря этому пресная вода просачивается через полупроницаемую мембрану. Чтобы предотвратить накопление соли вблизи мембраны, насос должен постоянно прокачивать по трубам соленую воду. На практике трубы должны иметь очень малый диаметр, и поэтому установку приходится изготовлять из многих тысяч труб.
В обычных установках по опреснению воды методом обратного осмоса трубы, изображенные на рисунке выше, изготавливают из пористого вещества, выложенного с внутренней стороны очень тонкой пленкой из ацетата целлюлозы. Ацетат целлюлозы (из которого изготовляют целлофан и основу фотографической пленки) играет роль полупроницаемой мембраны. Установка состоит из множества таких труб, уложенных параллельно друг другу. Скорость проникновения воды через мембрану довольно невелика. Например, при опреснении соленой воды из скважины, содержащей 0,5% растворенных солей, при давлении 50 атм в течение суток удается получить приблизительно 700 л пресной воды с каждого квадратного метра мембраны. Поскольку для получения большой площади поверхности необходимо очень много тонких труб, процесс обратного осмоса пока еще не используется для получения больших количеств пресной воды. Однако этот процесс представляется многообещающим, если будут разработаны улучшенные мембраны, в особенности для опреснения соленой воды из скважин. Эта вода имеет более низкую концентрацию растворенных солей по сравнению с морской водой, что позволяет проводить ее опреснение при более низких давлениях.
ОПРЕСНЕНИЕ ВОДЫ МЕТОДОМ ЭЛЕКТРОМАГНИТЕОГО ПОЛЯ
Другой принципиально отличный от традиционных методов опреснения морской воды методом электромагнитного поля предложил изобретатель В. М. Рофман (paragraf207.com/Perelik/Soveti/4.html). Он предложил создать специальную генерируемую сильными электромагнитными полями ячейку, где вода движется в ламинарном режиме со скоростью до 2,5 м/с и на неё воздействуют точно подобранные соотношения величин трансформирующих магнитных и ориентирующих электрических сил. В таких условиях по мнению В. М. Рофмана будет происходить изменение формы молекулы воды из угловой в линейную.Рис. Более сложные ассоциаты кластеров
По расчётам изобретателя, для превращения 1 моля воды из угловой формы молекулы в линейную необходим электромагнит с напряженностью магнитного поля 4,6 107 А/м и величиной магнитной индукции 58 Тл. Такие условия генерации магнитного поля являются очень жесткими. На сегодняшний день они находятся на самом пределе достигнутого технологией уровня управления электромагнитными взаимодействиями в сверхпроводящих магнитах. Однако, как считает изобретатель уже сегодня имеются надёжные перспективы усовершенствования этой технологии на базе достижении физики высокотемпературной сверхпроводимости.
Такая необычная вода должна кипеть не при +100 С, а при минус 80 С. Это позволило бы использовать в технологическом процессе дистилляции тепловую энергию самой морской воды и рассеянное тепло окружающей среды. С другой стороны конденсация пара в дистиллят пресной воды, при снятии магнитного воздействия с диполей её молекул, происходит за счёт обратного самопроизвольного образования водородных связей при температуре окружающей среды, что исключает какие-либо дополнительные энергетические затраты при проведении этих технологических операций.
Сегодня из-за высоких энергетических затрат стоимость получения пресной воды на лучших дистилляционных установках составляет $2,3 на 1 м3. Повышенная энергоёмкость процесса опреснения связана с тем, что вода обладает рядом аномальных физико-химических свойств – высокими значениями температуры кипения (+100 С), удельной теплоёмкости (1 кал/г.град при 15 С) и скрытой теплоты парообразования (586 кал/г при 20 С).
Эти физико-химические аномалии обусловлены строением её молекулы. Известно, что молекулы воды имеют очень простую химическую/физическую структуру - стороны угла двух атомов водорода находятся по отношению к атому кислорода под углом 104,7°. Молекула воды представляет собой маленький диполь, содержащий положительный и отрицательный заряды на полюсах. Именно такая структура и определяет полярность молекулы воды. Если соединить прямыми линиями эпицентры положительных и отрицательных зарядов получится объемная геометрическая фигура - правильный тетраэдр.

Рис. Структура молекулы воды: а) угловая; б) шаровая; в) тетраэдрическая
Из восьми электронов, составляющих внешний слой атома кислорода в молекуле воды, две электронные пары образуют ковалентные связи О – Н, а остальные четыре электрона представляют собой две неподелённые электронные пары. По этой причине в молекуле воды имеется четыре полюса электрических зарядов – два положительных и два отрицательных. Атом кислорода в молекуле воды находится в состоянии sp2-гибридизации. Поэтому валентный угол НОН (104,3°) близок к тетраэдрическому (109,5°). Электроны, образующие связи О—Н, смещены к более электроотрицательному атому кислорода. В результате атомы водорода приобретают эффективные положительные заряды, поскольку на них создаются два положительных полюса. Центры отрицательных зарядов неподеленных электронных пар атома кислорода, находящиеся на гибридных - орбиталях, смещены относительно ядра атома и в свою очередь создают два отрицательных полюса.
Молекула воды имеет угловое строение; входящие в ее состав ядра образуют равнобедренный треугольник, в основании которого находятся два протона, а в вершине — ядро атома кислорода, Межъядерные расстояния О—Н близки к 0,1 нм, расстояние между ядрами атомов водорода равно 0,15 нм. Из восьми электронов, составляющих внешний электронный слой атома кислорода в молекуле воды две электронные пары образуют ковалентные связи О—Н, а остальные четыре электрона представляют собой две неподеленных электронных пары.
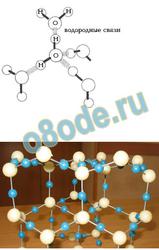
Благодаря наличию водородных связей каждая молекула воды образует водородную связь с 4-мя соседними молекулами, образуя ажурный сетчатый каркас в молекуле льда. Однако, в жидком состоянии вода – неупорядоченная жидкость; эти водородные связи - спонтанные, короткоживущие, быстро рвутся и образуются вновь. Всё это приводит к неоднородности в структуре воды.
Рис. В кристалле льда (внизу) каждая молекула воды образует водородную связь с 4-мя соседними молекулами, образуя ажурный сетчатый каркас (вверху)
То, что вода неоднородна по своему составу, было установлено давно. С давних пор известно, что лёд плавает на поверхности воды, то есть плотность кристаллического льда меньше, чем плотность жидкости. Почти у всех остальных веществ кристалл плотнее жидкой фазы. К тому же и после плавления при повышении температуры плотность воды продолжает увеличиваться и достигает максимума при 4°C. Менее известна аномалия сжимаемости воды: при нагреве от точки плавления вплоть до 40°C она уменьшается, а потом увеличивается. Теплоёмкость воды тоже зависит от температуры немонотонно. Кроме того, при температуре ниже 30°C с увеличением давления от атмосферного до 0,2 ГПа вязкость воды уменьшается, а коэффициент самодиффузии - параметр, который определяет скорость перемещения молекул воды относительно друг друга растёт. Для других жидкостей зависимость обратная, и почти нигде не бывает, чтобы какой-то важный параметр вёл себя не монотонно, т.е. сначала рос, а после прохождения критического значения температуры или давления уменьшался. Возникло предположение, что на самом деле вода — это не единая жидкость, а смесь компонентов-ассоциатов, которые различаются свойствами, например плотностью и вязкостью, а следовательно, и структурой. Такие идеи стали возникать в конце XIX века, когда накопилось много данных об аномалиях воды.
Сейчас существует большое количество различных теорий и моделей, объясняющих структуру и свойства воды. Общим у них является представление о водородных связях как основном факторе, определяющем образование структурированных ассоциатов. Вода – это кооперативная система, в ней существуют цепные образования водородных связей. При этом всякое воздействие на воду распространяется эстафетным путем на тысячи межатомных расстояний..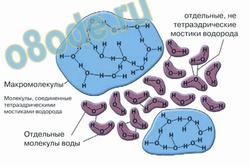
Рис. Современная клатратно-фрактальная модель воды. На рисунке представлены как отдельные кластерно-ассоциативные структуры молекул воды, так и отдельные молекулы воды, не связанные водородными связями.
Сейчас наукой доказано, что особенности физических свойств воды и многочисленные короткоживущие водородные связи между соседними атомами водорода и кислорода в молекуле воды создают благоприятные возможности для образования особых структур-ассоциатов (кластеров), воспринимающих, хранящих и передающих самую различную информацию.
Согласно расчётам, отдельный кластер воды состоит из 57 молекул воды и взаимодействует с другими кластерами за счет свободных водородных связей. Это приводит к появлению структур второго порядка в виде шестигранников, состоящих из 912 молекул воды. При этом свойства кластеров зависят от того, в каком соотношении выступают на поверхность кислород и водород. Конфигурация элементов воды реагирует на любое внешнее воздействие и примеси, что объясняет чрезвычайно лабильный характер их взаимодействия. В обычной воде совокупность отдельных молекул воды и случайных ассоциатов составляет 60% (деструктурированная вода), а 40% - это кластеры (структурированная вода).

Рис. Отдельный кластер воды
Структурной единицей такой воды является кластер, состоящий из отдельных молекул воды, природа которых обусловлена дальними кулоновскими силами. В структуре кластеров закодирована информация о взаимодействиях, имевших место с данными молекулами воды. В водных кластерах за счёт взаимодействия между ковалентными и водородными связями между атомами кислорода и атомами водорода может происходить миграция протона (Н+) по эстафетному механизму, приводящие к делокализации протона в пределах кластера.

Рис. Ассоциация пяти отдельных кластеров в клатрат.
Вода, состоящая из множества кластеров различных типов, образует иерархическую пространственную жидкокристаллическую структуру, которая может воспринимать и хранить огромные объемы информации.
На рисунке в качестве примера приведены схемы нескольких простейших кластерных структур.
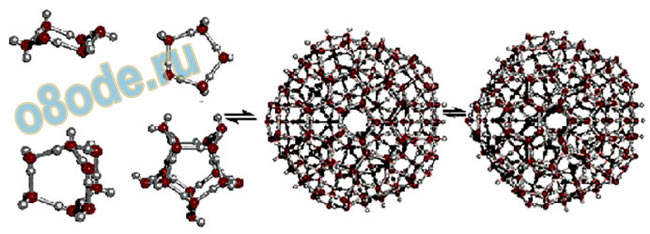
Для каждой температуры в водной системе имеет место равновесие:
Н2О <=> (Н2О)2 <=> (Н2О)3 <=> (Н2О)n
С повышением температуры равновесие смещается в сторону образования одиночных молекул, а с понижением – ассоциированных. Ассоциация молекул воды через водородные связи является причиной её аномальных свойств по показателям температуры кипения, теплоёмкости, теплоты парообразования и др, считает изобретатель. Если бы вода не была ассоциированной жидкостью, то, как мономолекулярная окись водорода, она имела бы температуру кипения около минус 80 С.
Под воздействием физического фактора, препятствующего формированию водородных связей и ассоциации молекул воды в димеры, триммеры и полимеры, вода в этой ячейке начинает переходить в парообразное состояние при температуре минус 80 С с интенсивной дистилляцией воды за счёт тепла окружающей среды. Когда пар выйдет из зоны действия этого физического фактора и войдёт в конденсатор, вода вновь приобретёт способность к ассоциации и, соответственно, начнёт конденсироваться в жидкость при температуре окружающей среды.
Лед и пар - различные агрегатные состояния воды, и поэтому логично предположить, что в жидкой промежуточной фазе валентный угол отдельной молекулы воды лежит в диапазоне между значениями в твердой фазе и в паре. В кристалле льда валентный угол молекулы воды близок к 109,5о. При таянии льда межмолекулярные водородные связи ослабевают, расстояние Н-Н несколько сокращается, валентный угол уменьшается. При нагревании жидкой воды происходит разупорядочение кластерной структуры, и этот угол продолжает уменьшаться. В парообразном состоянии валентный угол молекулы воды составляет уже 104,5о.
Но если это угол меняется от температуры, то, возможно он изменится и при воздействии на воду сильного электромагнитного поля?
Изобретатель В. М. Рофман считает, что посредством управления процессами электромагнитного взаимодействия можно устранить зарядовую асимметрию и угловую форму молекулы воды трансформировать в симметричную, линейную структуру, не образующую ассоциаций. Такое изменение конфигурации молекулы воды можно осуществить считает В. М. Рофман, если к её положительному и отрицательному зарядовым центрам одновременно приложить деформирующие силы, направленные противоположные стороны, используя известный физический эффект генерации сил Лоренца в постоянном магнитном поле.
При этом сам изобретатель признаётся, что никаких существенных изменений в степени ассоциации молекул воды при её магнитной обработке не происходит. При тепловом движении дипольной молекулы воды перпендикулярно силовым линиям магнитного поля, вдоль оси Y (см. вектор V), будет возникать момент сил F1, F2 (сила Лоренса), пытающихся развернуть молекулу в горизонтальной плоскости. При движении молекулы в горизонтальной плоскости, вдоль оси Z , будет возникать момент сил в вертикальной плоскости.
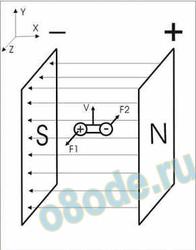
Рис. Молекула воды в магнитном поле
Из этих рассуждений видно, что изменить структуру молекулы сила Лоренца никак не может, а действует она исключительно на движущуюся перпендикулярно силовым линиям магнитного поля молекулу. Когда мы говорим об ассоциации молекул воды, эти физические апелляции к силе Лоренца вообще лишены всякого смысла и абсурдны. Тем более абсурдны выводы о том, что сила Лоренца растягивает молекулу. Поскольку сила Лоренца всегда направлена перпендикулярно скорости движения молекулы, она не создаёт работы и не изменяет энергии заряженной частицы. Она только изменяет направление её движения – отклоняет её с её траектории, ни каким образом не изменяя её энергии и тем более она не может вызвать молекулярные перестройки.
Однако, как считает изобретатель, если заряды диполей воды сориентировать внешним электрическим полем строго регулярно, под углом 90 относительно вектора магнитной индукции, то можно получить необходимый эффект резкого снижения степени ассоциации в водной среде. Хотя совершенно непонятно каким образом это можно достигнуть? Ведь сила Лоренца не способна изменить ни энергию ни структуру молекулы и тем более вызвать перераспределению внутренней энергии между различными видами химических связей - ковалентной и водородной.
Если даже допустить, что при наложении сильного электромагнитного поля на движущиеся диполи молекул воды в электромагнитной ячейке будет происходить генерация собственных электромагнитных полей и наложение - супериндукция поля в результате чего валентный угол в молекуле будет меняться так, что теоретически могут образовываться молекулы с различными валентными углами, то всё равно это изменение валентного угла будет чрезвычайно малым и непостоянным. А эффект изменения валентного угла будет таким незначительным, что это не будет оказывать влияние на свойства воды. И совершенно непонятно, как такое малое изменение валентного угла скажется на ассоциативность молекулы. Например, в самой ассоциативной структуре твёрдой воды – кристалле льда валентный угол молекулы воды близок к 109,5о. При таянии льда межмолекулярные водородные связи ослабевают, расстояние Н-Н несколько сокращается, валентный угол уменьшается. При нагревании жидкой воды происходит разупорядочение кластерной структуры, и этот угол продолжает уменьшаться. В парообразном состоянии воды, где вода присутвует в виде отдельных молекул валентный угол составляет 104,5о, т.е. происходит уменьшение на 5 градусов. Но это уменьшение во первых непостоянное, стоит воде вновь сконденсироваться в жидкость – валентный угол становится приблизительно равным 106о, т.е. увеличивается на несколько градусов и когда вода кристаллизуется в лёд он становится опять близок к правильному тетраэдр, т.е. 109,5о. Но представление о молекуле воды как о линейной структуре для химика – полнейший абсурд, поскольку как известно именно такое строение молекулы воды обусловлено электростатическими силами притяжения и отталкивания между двумя положительно заряжёнными атомами водорода и отрицательно заряженной неподелённой парой атома кислорода. Именно эта свободная пара электронов и разворачивает молекулу в пространстве.
Таким образом, эта модель совершенно не объясняет каким образом под воздействием электромагнитного поля происходят внутримолекулярные изменения и пока лишь остается красивой гипотезой, одной из не многих и не более этого.
Литература: Апельцин И. Э., Клячко В. А., Опреснение воды, М., 1968; Павлов Ю. В., Опреснение воды, М., 1972: Слесаренко В. Н., Современные методы опреснения морских и соленых вод, М., 1973, Spiegler К. S. [е. d.], Principles of desalination, N.Y. - L., 1966., Рофман В. М. paragraf207.com/Perelik/Soveti/4.html