Новый взгляд на структуру и аномальные свойства воды
А.А.Гришаев, независимый исследователь
1. Введение.
Считается, что аномальные свойства воды – повышенные температуры плавления и кипения, большая диэлектрическая проницаемость, способность к образованию ассоциатов, и др. – обусловлены наличием т.н. водородных связей между молекулами воды [1-3]. Но что такое водородная связь? Полагают, что атом водорода в молекуле воды, оставаясь химически присоединён к своему атому кислорода, способен образовать слабую связь с атомом кислорода другой молекулы воды. Схематически, такой водородный мостик обозначают
О – Н ××× О,
где штрих означает химическую связь, а троеточие – слабую. Структура льда [1-3], как полагают, построена на таких водородных мостиках. В обычном гексагональном льду (лёд I, при атмосферном давлении) элементарная кристаллическая ячейка имеет тетрагональную симметрию: центральная молекула воды окружена четырьмя соседними молекулами, которые находятся в вершинах тетраэдра. Считается, что на центральную молекулу приходится четыре водородные связи, две из которых порождаются двумя «своими» атомами водорода, а две других – двумя «чужими». Малая плотность льда обусловлена большой длиной водородных мостиков: расстояния между ядрами кислорода составляют 2.76 Ангстрем при длине ОН-связи 0.96 Ангстрем [1].
Разумного объяснения феномена водородной связи не дают ни «электростатическая» модель Полинга, ни метод молекулярных орбиталей (см., например, [4,5]). Объяснение межатомных связей с позиций электростатики нелепо [6] – в согласии с теоремой Ирншоу: «устойчивая статическая конфигурация электрических зарядов невозможна» [7]. Действие этой теоремы распространяется, очевидно, и на совокупности атомов или молекул, в которых электроны представляют размазанными по т.н. электронным облакам. Что же касается метода молекулярных орбиталей, то он ровным счётом ничего не объясняет: он лишь описывает молекулярные соединения – причём, не только существующие, но, с неменьшим успехом, и «не существующие» [8].
Таким образом, в рамках традиционных представлений не находит объяснения феномен длинных связей между молекулами воды – а ведь этими длинными связями во многом определяются аномальные свойства воды, и, практически, полностью определяется структура льда. В данной статье мы предлагаем физическую модель, которая, на наш взгляд, приоткрывает тайну этих длинных связей.
2. Необходимые предварительные замечания.
Как мы излагали ранее [9], каждый атомарный электрон связан лишь с одним соответствующим ему протоном ядра. Причём, кулоновское взаимодействие не играет здесь никакой роли: атомарная связка «протон-электрон» формируется благодаря попеременным прерываниям квантовых пульсаций на электронной частоте [10] у электрона и протона – из-за чего они вынуждены находиться на определённом расстоянии друг от друга [11]. Поскольку их заряды при этом оказываются в бытии попеременно, то отпадает необходимость в механизме, препятствующем их кулоновскому притяжению – и атомарный электрон не обязан пребывать в орбитальном или ином движении для того, чтобы атомная структура была устойчивой.
Поэтому мы не разделяем ни резерфордовский подход, согласно которому атомарные электроны обращаются вокруг ядра, ни квантово-механический подход, согласно которому они размазаны по электронным облакам. Мы полагаем, что каждый атомарный электрон пребывает в индивидуальной области удержания, в которой на него действует связующий алгоритм. Эта область удержания имеет, по-видимому, шаровую форму и размер, на порядок меньший расстояния от ядра. Мы привели свидетельства [12] о том, что расстояние между электроном и протоном в атомарной связке не увеличивается при появлении у этой связки энергии возбуждения. Т.е., атомный радиус не зависит от того, возбуждён атом или нет – будучи всегда таковым, каков он в основном состоянии.
Химическая же связь, как мы излагали ранее [6], возможна при перекрытии областей удержания двух валентных электронов [9], принадлежащих тому и другому связуемым атомам. Химическая связь представляет собой циклический процесс [6], при котором каждый из этих электронов переключается из состава одного атома в состав другого.
По логике нашей модели химической связи, атом кислорода, имеющий два валентных электрона, может химически присоединить не более двух атомов водорода – причём, в направлениях двух задействованных валентностей кислорода, на периферии получившейся молекулы воды будут находиться два «голых» протона.
3. Модель длинной связи между молекулами воды.
Длина ОН-связи, т.е. расстояние между ядром кислорода и «голым» протоном, в молекуле водяного пара составляет 0.96 Ангстрем [1]. Эта величина, практически, равна сумме атомных радиусов кислорода и водорода. Длина же водородных связей во льду, т.е. расстояние между ядрами кислорода, составляет 2.76 Ангстрем [1] – что, практически, втрое (!) больше длины ОН-связи. Эта троекратность и подсказала нам версию механизма длинных связей между молекулами воды.
Такая связь, на наш взгляд, осуществляется не через одну группу ОН, как это принято считать, а через две, принадлежащие той и другой связуемым молекулам воды – как это схематически показано на Рис.1. При такой конфигурации существует возможность связки двух молекул воды, если расстояние между «голыми» протонами из задействованных групп ОН как раз равно длине ОН-связи.

Рис.1
Действительно, в нашей модели химической связи [6], встречные переключения валентных электронов – из состава одного атома в состав другого – упорядочиваются циклическими перебросами кванта возбуждения из одного атома в другой. В условиях теплового равновесия, наиболее вероятная энергия этого кванта соответствует максимуму равновесного спектра, т.е. составляет 5kT, где k – постоянная Больцмана, T – абсолютная температура. Перебросы кванта возбуждения автоматически управляются Навигатором квантовых перебросов энергии [13]. Роль Навигатора при формировании химической связи подробно описана в [6]. По логике «цифрового» физического мира [14], Навигатор сканирует пространство вокруг возбуждённого атома в поисках атома-адресата, которому может быть переброшена энергия возбуждения: от ядра возбуждённого атома начинает расходиться сферическая «поисковая» волна. У первого же атома, который накрывает эта волна, появляется шанс стать получателем энергии возбуждения. При обычной химической связи, таким получателем оказывается – с вероятностью, близкой к единице – ближайший сосед, поэтому квант возбуждения может неограниченно долго перебрасываться из одного из связуемых атомов в другой, и обратно. Ситуация же, изображённая на Рис.1, несколько иная. Когда в задействованной группе ОН возбуждён атом водорода, то поисковая волна, расходящаяся от его ядра, т.е. от протона, практически одновременно накрывает как ядро атома кислорода из своей группы ОН, так и ядро атома водорода из чужой группы ОН. Поэтому вероятности переброса кванта возбуждения как своему атому кислорода, так и чужому атому водорода – практически одинаковы. Таким образом, существует реальная возможность переброса кванта из одной группы ОН в другую – и поэтому весьма вероятен процесс циклических перемещений кванта «туда-сюда» вдоль всей цепочки О–Н…Н–О. Этот процесс, способный длиться неопределённо долго, и порождает, на наш взгляд, длинную связь между молекулами воды.
Может показаться непривычным, что сам по себе циклический обмен квантом возбуждения у пары атомных групп способен оказывать на эту пару механически стабилизирующее действие. Наверное, особенно непривычно это покажется тем теоретикам, для которых вполне привычна ковалентная связь «на обменной энергии» - т.е. на чисто математическом трюкачестве [6]. Но о том, что вышеизложенная модель длинной связи физична, и что повторяющиеся перебросы кванта возбуждения могут оказывать механическое связующее действие на молекулы, свидетельствует известный эффектный опыт. В кювету с оптически нелинейной жидкостью, например, с нитробензолом, направляют лазерный луч – так, чтобы он проходил параллельно поверхности жидкости на небольшой глубине. Интенсивность лазерного луча должна быть такой, чтобы произошла нелинейная канализация энергии, т.е. чтобы образовался «световод» в жидкости. После этого, с помощью вентилятора обдувают поверхность жидкости, пуская по ней волну. И эта волна заставляет волнообразно изгибаться «световод», по которому идёт лазерный луч!
Не будем упускать из виду, что модель длинной связи кардинально расходится с моделью водородной связи в вопросе о структуре связующего мостика. Согласно модели водородной связи, «на каждой линии кислород-кислород находится только один атом водорода» [1], тогда как модель длинной связи говорит о двух атомах водорода между двумя связуемыми атомами кислорода (см. Рис.1). Какая из этих моделей лучше согласуется с экспериментом, т.е. с результатами структурных исследований?
4. Структура льда по данным нейтронографии.
В работе [15] исследовалась структура монокристалла тяжёлого льда (D2O, при температурах –50оС и –150оС) методом рассеяния на нём нейтронов с энергией, эквивалентной длине волны 1.062 Ангстрем. Конфигурация атомов в тяжёлом льду, практически, идентична их конфигурации в обычном льду (Н2О), тогда как рассеяние нейтронов на ядрах дейтерия эффективнее, чем на ядрах водорода – что даёт возможность получить более качественные картины рассеяния.
Анализ этих картин дал конфигурацию элементарной кристаллической ячейки, которую мы воспроизводим на Рис.2. Мы видим, что опыт чётко свидетельствует о двух наиболее вероятных положениях ядер дейтерия на каждой линии кислород-кислород – что вполне соответствует структуре длинной связи, схематически изображённой на Рис.1. Однако, очевидна невозможность стационарных длинных связей через пару атомов дейтерия или водорода, поскольку этих атомов требовалось бы вдвое больше, чем следует из химического состава воды. Авторы [15] полагали, что их результаты подтвердили модель водородной связи, через один атом водорода – который может находиться в двух положениях: ближе либо к одному атому кислорода, либо к другому. Но поскольку эти два положения оказались равновероятными, авторы говорили об «усреднённой структуре льда», а которой «полу-атом водорода находится в каждом из 4N положений, содержащихся в упаковке из N атомов кислорода» [15] (перевод наш), и на своём рисунке (Рис.2) они обозначили малым кружком «полу-атом дейтерия». Но, насколько нам известно, до сих пор не предложена модель, которая объясняла бы – что должно происходить на молекулярном уровне во льду, чтобы, на линии каждой связи О…О через один атом водорода, для него имелось бы два равновероятных положения.
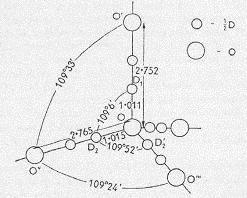
Рис.2
Между тем, эту загадку разрешает вышеизложенная модель длинной связи О–Н…Н–О. Однако, как уже отмечалось выше, в воде не хватит атомов водорода для того, чтобы длинные связи во льду были стационарными. Тогда можно допустить, что, на каждый момент времени, длинными связями во льду связана лишь часть пар соседствующих атомов кислорода – т.е., что длинные связи являются переключаемыми. Иными словами, межмолекулярная структура воды в конденсированном состоянии (жидком или твёрдом) является динамической. Этот вывод, который оказывается удивительно плодотворным, является, на наш взгляд, следствием динамичности структур самих молекул воды – когда вода находится в конденсированном состоянии.
5. Динамичность структур молекул воды в конденсированном состоянии.
Традиционно считается, что структура молекулы воды «нерушима» - в пределах запаса устойчивости, который обеспечивается двумя стационарными химическими связями в этой молекуле. Действительно, молекулы Н2О в водяном паре ведут себя как статические структурные образования – здесь нет места для какой-нибудь динамики их структуры. Но в конденсированных состояниях – которые возможны лишь при количествах соседствующих молекул воды, больших чем некоторое критическое – молекулы воды должны иметь дополнительную степень свободы.
Мы полагаем, что эта дополнительная степень свободы обусловлена особым, динамическим, режимом у атомов кислорода. А именно: четыре самые длинные связки «протон-электрон» у кислорода переводятся из состояния невалентных в состояния валентных поочерёдно – так, что валентными, на любой момент времени, являются какие-либо две из них. Ранее [16] мы говорили об аналогичном феномене – циклических переключениях направленных валентностей у атомов металлов. Но у атома металла эти переключения, как нам представляется, имеют место независимо от его агрегатного состояния, а частоты этих переключений зависят только от температуры [17]. У атомов же кислорода в молекулах воды, как мы полагаем, переключения направленных валентностей имеют место лишь при конденсированных состояниях.
Каковы оказываются следствия этих переключений направленных валентностей? Если кислородная связка «протон-электрон», к которой химически присоединён атом водорода, перестаёт быть валентной, то химическая связь в этой группе ОН немедленно «отключается», что делает возможным отсоединение атома водорода без каких-либо энергозатрат. В условиях близкого соседства молекул воды, этот атом будет изъят и присоединён к одному из соседних атомов кислорода – через одну из его свободных связок «протон-электрон», которая вновь стала валентной. Этот процесс перехода атома водорода в состав соседней молекулы воды должен происходить за характерное «химическое» время, т.е. за ~10-12-10-11 с. Таким образом, вода в конденсированном состоянии предстаёт перед нами не в виде механического конгломерата молекул, имеющих неизменный атомный состав, как это обычно представляют – а в виде бурлящей на молекулярном уровне среды, в которой каждая молекула регулярно обменивается атомами водорода с соседями.
По логике вышеизложенного, длинные связи возможны между теми молекулами воды, у которых атомы водорода из их групп ОН оказываются на расстоянии, примерно равным длине ОН-связи. Кристаллическая структура на таких связях возможна лишь при чёткой согласованности частот и порядка переключений направленных валентностей у атомов кислорода, в результате чего молекула воды почти всё время имеет длинные связи с двумя соседями. В жидкой же воде отсутствует кристаллическая упорядоченность переключений длинных связей – мы полагаем, что здесь допустимы длинные связи, у которых цепочка атомов О–Н…Н–О не обязательно вытянута «в струночку». А именно, здесь допустимы «ломаные» цепочки длинных связей, как это схематически изображено на Рис.3.
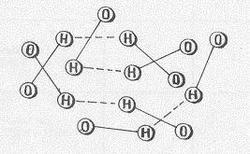
Рис.3
Как можно видеть, расстояния между атомами в вершинах этих «ломаных» остаются прежними, и вышеописанный механизм циклических перемещений кванта возбуждения «туда-сюда» по цепочке О–Н…Н–О ничуть не осложняется. Здесь и скрывается, на наш взгляд, главная причина различий структур льда и воды: длинные связи нестационарны, переключаемы, но во льду они «вытянуты в струночку», а в воде они могут быть «ломаными». Этим качественно объясняется то, что вода, по сравнению со льдом, имеет несколько большую плотность и несопоставимо большую текучесть.
6. Присущи ли воде скрытые теплоты фазовых превращений?
Вышеизложенная модель кардинально расходится с традиционным подходом – согласно которому, жидкое состояние воды отличается от твёрдого тем, что в жидком состоянии «часть водородных связей разорвана». Так, Полинг для количества разорванных водородных связей в воде получил расчётную цифру 15% [1], взяв за основу теплоту сублимации льда. Казалось бы, такой подход корректен, поскольку считается, что, именно благодаря водородным связям, у льда и воды аномально велики теплоты сублимации, плавления и испарения.
Но заметим, что теплота сублимации здесь является не экспериментальной величиной – она принята равной сумме теплот плавления и испарения. Плавление же, как и замерзание воды, происходят при постоянной характеристической температуре. Как можно измерить скрытую теплоту такого процесса? В калориметрическом методе измеряемой величиной является приращение температуры буфера. Но это приращение равно нулю, если исследуемый процесс протекает изотермически. Нас пытаются убедить в том, что, например, для процесса плавления, несмотря на его изотермичность, требуется тепло из окружающей среды – это, якобы, и есть скрытая теплота плавления. Но вот простой пример: во внутреннем стаканчике калориметра находятся вода и лёд – в тепловом равновесии с буфером. При достижении точки ликвидуса, фазовое равновесие между льдом и водой нарушается. Если далее тепло для таяния льда будет заимствоваться из буфера, то температура буфера понизится – и, следовательно, поток тепла «на таяние» прекратится. Между тем, при тепловом равновесии смеси вода-лёд с буфером, в условиях даже минимального превышения точки ликвидуса, лёд растает весь. Откуда же он позаимствует тепло в этом случае?
Природные явления дают ещё более поразительные указания на то, что с теплотами фазовых превращений воды – что-то не так. Рассмотрим, что должно происходить при образовании льда на открытых водоёмах – если замерзание воды сопровождается выделением теплоты плавления. Лёд нарастает снизу, а теплопроводность у льда на два порядка хуже, чем у воды – поэтому, практически, вся названная «теплота» должна выделяться в воду подо льдом. Запишем уравнение теплового баланса; справочные величины таковы: теплота плавления льда – 330 кДж/кг, плотность льда – 900 кг/м3, удельная теплоёмкость воды – 4.19 кДж/(кг×град), плотность воды – 1000 кг/м3. И получим, что образование слоя льда толщиной 1 мм вызывало бы нагрев прилегающего слоя воды толщиной 1 мм на 70 градусов, а слоя в 0.5 мм – на 140 градусов (правда, уже при 100оС началось бы кипение). Мы здесь не учитывали конвекцию: в интервале от 0о до 4оС, более тёплая вода опускается, а более холодная поднимается. Но, даже в условиях такой конвекции, при наличии на поверхности воды источника тепла имел бы место соответствующий градиент температуры: у поверхности вода была бы теплее. В действительности же, типичный арктический профиль температуры в воде подо льдом чётко показывает: контактирующая со льдом вода имеет температуру, близкую к точке замерзания, а, по мере увеличения глубины (в пределах некоторого слоя), температура увеличивается [18] – что свидетельствует об отсутствии потока тепла в воду от льда, даже от растущего. Океанологи давно заметили этот парадокс, поэтому они ухватились за успокаивающий их тезис о том, что «тепло кристаллизации… следуя направлению градиента температуры, уходит через лёд в атмосферу» [18]. Неужели океанологи не знают, что теплопроводность у льда на два порядка хуже, чем у воды?
Кстати, не обязательно отправляться в Арктику, чтобы убедиться в отсутствии выделения тепла при замерзании воды. В телепрограмме «Разрушители легенд» демонстрировали следующий эффектный опыт. Из холодильника берётся бутылка переохлаждённого жидкого пива. Шлепок по этой бутылке – и пиво в ней за несколько секунд замерзает в ледяные хлопья. При этом бутылка остаётся холодной – проверено! Куда же тогда девается «тепло кристаллизации»?
Теперь рассмотрим испарение воды и допустим, что для её испарения требуется заимствование тепла из окружения – в частности, из остающейся воды, которая ещё не испарилась. В пользу охлаждения воды при испарении с её поверхности, приводят известный пример с измерителем влажности воздуха, на основе двух одинаковых термометров, у одного из которых шарик со ртутью обмотан влажной тряпочкой. При испарении воды с этой тряпочки, увлажнённый термометр показывает меньшую температуру, чем сухой. Но является ли эта разность показаний свидетельством о корректности справочного значения теплоты испарения воды? Это значение составляет 2450 кДж/кг [19], если пренебречь слабой температурной зависимостью в диапазоне от 0о до 100оС. Пусть влажность воздуха невелика, и испарение происходит интенсивно. Будем считать, что лишь половина тепла, требуемого на испарение, приобретается за счёт охлаждения остающейся воды (а вторая половина – за счёт охлаждения окружающего воздуха). Пусть некоторое исходное количество воды находится при некоторой стартовой температуре. Какая часть от исходного количества воды должна испариться, чтобы оставшаяся часть охладилась до 0оС? Ответ представляет нижняя зависимость на Рис.4. Можно возразить, что испарение происходит не мгновенно – при этом охлаждается и та вода, которая ещё успеет испариться. Допустим, что это так, и переформулируем задачу: какая часть воды должна испариться, чтобы, на тепловом эффекте этого перехода, вся исходная вода могла бы охладиться до 0оС? Ответ представляет верхняя зависимость на Рис.4. Эта верхняя зависимость, в рамках сформулированной задачи, даёт завышенные цифры, а нижняя зависимость – заниженные; «правильные» цифры должны находиться где-то между этими двумя зависимостями. Но эти «правильные» цифры совершенно неадекватны реалиям, ведь обычно разность показаний сухого и увлажнённого термометров составляет всего-то единицы градусов – причём после того, как эта разность стабилизируется, она, практически, не изменяется до конца испарения воды. Значит, эта разность говорит отнюдь не о корректности справочного значения теплоты испарения воды.
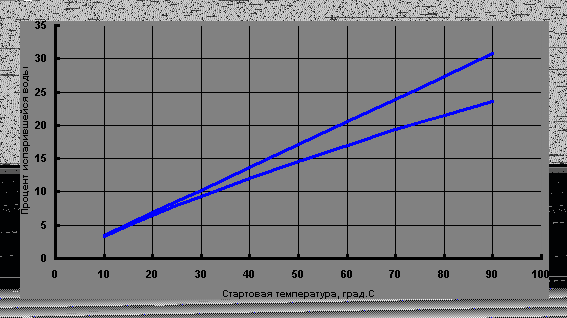
Рис.4
Но каков тогда механизм охлаждения влажной тряпочки? Выше (п.5) упоминалось о том, что жидкое состояние воды возможно лишь при наличии достаточно большого коллектива её молекул. В процессе испарения воды с тряпочки, уменьшаются размеры остающихся микрокапель – и мы полагаем, что при достижении микрокаплей некоторого критического размера, происходит её скачкообразный переход в парообразное состояние. Можно сказать, что происходит взрывное испарение микрокапли, с резким расширением получившихся водяных паров – а, при расширении газа, он, как известно, охлаждается.
Приведённые выше примеры иллюстрируют, к каким противоречиям с практикой мы приходим, если брать за основу справочные значения теплот плавления и испарения воды. На наш взгляд, эти теплоты являются фикцией: фазовое превращение происходит при характеристической температуре, но заимствованием или отдачей тепла оно не сопровождается. Этот тезис вполне согласуется с моделью длинных связей в воде (п.3). Действительно, модель длинных связей является развитием нашей модели химической связи [6] – согласно которой, энергия химических связей, как отдельная форма энергии, не существует [20].
7. Какова причина аномальных электрических свойств воды?
Считается, что часть молекул жидкой воды диссоциирована на ионы гидроксила ОН- и водорода Н+. Измерения константы диссоциации дают, что в чистой воде при 0оС концентрация тех и других ионов составляет 3.38×10-8 от концентрации молекул воды, а при 100оС эта цифра составляет 7.7×10-7 [21], т.е. на интервале температур в 100о концентрация ионов изменяется почти в 23 раза. Каков механизм этой диссоциации на ионы ОН- и Н+?
Уточним, что речь ведут о полноценных ионах: молекула воды, якобы, диссоциирует таким образом, что атом водорода оставляет свой электрон в группе ОН. Могут ли ионы ОН- и Н+ в воде быть результатом тепловой диссоциации? Энергия диссоциации молекулы воды на нейтральные радикалы ОН и Н составляет 116 ккал/моль [22], или 5.0 эВ. Энергию диссоциации на ионы ОН- и Н+ мы не нашли в литературе – но она, очевидно, больше энергии диссоциации на нейтральные радикалы. Тогда, тепловая диссоциация могла бы дать отношение концентраций ионов и нейтральных молекул, которое, по Больцману, заведомо меньше, чем exp{-5.0эВ/kT} – что при комнатной температуре составляет e-192»4.1×10-84. Запредельная малость этой величины говорит о том, что механизм диссоциации молекул воды на ионы ОН- и Н+ не является тепловым. Не является он и радиационным – о чём свидетельствует температурная зависимость концентраций этих ионов. Но тогда каков же этот механизм? Не говорить же всерьёз о том, что вода является настолько универсальным растворителем, что немного растворяет даже саму себя!
Как отмечалось выше (п.5), каждая молекула воды, обмениваясь атомами водорода с соседями, постоянно испытывает циклические диссоциации-рекомбинации. Следует добавить один штрих, чтобы дополнить эту картину сопутствующими электрическими феноменами. Мы полагаем, что переключения направленных валентностей в атоме кислорода производятся в такие моменты времени, когда в связке «протон-электрон», валентность которой «отключается», в тепловом бытии находится электрон – в результате эта связка на некоторое время «зависает» в состоянии, имитирующем наличие нескомпенсированного отрицательного элементарного заряда. Атом водорода, как отмечалось выше, без каких-либо энергозатрат отделяется от кислородной связки «протон-электрон», потерявшей статус валентной. Но эта связка имитирует отрицательный элементарный заряд – поэтому сразу после того, как электрон водорода покинет область удержания электрона кислорода, атом водорода проиндуцирует противоположный, т.е. положительный зарядовый разбаланс. В этом состоянии – с «зависшим» в тепловом бытии протоном – атом водорода будет проявлять себя как протон (такое «зависание» блокирует возможность колебаний зарядового разбаланса, т.е. блокирует возможность возбуждения атома [12]. Этим можно объяснить, почему у воды, кишащей атомарным водородом, отсутствуют водородные спектральные линии поглощения-излучения – в частности, вода прозрачна в видимом диапазоне). Обрисованная картина означает, что вода буквально бурлит электричеством: постоянно происходит тотальная диссоциация-рекомбинация молекул, причём они диссоциируют на частицы, несущие противоположные электрические заряды. Благодаря этому тотальному ауто-гидролизу воды и возможен её т.н. электролиз, причём даже при напряжениях между электродами в единицы вольт. Для сравнения: «электролиз», например, бензина возможен лишь при достижении пробивного напряжения. Воду можно рассматривать как жидкую плазму, но следует иметь в виду, что электрические заряды в этой плазме являются проимитированными – будучи обусловлены соответствующими зарядовыми разбалансами – и что времена жизни этих электрических зарядов невелики, будучи сопоставимы с характерным химическим временем (п.5). На наш взгляд, именно наличие этих зарядов в воде обусловливает аномально высокую (»80) диэлектрическую проницаемость воды в постоянном поле (в переменном поле эта величина быстро уменьшается при увеличении частоты).
Малость времён жизни этих зарядов объясняет, почему традиционными методами исследования не обнаруживается тотальная диссоциация молекул воды на радикалы Н[+] и OH[-], где квадратные скобки означают, что заряд проимитирован через статический зарядовый разбаланс. Так, при исследованиях электропроводности воды, успевают проявить себя лишь радикалы Н[+] и OH[-], находящиеся в тончайших приэлектродных слоях, что и порождает иллюзию ничтожности концентраций ионов ОН- и Н+ в воде – ведь эти ионы считаются долгоживущими. И, в рамках традиционного подхода, не находит разумного объяснения факт аномально высокой подвижности «долгоживущих» ионов Н+ в воде и во льду – причём, «во льду подвижность протонов примерно в сто раз больше, чем в жидкой воде» [23]. Это выглядит так, как будто «протон, подходя с одной стороны к цепочке молекул воды, связанных водородной связью, вызывает появление свободного протона с другой стороны цепочки» [23]. Авторы [4], не вдаваясь в подробности, говорят, что «миграция протона вдоль Н-связей происходит за счёт сравнительно быстрого туннельного эффекта». Это сказочное объяснение нас не устраивает. По логике вышеизложенного, за быструю миграцию протона в воде и особенно во льду ошибочно принимают результат цепочки последовательных переформирований составов молекул. «Лишний протон» включается в состав молекулы, отчего другой протон оказывается «лишним», и т.д. В итоге протон, который «появился» в конце этой цепочки – это далеко не тот же протон, который «исчез» в её начале.
8. Чем обусловлена химическая агрессивность воды?
Традиционно считается, что химическая агрессивность жидкой воды, в частности, её высокая растворяющая способность, обусловлена электростатическим действием электрических диполей, каковыми являются молекулы воды. Эти диполи, якобы, разворачиваясь к атомам растворяемого вещества теми или иными своими полюсами, буквально растаскивают это вещество на ионы.
Мы уже проиллюстрировали ранее: допущение того, что молекула может держаться на электростатическом притяжении ионов, приводит к абсурдным выводам [6]. Не менее абсурдно, на наш взгляд, допущение того, что молекула может быть разорвана на ионы электростатическим действием дипольных молекул. Достоверно известно: чтобы заряженная частица ионизировала вещество, она должна иметь некоторую пороговую энергию. У электрического диполя ионизирующая способность гораздо хуже, чем у заряженной частицы, поскольку действия противоположных зарядов диполя частично компенсируют друг друга. Остаётся возможность столкновительного развала вещества на ионы – но этим, тепловым, механизмом не объяснить высокую растворяющую способность воды.
Между тем, эта высокая растворяющая способность прямо следует из вышеизложенной модели – согласно которой, вода кишит радикалами ОН[-] и Н[+], имеющими свободные валентности. Правда, времена жизни этих свободных валентностей сопоставимы с характерным химическим временем (п.5) – но этого достаточно для образования химических связей с атомами контактирующего вещества – если такая возможность имеется.
Вот, например: как происходит водная коррозия чёрных металлов? Странным образом, в учебниках по физической химии [21,24] эта коррозия трактуется как электрохимическая – через образование гальванической пары металлов и растворение того из них, который имеет более положительный потенциал. Но даже дети знают, что, при контакте с водой, железо обычно не растворяется, а превращается в ржавчину. В школе детям объясняют, что ржавчина – это гидроокись железа, т.е. результат химической реакции. А откуда берётся кислород при образовании этой гидроокиси? «Из воздуха, конечно», - отвечают теоретики. Но известно, что «при неравномерной аэрации сильнее всего корродируют участки, куда доступ кислорода затруднён, например подводные части металлических сооружений…» [24]. Не означает ли это, что для водной коррозии железа не требуется дополнительный кислород – кроме того, который входит в химический состав воды?
В самом деле, рассмотрим, что происходит при контакте двух сред, имеющих динамические структуры: металла, атомы которого испытывают циклические переключения направленных валентностей [16], и воды, кишащей радикалами ОН[-] и Н[+], которые имеют свободные валентности. Как отмечалось в [16], химическая активность чистых непассивированных поверхностей металлов обусловлена тем, что у поверхностных атомов временно валентными периодически оказываются связки «протон-электрон», направленные наружу – эти связки легко образуют химические связи с радикалами внешней среды, также имеющими свободные валентные связки. Поэтому радикалы ОН[-] и Н[+] должны легко «садиться» на валентные связки атомов металла, замыкая их всех на себя и постепенно исключая атомы металла из состава динамической кристаллической решётки – и, таким образом, формировать конгломерат гидроокиси. Подчеркнём, что химическая структура этой гидроокиси является динамической: каждый атом металла в ней продолжает испытывать циклические переключения направленных валентностей, и поэтому он может образовывать химические связи с окружающими его несколькими водными радикалами только поочерёдно.
Теперь мы можем пояснить, почему эффективен метод защиты от коррозии посредством отрицательного потенциала на защищаемом изделии – либо через создание гальванической пары с «жертвенным анодом», либо через подключение к «минусу» источника постоянного напряжения. Отрицательный потенциал позволяет взаимодействовать с изделием радикалам Н[+], но не ОН[-] – поэтому возможность образования гидроокиси исключается.
9. Как проводят ток водные растворы электролитов?
Электролитами называют соли, кислоты и щёлочи, водные растворы которых проводят электрический ток (иногда, для краткости, так называют сами эти растворы) [21]. Считается твёрдо установленным, что электрический ток через раствор электролита обусловлен движением ионов противоположного знака, на которые диссоциировано растворённое вещество. Каждый такой ион считается окружённым гидратной оболочкой, которая уменьшает его подвижность, но бесспорным считается факт, что в центре этой гидратной оболочки находится полноценный ион – например, в растворе поваренной соли это либо ион Na+, с одним потерянным электроном, либо ион Cl-, с одним добавленным электроном.
Корректность этих представлений, как полагают, надёжно подтверждена тем фактом, что, например, продукты гидролиза соли, т.е. металл и остаток, при прохождении постоянного тока движутся к противоположным электродам: металл осаждается на катоде, а остаток выделяется на аноде. Причём, строго выполняется закон Фарадея: количества выделившихся на электродах продуктов гидролиза определяются только количеством электричества, прошедшего через раствор электролита.
Однако, эти традиционные представления обходят молчанием вопрос о механизме гидролиза, который разрывал бы растворяемое вещество не на нейтральные радикалы, а именно на ионы. Так, чтобы выполнялся закон Фарадея для растворов солей алюминия, атомы алюминия там должны быть трижды ионизированы. Энергии связей трёх внешних электронов алюминия есть 5.98, 18.82 и 28.44 эВ [25], что в сумме составляет 53.24 эВ. Это чудовищная, по химическим меркам, величина. Тройная ионизация алюминия не может быть обеспечена растаскиванием молекулы соли дипольными молекулами воды. На это теоретики говорят, что алюминий трижды ионизирован уже в молекуле соли, а молекулы воды растаскивают «готовые» ионы. А почему же эти «готовые» ионы не воссоединяются в растворе? Теоретики отвечают, что ионам мешают воссоединяться их гидратные оболочки. Но этот тезис, на наш взгляд, не выдерживает критики. Действительно, напряжённость электрического поля иона, ослабленная гидратной оболочкой в 80 раз (это значение диэлектрической проницаемости воды) даже на расстоянии 0.1 m от иона составляет десятки киловольт на метр, а ток в электролитической ванне начинает течь при разности потенциалов между электродами в единицы вольт, т.е. при напряжённостях поля менее одного вольта на метр. Выходит, что гидратные оболочки сводят на нет сильное кулоновское притяжение ионов друг к другу, но отнюдь не сводят на нет их гораздо более слабое притяжение к электродам. Это противоречие свидетельствует о некорректности представлений о том, что продукты гидролиза электролитов являются полноценными ионами.
Напротив, мы полагаем, что молекулы электролитов не содержат «готовых ионов», и что продукты гидролиза этих молекул имеют в своих составах одинаковые количества носителей отрицательного и положительного элементарных зарядов. Эффективные же заряды в растворах электролитах появляются в результате взаимодействия продуктов гидролиза с химически агрессивной средой, кишащей радикалами ОН[-] и Н[+].
Так, соли металлов химически неустойчивы (и гигроскопичны), на наш взгляд, из-за циклических переключений направленных валентностей у атомов металла [16]. Пусть у поверхностного атома металла Ме направленная наружу свободная связка «протон-электрон» становится валентной, и в ней начинаются тепловые колебания зарядового разбаланса [9]. Когда в этой связке доминирует отрицательный заряд, он притягивает радикалы Н[+] – которые разворачиваются к атому металла своими протонами, но не электронами, и поэтому образование химического соединения МеН маловероятно. Когда же в той связке доминирует положительный заряд, он притягивает радикалы ОН[-] – которые разворачиваются к атому металла своими свободными электронами, и образование химического соединения МеОН весьма вероятно. При образовании этого соединения, статический зарядовый разбаланс у радикала ОН[-] пропадает; на временах усреднения, больших по сравнению с периодом тепловых колебаний, соединение МеОН ведёт себя как электрически нейтральное. Но заметим, что вблизи МеОН остаётся радикал Н[+], заряд которого оказывается нескомпенсирован. Мы рассмотрели случай одновалентного металла; если же металл, скажем, трёхвалентен, то рядом с соединением Ме(ОН)3 должны находиться три радикала Н[+]. Каждая связь Ме–ОН существует недолго, до потери статуса валентной у задействованной связки «протон-электрон» атома металла – поэтому металло-гидроксильное соединение должно иметь динамическую структуру. Но, в результате, будет формироваться динамический гидратный комплекс с эффективным зарядом, порождаемым радикалами Н[+] – в количестве, равном валентности металла. Этими гидратными комплексами, на наш взгляд, и обеспечивается хорошая электропроводность водных растворов солей металлов.
Что касается растворения в воде кислот и щелочей, то в первом случае в растворе оказывается избыточное количество радикалов Н[+], а во втором – радикалов ОН[-]. Благодаря этим сдвигам электрического равновесия, на наш взгляд, хорошую электропроводность имеют водные растворы кислот и щелочей.
Теперь мы можем пояснить ситуацию со спиртами и сахарами, молекулы которых содержат радикалы ОН и Н и отлично растворяются в воде – но эти растворы плохо проводят электрический ток. Дело в том, что при растворении спиртов и сахаров образуются одинаковые количества радикалов ОН[-] и Н[+] – что, в терминах гидролиза, эквивалентно добавлению чистой воды.
10. В чём секрет феномена структурированности воды?
По логике вышеизложенного, феномен структурированности воды никоим образом не сводится к наличию в ней квазиустойчивых молекулярных ассоциатов, которые «держатся» на стационарных межмолекулярных связях – поскольку, как мы постарались показать, длинные связи в воде являются принципиально переключаемыми. На наш взгляд, разгадка структурированности воды связана со специфической упорядоченностью переключений длинных связей и с сопутствующими электрическими эффектами.
Едва ли можно сомневаться в том, что в монокристалле льда частота и порядок переключений длинных связей заданы весьма жёстко – иначе поддержание кристаллической структуры льда было бы проблематично. В жидкой же воде допускается некоторая «гибкость» этих переключений – и, как результат, возможна адаптация динамической структуры к специфическим молекулам или радикалам.
Структурированность воды, которая возникает при контакте с такими молекулами или радикалами, можно назвать вынужденной. Так, в металло-гидратном комплексе (п.9) каждое переключение направленной валентности у атома металла приводит к нейтрализации заряда радикала Н[+], находившегося по соседству с бывшей металло-гидроксильной связью, и к появлению нескомпенсированного заряда другого радикала Н[+] – по соседству с новой образовавшейся металло-гидроксильной связью. Как можно видеть, в металло-гидратном комплексе происходят вынужденные скачкообразные миграции нескомпенсированного электрического заряда – что должно влиять на динамику длинных связей в окружающей воде. Поскольку переключения направленных валентностей и соответствующие скачки заряда имеют период повторения, то имеет смысл говорить о волнообразных возмущениях обычной картины динамики длинных связей в воде – т.е. о структурных волнах, с сопутствующими им волнами перераспределения электрических зарядов. Отношение расстояния между молекулами, ~3 Ангстрем, к «химическому времени», ~10-12 с, даёт нам грубую оценку скорости структурной релаксации, ~300 м/с – это и есть скорость структурной волны. Умножение этой скорости на период повторения валентных конфигураций у атома металла, ~10-10 с [17], даёт длину «металлической» структурной волны в воде - ~0.1 m. Эта величина кажется, на первый взгляд, слишком малой – соответствуя длине волны ультрафиолетового излучения. Но физические механизмы структурных и электромагнитных волн кардинально различаются, и даже скорости этих волн разнятся на 6 порядков. На длине в 0.1 m укладывается ~300 молекул в воде – поэтому такая длина структурной волны не представляется нам слишком малой. Что касается растворов кислот и щёлочей, то в них также должны происходить «скачки зарядов» благодаря избыточным радикалам Н[+] или ОН[-], и эти «скачки» также должны являться генераторами структурных волн – но у нас недостаточно информации, чтобы оценить их частоту и длину.
Если в большом объёме воды находится локальный источник структурных волн, то они будут распространяться до тех пор, пока не будут погашены тепловыми или механическими шумами. Структурные волны в воде – это не фантазия: известны факты, которые трудно объяснить без допущения того, что некоторые обитатели морей способны воспринимать эти волны. Так, проводились опыты с акулами: на значительном удалении они «моментально» и безошибочно реагировали на появление в воде небольшого количества свежей крови – причём восприятия по обонятельному, зрительному и вибрационному каналам были совершенно исключены. В рамках традиционных представлений эти результаты не нашли объяснения, поэтому они остались малоизвестны.
Теперь рассмотрим случай, когда источник структурных волн находится в небольшом объёме воды, так что весь этот объём оказывается специфически структурирован. Известно, что при осторожном разбавлении такой воды, добавленная чистая вода приобретает такое же структурирование – причём, этот результат повторяется при огромном количестве разбавлений. Таким образом, вышеизложенная модель даёт разумное объяснение феномену гомеопатического целебного действия «мнимых растворов» (см., например, [26,27]). Речь идёт о таких степенях разбавления, при которых, например, на десять склянок с водой приходится не более одной (!) молекулы исходно растворённого лекарства, но вода из каждой из этих склянок оказывает одинаковое специфическое целебное действие – будучи специфически структурированной. Такое структурирование воды можно называть остаточным, или, собственно, «памятью воды». Уместно добавить, что взаимоосвязанность структурных и электрических возмущений в воде означает, что остаточную структурированность воды можно получить, не приводя воду в контакт ни с одной молекулой специфического вещества – а подвергая воду электромагнитному воздействию со специфическим спектром. Такая вода тоже должна оказывать специфическое целебное действие. Сообщалось об удачных опытах подобного рода, но эти результаты также остались малоизвестны.
Наконец, вышеизложенная модель согласуется с феноменом благотворного биологического действия талой воды [28]. При замерзании воды, её структурированность, в том числе патогенная, устраняется – ведь структура льда не зависит от характера структурированности воды, из которой этот лёд образуется. При оттаивании же льда, талая вода некоторое время является «незамутнённой» в структурном смысле, у неё чиста «память» на контактирующие с ней вещества – чем, на наш взгляд, и можно объяснить особую пригодность такой воды для живых организмов. Хорошо известно, что в ночь на 19 января, после полуночи по местному солнечному времени, жидкая природная вода приобретает особые, биологически благотворные, свойства. Мы полагаем, что это является результатом принудительного сброса избыточного структурирования воды, в результате чего она «обновляется», приобретая свойства, близкие к свойствам талой воды. Даже в домашних условиях легко заметить, что, после такого «обновления», у воды из того же источника изменяется вязкость – хотя содержание примесей и растворённых веществ в ней остаётся прежним.
11. Заключение.
Предложенная выше модель длинных связей в воде является развитием нашей модели химической связи [6]. Из принципиальной динамичности структуры, основанной на длинных связях, логично следует тотальная диссоциация молекул воды на короткоживущие радикалы Н[+] и ОН[-]. Вода представляет собой, фактически, жидкую плазму – чем во многом и обусловлены её аномальные свойства. Впрочем, мы обрисовали лишь качественную сторону лишь некоторых особенностей воды – самого удивительного вещества на планете.
Автор благодарит Ивана, автора сайта ivanik3.narod.ru , за помощь в доступе к первоисточникам, а также участников форума на live.cnews.ru за полезное обсуждение.
Комментарий от О.В.Мосина:
У меня возникли некоторые вопросы и сомнения, особенно о так называемом кванте возбуждения и его передаче от одной молекулы к другой. Квантовая теория поля действительно рассматривает любую элементарную частицу как квант возбуждения определенного квантового поля. Причём, для каждого типа частиц вводится собственное поле. Квантовые поля взаимодействуют, в этом случае их кванты могут превращаться друг в друга. Самый яркий пример возбуждения атомов или молекул квантами света, когда квант энергии при поглощении её молекулой заставляет перейти электрон с более низкой на более высокую орбиту, с которой этот электрон опять спускается на более низкую орбиту с излучением кванта света фотона с энергией E=hv. Этот процесс пикосекундный.Возбуждение атомов и молекул также имеет место, например, при радиоактивном распаде и превращении одних частиц в другие (например, деление ядер урана и плутония), которое всегда осуществляется сообщением энергии извне. Если эта энергия достаточно велика, то можно перевести нуклон из его уровня в структуре ядра на уровень, лежащий за пределами ядра.
Так, например, при поглощении ядром гамма-фотонов большой энергии наблюдается выбрасывание из ядра протона, нейтрона или альфа-частицы. Возбуждение ядер возможно в результате не только а -, но и р-распада. Испускаемые при радиоактивном распаде у-лучи имеют энергию кванта hv, как правило, не ниже 0 1 Мэв и представляют собой коротковолновое электромагнитное излучение с длиной волны.
Энергия возбуждения ядра может передаваться не только фотону, но и одному из атомных электронов. Энергия возбуждения, сообщенная ядру при захвате частицы, обусловливает движение ядерной материи, аналогичное движению жидкости под действием поверхностного натяжения. Вследствие деформации ядро подобно жидкой капле может разделиться на несколько осколков. Для возбуждения ядра всегда необходимо сообщить ему достаточное количество энергии ( энергии возбуждения), что можно сделать путем обстрела ядра, например а-частицами или протонами. Если энергия возбуждения ядра окажется меньшей, чем энергия активации, то деформация возбужденного ядра-капли не дойдет до критической, ядро не разделится и вернется в основное состояние, испустив у-квант.Так что совершенно непонятно, откуда берётся такая большая энергия, позволяющая осуществлять такой квантовый обмен квантами возбуждения.
Это на мой взгляд, самый уязвимый момент данной гипотезы. Говоря объективно, стоит ли изобретать велосипед, когда большинство аномальных свойств воды объясняются наличием водородных связей и формированием ассоциатов воды, а не мифическими квантами возбуждения. Ну ладно. Может быть я не прав. Я химик, а не физик.
С уважением, О. В. Мосин
Ссылки к статье
1. Л.Паулинг. Природа химической связи. «Госхимиздат», М.-Л., 1947.
2. Г.Н.Зацепина. Свойства и структура воды. «Изд-во Московского университета», 1974.
3. А.Эйзенберг, В.Кауцман. Структура и свойства воды. «Гидрометеоиздат», Л., 1975.
4. Дж.Пиментел, О.Мак-Клеллан. Водородная связь. «Мир», М., 1964.
5. Г.Герцберг. Электронные спектры и строение многоатомных молекул. «Мир», М., 1969.
6. А.А.Гришаев. Новый взгляд на химическую связь и на парадоксы молекулярных спектров. – Доступна на данном сайте.
7. И.Е.Тамм. Основы теории электричества. «Гос. изд-во технико-теоретической литературы», М., 1956.
8. О.П.Чаркин. Проблемы теории валентности, химической связи, молекулярной структуры. Серия «Новое в жизни, науке, технике», 7, 1987. «Знание», М.
9. А.А.Гришаев. Зарядовые разбалансы – отличительный признак валентных электронов. – Доступна на данном сайте.
10. А.А.Гришаев. Разноимённые электрические заряды, как противофазные квантовые пульсации. – Доступна на данном сайте.
11. А.А.Гришаев. Автономные превращения энергии квантовых пульсаторов – фундамент закона сохранения энергии. – Доступна на данном сайте.
12. А.А.Гришаев. Зарядовые разбалансы в «нейтральных» атомах. – Доступна на данном сайте.
13. А.А.Гришаев. Навигатор квантовых перебросов энергии. – Доступна на данном сайте.
14. А.А.Гришаев. Этот «цифровой» физический мир, 2010. – Доступна на данном сайте.
15. S.W.Peterson, H.A.Levy. A single-crystal neutron diffraction study of heavy ice. Acta.Cryst., 10 (1957) 70.
16. А.А.Гришаев. Металлы: нестационарные химические связи и два механизма переноса электричества. – Доступна на данном сайте.
17. А.А.Гришаев. Температурная зависимость частоты переключений направленных валентностей у атомов металлов. – Доступна на данном сайте.
18. Л.А.Жуков. Общая океанология. «Гидрометеоиздат», Л., 1976.
19. А.С.Енохович. Справочник по физике и технике. «Просвещение», М., 1976.
20. А.А.Гришаев. О температуре и тепловых эффектах химических реакций. – Доступна на данном сайте.
21. Н.Ф.Федулов, В.А.Киреев. Учебник физической химии. «Госхимиздат», М., 1955.
22. Т.Коттрелл. Прочность химических связей. «Изд-во иностр. литературы», М., 1956.
23. Ю.П.Сырников. К вопросу о термодинамических процессах в живой системе и о роли воды в этих процессах. «Структура и роль воды в живом организме», Сборник 1, стр. 58. «Изд-во Ленинградского университета», 1966.
24. А.И.Бродский. Физическая химия. Т.2. «Госхимиздат», М.-Л., 1948.
25. Таблицы физических величин. Справочник. Под ред. акад. И.К.Кикоина. «Атомиздат», М., 1976.
26. Память воды, гомеопатия, опыты, факты, доказательства. Веб-ресурс www.agro-moscow.ru/article_info.php?articles_id=74
27. В.Зильбер. природа действия гомеопатических лекарств. Наука и жизнь, 12, 2000. Доступна также на: www.nkj.ru/archive/articles/9293/
28. А.К.Гуман. Особенности талой воды. «Структура и роль воды в живом организме», Сборник 1, стр. 179. «Изд-во Ленинградского университета», 1966.
Источник: newfiz.narod.ru
спасибо