Сообщение:
Если взять вместо химич. формулы Н2О формулу Н1-НО (Н - элемент-1, Н1 - элемент-119, то что получится?
Всем известно, что вода замерзает при 0 град. С, а кипит - при 100град.С, а вода с хим. формулой Н2О должна замерзать при - (минус) 90град.С, кипеть при - (минус 70град) и все Академики и Доктора наук знают об этом, но объяснить не могут (казус воды) и другие необычные свойства воды. Автор объясняет 20 "необычных" свойств воды - при условии, что хим. формула воды будет Н1-НО (более 20 необыч. свойств воды).
Казус воды
Здравствуйте,
Я честно говоря не знаю, что за элемент 119, но объяснение этому факту очень простое. Никакого казуса
здесь нет. Водород имеет три природных изотопа, различающиеся количеством нейтронов: протий 1H, дейтерий 2Н (или D) и тритий 3Н (или Т), последний из которых радиоактивен. В лабораторных уссловиях были синтезированы и искусственные короткоживущие изотопы водорода 4Н и 5Н.
Кислород в свою очередь имеет три изотопных разновидности: 16О, 17Ои 18О (тяжелый), среднее содержание которых составляет 99,759%; 0,204% и 0,037%. Кроме природных, существуют 10 искусственно созданных изотопов с массовыми числами от 12 до 24. Из них: 12O, 13O, 14O и 15O – легкие, 19O, 20O, 21O, 22O и 23O – тяжелые, а сверхтяжелый изотоп – 24O получен в 1975 году. Как и искусственные изотопы водорода, они недолговечны и радиоактивны. Большинство радиоактивных изотопов кислорода имеют периоды полураспада от несколько десятков секунд до наносекунд. Наиболее стабильные изотопы 14O и 15О с периодом полураспада 122 и 50 сек.
С учетом этих данных количество возможных изотопных разновидностей воды (изотопологов) с химической формулой Н20 составляет 135, в которых атомы Н, D, T, 16O, 17O и 18O представлены в различных сочетаниях. Однако распад почти всех радиоактивных изотопов водорода и кислорода происходит за секунды или доли секунды (иключением является тритий, период полураспада которого составляет 12 лет). За это короткое время никакие химические связи просто не успевают образоваться, поэтому молекул воды с такими изотопами в природных условиях не существует, хотя молекулы таких вод могут быть получены в условиях современных ускорителей изотопов – в синхрофазотронах.
Если подсчитать все возможные изотопные разновидности воды, существующие в природе с общей формулой Н2О, то общее количество возможных тяжёлых вод
получится 18 (поскольку существует два стабильных изотопа водорода и три — кислорода). Из них 9 вариантов – нерадиоактивные (стабильные) и 9 радиоактивных с участием трития.
Стабильные:
Н2 16O, Н217O, Н218O, HD16O, HD17O, HD18O, D216O, D217O, D218O
Радиоактивные:
T216O, T217O, T218O, DT16O, DT17O, DT18O, HT16O, HT17O, HT18O
Таким образом, в природе возможно существование молекул воды, в которых содержатся любые из трех водородных изотопов (Н. D и Т) и 3 изотопа кислорода (17O и 18O) в любом сочетании. Однако 99,97% всей водs - в гидросфере представлено обычной водой химической формулы 1Н2160, доля тяжелой воды 2Н2160 составляет менее 0,02%. В среднем в природных водах в 10000 молекул содержится 9973 молекул H216O, 3 молекулы HD16O, 4 молекул H217O, 20 молекул H218O и около 2 молекул D216O. Еще реже, чем D216O, встречаются и девять радиоактивных естественных видов воды, содержащих тритий.
В составе воды природные изотопы водорода (Н и D) и кислорода (16O, 17O и 18O) образуют 9 конфигураций, 6 из которых образованы изотопами дейтерия - HD16O, HD17O, HD18O, D216O, D217O, D218O, и 3 конфигурации образованы изотопами кислорода - Н216O, Н217O, Н218O. В среднем, в природных водах в 10000 молекулах содержится 9973 молекул H216O, 3 молекулы HD16O, 4 молекулы H217O, 20 молекул H218O и около 2 молекул D216O. Физико-химические свойства изотопологов воды больше всего различаются для пар тяжелых изотопов 1Н/2Н, 1Н/3Н и в меньшей мере 16О/18О (Табл.).
Таблица. Изменение физических свойств воды при изотопном замещении
- Физические свойства; H216O; D216O; H218O
- Плотность при 20 °C, г/см3; 0,997; 1,105; 1,111
- Температура максимальной плотности, °C; 3,98; 11,24; 4,30
- Температура плавления при 1 атм, °C; 0; 3,81; 0,28
- Температура кипения при 1 атм, °C; 100,00; 101,42; 100,14
- Давление пара при 100 °C, Торр; 760,00; 721,60; 758,10
- Вязкость при 20 °C, сантипуаз; 1,002; 1,47; 1,056
Далее физико-химические свойства определяются строением молекулы воды. Электронная конфигурация атома кислорода обозначается 1s22s22р4. Число электронов в атоме кислорода равно сумме верхних индексов при обозначении sи p-орбиталей. S-орбитали у атома кислорода заняты полностью, на одной р-орбитали расположены два парных электрона, а двум 2p-орбиталям до заполнения не хватает 2 электронов. Согласно теории гибридизации атомных орбиталей и метода валентных связей (ВС), пара неспаренных валентных 2p-электронов атома кислорода, находящихся в состоянии sp3гибридизации, взаимодействует с каждым из 1s электронов двух атомов водорода, образуя молекулу воды. На двух других sp3-гибридных орбиталях атома кислорода расположены две несвязывающие (спаренные) электронные пары, не участвующих в образовании связи. Все четыре пары электронов занимают определенные области в пространстве вокруг центрального атома кислорода в молекуле. Из-за взаимного электростатического отталкивания между связывающими и несвязывающими электронными парами, молекула воды принимает симметричную V-образную форму (расстояние между атомами Н 1,515 Å) с длиной связи О-Н 0,96 Å и величиной угла между ковалентными связями Н–О–Н 104,270 (рис. 1,а). Отличительной особенностью ковалентной связи является ее полярность. Поскольку атом кислорода содержит в своем составе больше электронов, чем атом водорода (т. е. кислород более электроотрицательный, чем водород), электроны двух атомов водорода смещаются в сторону более электроотрицательного атома кислорода, в результате два положительных заряда атомов водорода компенсируются равным по величине двум атомов водорода отрицательным зарядом атома кислорода. Это приводит к тому, что около ядер водорода образуется недостаток, а около ядра кислорода - избыток электронной плотности. В результате этого происходит перераспределение электронной плотности: молекула воды поляризуется, принимая свойства электрического диполя (дипольный момент 1,85 дебая) с положительным и отрицательным зарядами на полюсах (рис. 1,б). Рассматривая молекулу Н2О в качестве диполя можно объяснить многие электрические свойства воды (дипольный момент, диэлектрическая проницаемость и др.) При соединении прямыми линиями центров положительных и отрицательных зарядов молекулы воды получается объемная геометрическая фигура - правильный тетраэдр, признанный базовой структурой молекулы воды (рис. 1,г). Данная структура молекулы воды, в которой 4 электронных sp3-орбитали центрального атома кислорода направлены к вершинам тетраэдра, лучше всего объясняет ее физико-химические свойства и распределение электронной плотности и поэтому используется в теоретических расчетах.

Рис. 1. Изображения структур воды в различных теоретических моделях: а) угловая; б) орбитальная; в) химическая; г) тетраэдрическая.
Аналогичные данные по строению молекулы воды дают современные квантомеханические расчеты молекулы Н2О методом молекулярных орбиталей (МО) (рис. 2,a,б). Комбинация 4-х атомных орбиталей атома кислорода (2s-, 2рх-, 2py, 2pz) и двух 1s-орбиталей атомов водорода приводит к формированию 6 гибридизированных
молекулярных орбиталей с различной энергией и симметрией: 2-х связывающих (2а1 и 1b1), двух несвязывающих (3а1 и 1b2) и 2-х разрыхляющих (4а1 и 2b1) орбиталях (рис. 2). 8 электронов атомов водорода и кислорода размещаются попарно на двух связывающих и двух несвязывающих орбиталях соответственно возрастанию энергетических уровней орбиталей:
(2а1св)2 (1b1св)2(3а1)2(1b2)2
При этом электроны на связывающих 2а1 и 1b1 орбиталях ответственны за формирование связи О-Н, а на несвязывающих (3а1 и 1b2) орбиталях соответствуют свободным электронным парам в молекуле Н2О, как это описывается методом валентных связей. Таким образом, оба метода расчета строения молекулы Н2О приводят к примерно одинаковым результатам по строению молекулы H2О. Их этого, в частности, следует, что молекула Н2О должна обладать диамагнитными свойствами, т. е. не обладает собственным магнитным моментом и поэтому выталкивается из магнитного поля. Принципиальным отличием метода молекулярных орбиталей от метода валентных связей является разная энергия молекулярных орбиталей, что подтверждается наличием у молекулы Н2О четырех потенциалов ионизации (в эВ) 27,3 (2а1-орбиталь), 16,2 (1b1-орбиталь), 14,5 (3а1-орбиталь) и 12,6 (1b2-орбиталь), соответственно.

Рис. 2. Схема расположения координатных осей (а) и энергетическая диаграмма орбиталей молекулы воды методом МО (б).
Следующий уровень химической организации определяется способностью молекул воды образовывать пространственно-направленые межмолекулярные водородные связи (О-Н…О) с соседними молекулами Н2О, связывающие их друг с другом в отдельные пространственые межмолекулярные ассоциаты, состав которых выражается общей формулой (H2O)n, где n = 3-21 и более (по последним данным сотни и даже тысячи единиц). Водородная связь имеет важное значение в химии межмолекулярных взаимодействий и обусловлена слабыми электростатическими силами и донорно-акцепторными взаимодействиями. Она возникает при взаимодействии электронодефицитного электронами атома водорода одной молекулы воды с неподеленной электронной парой атома кислорода соседней молекулы воды. Теоретически одна молекула воды может образовать до четырёх классических водородных связей с соседними молекулами воды, т. е. водородная связь обладает характером кооперативности.
Отличительной особенностью водородной связи является сравнительно низкая прочность; она в 5-10 раз слабее химической ковалентной связи. По энергии водородная связь занимает промежуточное положение между химическими связями и Ван-дер-ваальсовыми взаимодействиями, удерживающими молекулы в твердой или жидкой фазе. Энергия водородной связи составляет 5-10 ккал/моль, в то время как энергия ковалентной связи ОН связи в воде - 109 ккал/моль. В то же время энергия ковалентной O-H связи в 200 раз больше тепловой энергии. Поэтому, водородные связи в жидком состоянии относительно слабы и неустойчивы: предполагается, что они могут легко возникать и исчезать в результате тепловых флуктуаций. Это приводит к тому, что вода должна рассматриваться как ассоциированная жидкость: как пространственная сеть молекул H2O, соединённых водородными связями. При рассмотрении воды как простой совокупности молекул Н2О её удельный вес должен составлять 1,84 г/см3, а температура кипения 63,5 °С. Но, как известно из школьного курса химии, при нормальной температуре и давлении удельный вес воды равен 1 г/см3, а температура кипения воды 100°С. Если бы вода - гидрид кислорода - Н2О, была бы обычным мономолекулярным соединением, как ее аналоги по шестой группе Периодической системы элементов Д. И. Менделеева гидрид серы Н2S, гидрид селена Н2Se, гидрид теллура Н2Те, то в жидком состоянии вода существовала бы в диапазоне температур от –90 0С до –70 0С (рис. 3). Однако на практике этого не происходит из-за наличия водородных связей между молекулами воды.
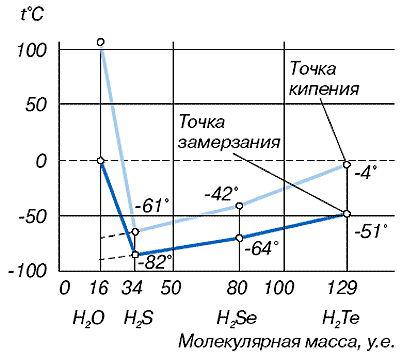
Рис. 3. Аномалии температур кипения и замерзания воды по сравнению с другими соединениями водорода
Поведение воды при охлаждении также аномально: вода сначала как другие жидкости: постепенно уплотняясь, уменьшает свой объем до +3,98 °С. При этой температуре вода имеет наибольшую плотность и наименьший объем (рис. 4). По этой причине лед не тонет, а остается на поверхности водоемов, надежно защищая обитателей водоема от замерзания - ведь его теплопроводность намного меньше, чем воды. Дальнейшее охлаждение воды до 0 0С постепенно приводит не к уменьшению, а к увеличению ее объема почти на 10 %, когда вода превращается в лед. Такое поведение воды свидетельствует об одновременном существовании 2 равновесных фаз – жидкой и квазикристаллической по аналогии с квазикристаллами, кристаллическая решетка которых имеет не только периодическое строение, но и обладает осями симметрии разных порядков, существование которых ранее противоречило представлениям кристаллографов. Эта теория, впервые выдвинутая известным отечественным физиком-теоретиком Я. И. Френкелем, основана на предположении, что часть молекул жидкости образует квазикристаллическую структуру, тогда как остальные молекулы являются газоподобными
, свободно движущимися по объему. Распределение молекул в малой окрестности любой фиксированной молекулы воды имеет определенную упорядоченность, несколько напоминающую кристаллическую, хотя и более рыхлую. По этой причине структуру жидкости иногда называют квазикристаллической или кристаллоподобной, т. е. обладающей симметрией и наличием упорядоченность во взаимном расположении атомов или молекул.
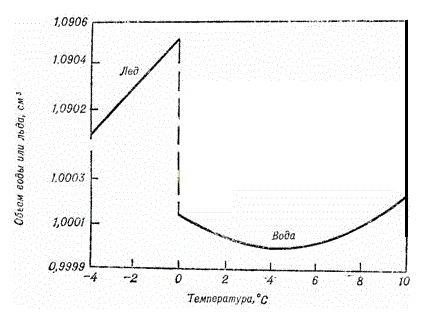
Рис. 4. Зависимость удельного объема льда и воды от температуры
Аномально высокая теплоемкость воды и теплопроводность также обеспечивается многочисленными водородными связями. При повышении температуры изменение теплоемкости воды понижается в пределах в интервале от 0 до 37 0С, при дальнейшем увеличении температуры теплоемкость возрастает. При этом в пределах температур, близким к физиологическим 37 °С, теплоемкость воды минимальна. Нормальная температура почти всех теплокровных живых организмов также находится вблизи этой точки. Таким образом, физика воды в области физиологических температур 35-41 °С констатирует вероятность достижения уникального состояния воды, когда массы квазикристаллической и жидкой воды равны между собой и способность одной структуры переходить в другую (вариабельность) - максимальная. Это свойство воды определяет равную вероятность протекания обратимых и необратимых биохимических реакций в организме человека, обеспечивая тем самым эффективную регуляцию метаболизма. Характерно, что явление прохождения теплоемкости воды через минимум при изменении температуры обладает своеобразной симметрией: при отрицательной температуре –200С теплоемкость воды также принимает минимальное значение.
Водородные связи также повышают температуру кипения, вязкость и поверхностное натяжение водных растворов. Это свойство проявляется в том, что вода всегда стремится сократить свою поверхность. Нескомпенсированные межмолекулярные силы наружного поверхностного слоя воды, вызванные квантовомеханическими силами, создают внешнюю пленку на поверхности воды, способную удерживать на поверхности воды различные мелкие предметы. Водородные связи ответственны за многие другие аномальные свойства воды, о которых я уже говорил (всего более 30). Более подробно обо всем этом читайте в статье О. В. Мосина Строение воды и физическая реальность
(Журнал Сознание и физическая реальность
, 2011, № 11, с. 16-32).