Изучение уровней включения изотопов 2Ни 13С в аминокислоты суммарных белков метилотрофных бактерий
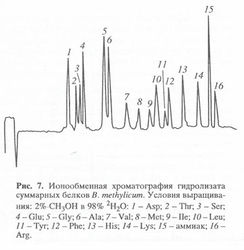
2Ни 13С-меченные аминокислоты в составе гидролизатов белка биомассы были получены в условиях, аналогичных таковым для секретируемых аминокислот (табл. 4). Хотя в таблице 4 приведены данные только для 10 аминокислот, не вызывает сомнения, что в остальных аминокислотах уровни изотопного включения сопоставимы, хотя они не детектируются данным методом. Это предположение подтверждается данными по разделению белковых гидролизатов метилотрофных бактерий методом ионнообменной хроматографии, где детектируется уже 16 аминокислот (см. рис. 3).
В экспериментах по получению аминокислот за счёт биоконверсии 13СН3ОН метилотрофными бактериями M. flagellatum была показана эффективность мечения аминокислот 13С. Так, в фенилаланине детектировалось 80,5 % метки, в аланине - 95 %, в глицине - 90% (см. табл. 4).
Таблица 4.
Уровни включения 2Н и 13С в аминокислоты общих белков биомассы B. methylicum и M. flagellatum (данные получены для Z-и Dns-производных аминокислот*).
- Аминокислоты; Содержание 2Н2О в среде, об% 24,5 49,5 73,5 98,0; 1 % 13СН3ОН
- Глицин; 15,0; 35,0; 50,0; 90,0; 90,0
- Аланин; 20,0; 45,0; 62,5; 97,5; 95,0
- Валин; 15,0; 36,3; 50,0; 50,0; 50,0
- лейцин (изолейцин); 10,0; 42,0; 45,0; 49,0; 49,0
- фенилаланин; 24,5; 37,5; 50,0; 95,0; 80,5
- тирозин; 20,0; 48,8; 68,8; 92,8; 53,5
- Серин; 15,0; 36,7; 47,6; 86,6; 73,3
- аспарагиновая кислота; 20,0; 36,7; 60,0; 66,6; 33,3
- глутаминовая кислота; 20,0; 40,0; 53,4; 70,0; 40,0
- Лизин; 10,0; 21,1; 40,0; 58,9; 54,4
*Данные по включению 2Н в аминокислоты приведены для B. methylicum при росте на средах, содержащих 2 об.% CH3OH и 24,5; 49,5; 73,5; 98,0 об.% 2Н2О.
Данные по включению 13С приведены для M. flagellatum при росте на среде, содержащей 1 об.% 13СН3ОН и 99 об.% Н2О.
Во всех экспериментах уровни включения 2Н и 13С в метаболически связанных аминокислотах обнаружили определённую коррелляцию. Так, уровни изотопного обогащения валина и лейцина, фенилаланина и тирозина совпадают (см. табл. 4). Уровни изотопного включения в глицине и серине, аспарагиновой и в глутаминовой кислотах также имеют близкие величины. Сравнивая данные таблицы 3 и 4 можно заключить, что уровни изотопного обогащения секретируемых аминокислот и соответствующих аминокислотных остатков суммарного белка в целом также коррелируют. Причина некоторых наблюдаемых расхождений в уровни включения изотопов в аминокислоты до конца не выяснена.
Как и в случае с секретируемыми аминокислотами, при росте бактерий на средах, содержащих 98 об.% 2Н2О или 1 об.% 13СН3ОН, низкие уровни включения 2Ни 13С в остатки лейцина (изолейцина) и метаболически связанные с ним аминокислоты, обусловлены ауксотрофностью бактерий в лейцине (изолейцине).