Солёная вода и полив растений
Вопрос:
Ситуация следующая: Мы с мужем живём в Арабских эмиратах у нас большой сад, где мы выращиваем тропические деревья : манго, банановые, финиковые и другие пальмы. С недавних пор начали заниматься продажей саженцев. Вопрос одного из клиентов поставил меня в тупик. Местность наша - на берегу океана, поэтому даже пресная подземная вода из скважин содержит соли. Какая допустимая концентрация соли в воде должна быть для полива таких деревьев? Сможете ли вы мне помочь с этим вопросом или Вы сможете подсказать, где я могу найти такого рода информацию? Спасибо заранее. Ирина.
Ответ:

Вода - прекрасный растворитель; поэтому в природе нет вод, которые не содержали бы некоторого количества каких-либо веществ. Даже кристально чистый ручеёк — и тот содержит в своей воде какие-нибудь растворённые вещества. От растворённых веществ и зависит вкус воды разных источников.
Солёность воды — это количество твёрдых солей (в основном хлорида натрия NaCl) в граммах, растворённое в 1 кг морской воды.
Измерить солёность воды можно несколькими способами: по плотности с помощью специального прибора ариометра, по водородному показателю среды с помощью рН-метра (оптимальная кислотность - 8,0 - 8,5 pH), или по электропроводности, определённой прибором солемером при заданной температуре.
Вода для полива растений не должна иметь высокую концентрацию солей. Ниже приводится оценка воды по электропроводности по Зонневельду:
1. ниже 0,75 мСм/см - хорошая,
2. 0,75 – 1,5 мСм/см - пригодная,
3. 1,5 – 2.25 мСм/см - концентрация солей высокая,
4. выше 2,25 мСм/см - концентрация солей очень высокая.
Для полива растений лучше использовать воду с ЕС 0,75-1,5 мСм/см. Если вы вынуждены работать с водой, ЕС которой находится в пределах 1,5-2.25 мСм/см, то очень правильно надо подойти к вопросу выбора субстрата. Основное требование, которое надо при этом учесть – возможность его промывки в случае накопления солей. В этом случае предпочтение лучше отдать инертным субстратам, таким как минеральная вата, кокос, перлит. Если предпочтение отдается торфяным субстратам, то надо предусмотреть добавление до 50% перлита. Вода с высокой и очень высокой концентрацией солей не может быть использована в теплицах без предварительной очистки от солей. Учитывая важность качества поливной воды при поливе, возрастает необходимость периодических анализов поливной воды и корректировки ее показателей.
В природных условиях вода всегда содержит растворенные соли, газы и органические вещества. Их количество и состав могут меняться в очень широких пределах. При концентрации солей до 1 г/кг воду считают пресной, до 25 г/кг - солоноватой, свыше - соленой. Соленость воды в Океане колеблется около 35 г/кг. Соленость морской воды может быть как ниже, так и выше этой величины. Максимальные концентрации солей наблюдаются в соляных озерах (до 300 г/кг) и в глубокозалегающих подземных водах (до 600 г/кг).
Обычно на 1000 граммов океанской воды приходится 35 граммов растворённых веществ — различных солей. Солёность морской воды принято считать не в процентах, т. е. в сотых долях, а в промиллях, т. е. в тысячных долях. Таким образом, солёность океанской воды будет равна 35 промиллям, и обозначается это так: 35 %. Состав солей воды океанов везде почти одинаков. Таким образом, оптимальная соленость морской воды составляет в пересчёте на твёрдый хлорид натрия NaCl 35 грамм соли на 1 л. пресной воды, что соответствует концентрации соли примерно 35 ppt (35 частей на одну тысячу).

Океанская и пресная воды по составу растворённых в них веществ совершенно различны. В морях и океанах главную часть составляют хлориды — соли соляной кислоты (например, поваренная соль и др.), а в водах рек — карбонаты — соли угольной кислоты (например, мел, известняк и др.). В составе солей океанской воды хлориды составляют около 90 процентов, а карбонаты всего 0,3 процента. В речной воде солевой состав совсем другой: карбонаты здесь составляют 60 процентов, а хлориды лишь 5 процентов. Кроме этих веществ, морская и пресная воды содержат ещё в больших количествах соли серной кислоты — сульфаты (например, гипс, алебастр, глауберову соль и др.).
Соли попали в воду океана одновременно с возникновением самих океанов. Образование земной коры происходило при высоких температурах. Различные вещества в виде газов выделялись из земли и носились тогда в атмосфере. Последующее охлаждение земной коры вызвало обильные дожди. Они захватывали с собой те вещества, которые носились в атмосфере. Таким образом, «очистилась» атмосфера молодой Земли, а воды, заполнившие огромные котловины на её поверхности, оказались солёными. Солёность вод мирового океана такая же древняя, как и сам океан. И действительно, все самые древние ископаемые водные животные являются морскими организмами, жившими в солёной воде.
Опресняющая же роль современных рек, которые вносят воду с материков в моря и океаны, ничтожна. Реки дают только 30 000 кубических километров пресной воды в год. Это ничтожно мало по сравнению с общим объёмом океанов и морей. Солёность морской воды приносит много неприятностей. Поэтому в островных странах, например, на Кипре морскую воду опресняют специальными опреснителями. В них морскую воду выпаривают, а собираемый пар, охлаждаясь, даёт желанную пресную воду. Изобретены также химические опреснители и специальные фильтры. Но они пока достаточно дорогие.
Вода - матрица жизни всех живых существ, основа обмена веществ, изменяя свою структуру, свои физико-химические свойства, она регулирует жизненные процессы. Без воды невозможны любые формы жизни. С водой связаны и синтез веществ, и процессы дыхания, и разложения сложных соединений, которые проходят в клетках всех живых организмов. В процессе жизнедеятельности постоянно расходуются одни вещества и образуются другие. Часть вновь образовавшихся молекул остается в клетке, часть транспортируется в другие клетки или выводится в окружающую среду. Для обеспечения процесса жизнедеятельности необходим постоянный подвод исходных составляющих и отвод из клетки побочных продуктов, образовавшихся в ходе биохимических реакций.
Транспорт молекул воды осуществляется по специально организованным передающим тканям. Перед тем, как попасть в клетку или выйти из нее, все вещества должны пройти через клеточную мембрану, отделяющую клетку от внешней среды. Процессы обмена веществ на мембранах тесно связаны с химическим составом воды. Содержание различных солей оказывает влияние на то, какие вещества и в каких количествах будут поступать в клетку или выходить из нее. Продукты, необходимые для жизнедеятельности организма, обычно транспортируются через мембрану в виде заряженных ионов. Транспорт может осуществляться активно — с использованием богатых энергией соединений или пассивно, за счет собственной кинетической энергии ионов. Пассивный транспорт — диффузия различных ионов через мембрану — осуществляется с разной скоростью. Относительная способность разных ионов диффундировать через мембрану определяет коэффициент проницаемости Р. Легче других проникает через мембраны ион К+, поэтому значение Р для К+ условно принимают за 1,0. У водоросли Nitella коэффициент проницаемости для ионов Na+ и Cl‾ равны 0,18 и 0,033 соответственно. Скорость проникновения ионов через мембрану зависит также от разности концентраций данного иона по обе стороны мембраны. Чем больше разность концентраций, тем больше ионов диффундирует в сторону меньшего их содержания. Кроме диффузии, идущей за счет разницы концентраций, существует активный транспорт ионов, при котором движение осуществляется за счет разности электрохимических потенциалов через специальные участки мембраны. Это движение может осуществляться и от меньшей концентрации к большей. Движущей силой процесса в этом случае является запас энергии в форме молекул АТФ.
Упрощенно структура живой клетки выглядит следующим образом: внутри клеточной стенки (сравнительно жесткого образования) располагается протопласт (живая часть клетки), в котором заключены все клеточные организмы, находящиеся в сложном растворе — цитоплазме. Клетки простейших бактерий (прокариот), животных (эукариот) и растений представлены на рисунках ниже.
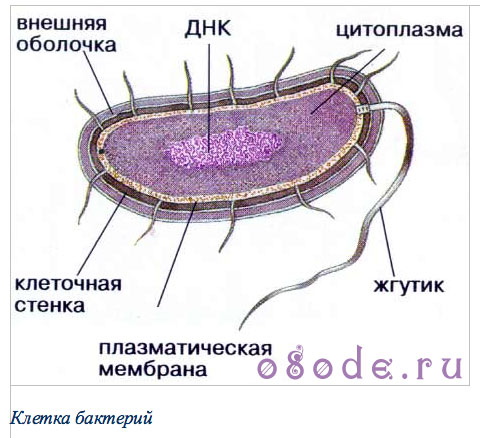
Клетка бактерий
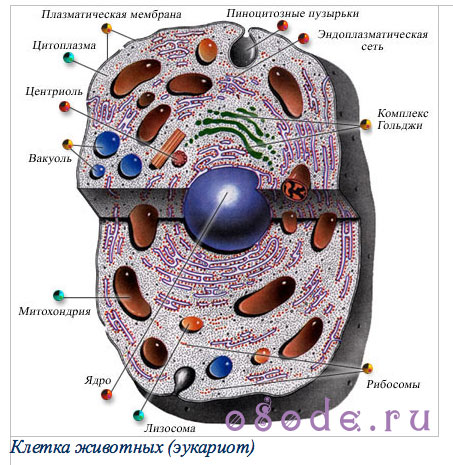
Клетка животных (эукариот)
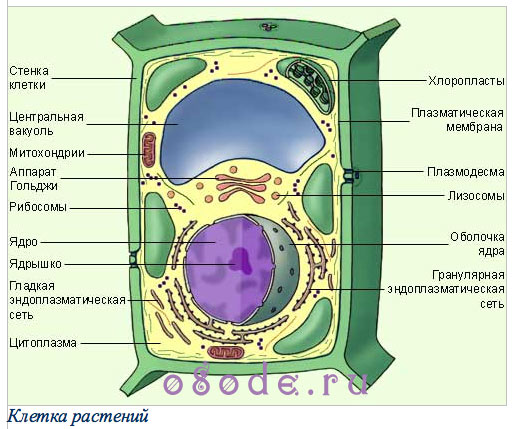
Клетка растений
Клеточная стенка имеет избирательную проницаемость для различных ионов, то есть различные вещества проникают сквозь мембрану с разными скоростями. Это определяется их различной растворимостью отдельных составляющих мембраны и различными скоростями перекачивания при активном транспорте. В результате образуется неравномерное распределение ряда веществ по обе стороны мембраны. Клетки растений активно накачивают калий, а близкий к нему натрий, наоборот, выталкивается в окружающую среду. Из-за более высоких концентраций некоторых ионов внутри клетки создается осмотическое (диффузное) давление, характеризующее стремление раствора, отторгнутого мембраной, к снижению концентрации (разбавлению). Осмотическое давление может достичь десятков атмосфер. Это давление создает напряженное состояние клеточной оболочки.
Напряжение мембраны зависит также от внешнего раствора. В зависимости от отношения осмотического давления внешнего раствора к давлению в клетке растворы подразделяются на три группы. Изотонические — в них разница давлений невелика (менее 0,5—1,0 атм); гипертонические — их давление выше, чем в клетке; противоположные им — гипотонические. Если клетка находится в гипертоническом растворе, то из нее происходит откачка воды, что приводит к уменьшению размера клетки и сжатию мембраны. Из гипотонических растворов вода поступает в клетки, что приводит к их набуханию (вплоть до разрыва мембраны) и потере части активных веществ.
Совокупность процессов регулирования осмотического давления жидкостей организма носит название осморегуляция. Этот процесс обнаружен у большинства организмов. У пресноводных рыб вода вместе с содержащимися в ней солями активно поступает в клетки через поверхность тела и жабры и выводится из организма через почки. У солоноводных рыб попавшая в организм вода выводится через кожные покровы, a NaCl выводится главным образом через жабры за счет специальных желез. Водные растения и пресноводные рыбы удовлетворяют потребность организма в ионах, поглощая их непосредственно из воды. Если она не содержит необходимые элементы, то при нормальном соотношении осмотических давлений происходит изменение содержания отдельных элементов, то есть изменение отношения ионов в организме. В ряде случаев это приводит к нарушению биохимических процессов.
В ходе экспериментов с пресноводными рыбами обнаружено, что они неплохо переносят изотонические растворы, полученные разбавлением морской воды, в то время как гипотонические растворы одной из солей — калия, магния, натрия или кальция — действовали смертельно. Был получен ряд токсичности ионов основных металлов:
Na+ < Ca2+, Mg2+ < K+
Опыты показали, что воздействие на рыб оказывает содержание Na+ в крови. При повышении концентрации Na+ в воде соответственно увеличивается его содержание в крови, а содержание К+ уменьшается. При повышении концентрации калия происходит обогащение организма натрием. Так что калий оказывает косвенное токсическое воздействие. Обогащение рыб натрием дифференцировано в зависимости от пола рыбы. Кровь самок быстрее обогащается натрием (возможно за счет реакции яичников).
При поглощении Na+ требуется большое количество энергии. При ассимиляции Na+ организмом происходит его замещение на NH4+. Аммоний может выделяться организмом из органических азотсодержащих соединений. Таким образом, повышенное потребление натрия приводит к нарушению белкового обмена. У растений повышение концентрации натрия приводит к блокаде поступления ионов калия через мембраны клеток. Растение может испытывать калийное голодание даже при достаточно высоком абсолютном содержании калия.
Анионы также имеют различное воздействие на обитателей. Так, нитраты для рыб значительно более ядовиты, чем хлориды. Для растений наиболее токсичны хлорид-ионы Cl‾, затем следуют сульфати карбонат-ионы (SO42‾ и СO32‾).
Кроме осмотического давления и абсолютного содержания того или иного иона в воде большое физиологическое значение имеет соотношение ионов, растворенных в воде. В первую очередь это относится к четырем ионам: K+ и Na+, Mg2+ и Са2+. Эти ионы попарно близки по химическим свойствам, и поэтому относительно транспорта через мембраны клеток являются антагонистами. Повышение относительной концентрации одного из ионов приводит к снижению поступления в клетку другого. Большинство природных вод имеет приблизительно равное суммарное содержание одновалентных и двухвалентных ионов. К такому соотношению приспособлены процессы жизнедеятельности водных организмов. Конечно, в различных регионах земного шара состав воды различен, но организмы имеют возможность приспосабливаться к некоторым изменениям химического состава.
Разные виды флоры и фауны чувствительны к различным концентрациям соли в среде обитания. Существуют морские, солоноватые и пресноводные виды растений и животных, а некоторые микроорганизмы – галофильные бактерии, обитающие в тёплых водах Мёртвого моря способны жить и размножаться при 30 %-ной концентрации соли в среде.
Проблема адаптации организмов к солёной воде связана с осморегуляцией. Соленость внутриклеточной среды организма, оптимальная для его жизнедеятельности, более или менее постоянна, причем невелика (7-10 % или около 1 %). Почти во всех случаях жизни соленость организма иная, чем у среды. В пресной воде животное более соленое, чем вода (гиперосмотично), в морской – менее соленое (гипоосмотично). Возникает осмотическое давление и связанные с ним проблемы. В пресной воде через покровы животного постоянно просачивается вода, и оно распухает. А если ее интенсивно удалять, вместе с ней выводятся растворенные ионы, а добыть новые трудно. Наоборот, в морской воде вода уходит через покровы, и тело съеживается, а глотание воды приводит к поглощению большого количества солей, и с ними надо что-то делать. Если говорить проще, то пресная вода стремится организм опреснить, а соленая – засолить. И все морские организмы эту проблему вынуждены решать различными способами. Первый, наиболее логичный - сделать покровы непроницаемыми. Это называется осмоизоляция, что на практике недостижимо. Гораздо лучше и эффективнее - использование активного транспорта ионов для изменения солености. Живые клетки умеют это делать, хотя и с затратой энергии. Более того: специально обученные белки могут захватывать и перемещать через мембрану избранные ионы (например, Na), причем даже против градиента их концентрации. И вот этот инструмент оказывается главным. Вот несколько наиболее распространенных типов ферментов, обеспечивающих направленный транспорт и накопление ионов в живых клетках.
Фермент Na-K-ATPаза обеспечивает перемещение Na+ из клеток в обмен на K+, поступающий в клетку. Этот фермент особенно активен в клетках жабер, почек, кишечнике, ректальной и солевой железах. В обмен на три выведенных иона Na+ в клетку обеспечивает поступление двух ионов K+, при этом гидролизуется одна молекула АТФ. В результате соотношение калия и натрия в клетке может достигать 10:1.
H-K-ATPаза обычно входит в кислый секрет желудочно-кишечного тракта и обеспечивает транспорт H+ из клеток в обмен на K+, поступающий в клетки (то есть обеспечивает повышенную кислотность внеклеточной среды.
Ca-ATPаза обеспечивает вынос Ca++ из клетки. Ее работа поддерживает низкий уровень кальция в цитоплазме, что позволяет использовать кальций в качестве сигнального элемента. Внутриклеточное содержание кальция составляет в среднем 10-7 – 10-6 М, притом что внеклеточное может достигать 10-3 М.
В пресной и морской воде должны работать разные системы водно-солевой регуляции. В таблице приведена способность к осморегуляции для различных организмов. Для кишечнополостных, иглокожих и полихет разница между внешней и внутренней солёностью составляет обычно 0.2-0.5 %, для моллюсков 1-3 %, для раков и личинок насекомых с водным дыханием 3-10%, для морских рыб – достигает 20-25‰ (у пресноводных рыб находится в пределах 5-10 %). Оптимальная для жизнедеятельности внутренняя соленость – 7-10 %. Поэтому пресноводным животным (с внешней соленостью 0) достичь ее заметно легче, чем морским (с внешней соленостью 33).
Таблица. Способности к осморегуляции у разных организмов.
морские виды
общая соленость, г/л
разница внешней и внутренней солености, г/л
Морская вода
34,0
Медуза Aurelia
33,2
0,7
Морской еж Echinus
33,7
0,2
Пескожил Arenicola
33,7
0,2
Мидия Mytilus
37,2
3,2
Креветка Palaemon
25,5
8,5
Акула Raja
15,4
18,6
Мурена
11,8
22,2
Скумбрия
10,6
23,4
пресноводные виды
общая соленость, г/л
разница внешней и внутренней солености, г/л
Пресная вода
0,15
Беззубка Anodonta
1,2
1,1
Водяной ослик Asellus
7,8
7,7
Мотыль Chironomus
3,2
3,1
Личинка комара Aedes
4,2
4,1
Лосось Salmo
8,5
8,4
Рекордсмены по устойчивости к солёности среди животных – это листоногие раки – жаброноги Artemia salina. Мощные системы прокачки ионов на жабрах позволяют им жить при практически любой солености – от 0 до 100%. Причем даже в условиях быстро меняющейся солености. Несколько менее известные, но также продвинутые осморегуляторы – личинки комаров Chironomus salinarius и Aedes caspius (они выносят от 0 до 60-70‰). Наконец, в соленых озерах (и даже лужах) поселяются взрослые водные жуки и клопы – довольно много видов, обитающих именно в таких водоемам. Но им, с их воздушным дыханием, перестроиться проще.
Насекомые и раки вообще достигли огромных успехов в создании покровов, через которые проходит кислород и углекислота (то есть можно дышать), но не проходит все остальное. Это, если подумать, замечательный путь приспособолений не только для осморегуляции – еще для наземного обезвоживания, а заодно защиты от токсикантов. Например, личинки слепней часами спокойно живут в формалине практически любой концентрации; только 96-й этанол фиксирует их.
Еще одна адаптация к солёности среди организмов – так называемый солевой анабиоз, наступающий при сильном, но временном повышении солености (например, в тех же соленых озерах во время засухи). Некоторые мелкие беспозвоночные умеют при этом, потеряв до половины внутренней воды, скукожиться и как бы окуклиться на несколько дней или даже недель. Такое известно для ряда простейших, нескольких коловраток, даже полихет (Nereis diversicolor, Fabricia sabella) и гарпактицид (Harpacticus fulvus).
Относительно растений, то это солончаковые растения и микроводоросли, способные выдерживать концентрации хлорида натрия от 30% и выше.
Ниже на диаграмме показана обобщенная картина изменения разнообразия жизни при различном градиенте солености. Существуют два пика разнообразия – острый пресноводный, при солености 0-5 %, и несколько более размазанный морской, при солености 20-40 %. Между ними – провал, заполненный узкой прослойкой солоноватоводных видов). Справа от морского пика наблюдается быстрый спад, а дальше весь оставшийся диапазон солености принадлежит немногим видам пресноводного происхождения.
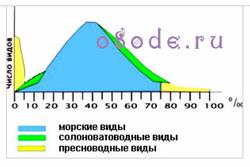
Диаграмма изменения разнообразия жизни при различном градиенте солености.
Верхним пределом распространения животных считается соленость около 20 %, бактерий – около 30 %.
Таким образом, суммируя вышесказанное, в качестве питьевой воды и воды для полива растений пригодна вода с концентрацией солей от 100 мг/кг до 1000 мг/кг. Оптимальным значением соли является концентрация 500 мг/кг при значении кислотно-щелочного баланса pH=6-8. Чтобы максимально обессолить и сделать более пригодным воду для полива растений можно удалить присутствующие в ней соли методом замораживания-оттаивания воды, о чём уже неоднократно сообщалось на нашем сайте. Или можно попробовать следующую несложную процедуру. Налейте воду в большую ёмкость и прокипятите её. Затем остудите её желательно при низкой температуре (при этом часть солей выпадет в осадок) и берите для полива только верхнюю треть воды, остальные две трети слейте в канализацию. Там осталась максимальная концентрация солей, не полезных вашим растениям. При незначительной жесткости достаточно прокипятить воду в течение 5-10 минут. Соли выпадут в осадок и останутся накипью на посуде. Но будьте аккуратны при поливе такой водой растений, поскольку при кипячении содержание кислорода в воде уменьшается.
Более подробно про то, какую воду лучше использовать для полива растений смотрите на нашем сайте по этой ссылке: /article/answer/voda_dla_poliva_ractenii.htm
С уважением,
к.х.н. О.В. Мосин
очень информационно качественный и понятный обзор. Большое спасибо за работу